一定温度下,某反应达平衡,平衡常数K= 。保持容器容积不变,升高温度,H2浓度减小,则下列说法
。保持容器容积不变,升高温度,H2浓度减小,则下列说法不正确 的是
 。保持容器容积不变,升高温度,H2浓度减小,则下列说法
。保持容器容积不变,升高温度,H2浓度减小,则下列说法| A.该反应的焓变为正值 |
| B.恒温恒容下,再充入CO2气体,H2浓度一定减小 |
| C.升高温度,会使正反应速率增大,逆反应速率减小,平衡正移 |
D.该反应化学方程式为CO2+H2 CO+H2O CO+H2O |
18-19高二上·北京·期中 查看更多[3]
(已下线)专题2.2.2 化学平衡常数(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)山东省枣庄市滕州市第一中学2019-2020高二上学期期末考试化学试题北京市第一七一中学2018-2019学年高二上学期期中考试化学试题
更新时间:2018-11-19 14:43:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关说法正确的是
| A.吸热反应一定不可以自发进行 |
| B.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 |
| C.NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) △H=+185.57KJ/mol,能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
D.N2(g)+3H2(g) 2NH3(g)△H<0,其他条件不变时升高温度,反应速率V(H2),平衡逆移,氢气的平衡转化率均减小 2NH3(g)△H<0,其他条件不变时升高温度,反应速率V(H2),平衡逆移,氢气的平衡转化率均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于可逆反应A(g) + 2B(g)⇌2C(g) △H<0,达到平衡时,要是正反应速率增大,且使A的转化率增大,以下的措施可行的是
| A.降低温度 | B.增大B的浓度 | C.减小C的浓度 | D.加入催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定条件下的密闭容器中:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-905.9 kJ·mol-1,下列叙述正确的是
4NO(g)+6H2O(g) ΔH=-905.9 kJ·mol-1,下列叙述正确的是
 4NO(g)+6H2O(g) ΔH=-905.9 kJ·mol-1,下列叙述正确的是
4NO(g)+6H2O(g) ΔH=-905.9 kJ·mol-1,下列叙述正确的是| A.平衡后升高温度,混合气体中NO含量增大 |
| B.平衡后降低压强,混合气体平均摩尔质量增大 |
| C.4molNH3和5molO2反应,达到平衡时放出热量为905.9kJ |
| D.平衡时,将水蒸气移除部分,此时逆反应速率降低,正反应速率不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在高温或放电条件下, 与
与 反应生成NO,NO进一步氧化生成
反应生成NO,NO进一步氧化生成 。
。
 。大气中过量的
。大气中过量的 和水体中过量的
和水体中过量的 、
、 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为
均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为 ,也可将水体中的
,也可将水体中的 转化为
转化为 。对于反应
。对于反应 ,下列说法正确的是
,下列说法正确的是
 与
与 反应生成NO,NO进一步氧化生成
反应生成NO,NO进一步氧化生成 。
。
 。大气中过量的
。大气中过量的 和水体中过量的
和水体中过量的 、
、 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为
均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为 ,也可将水体中的
,也可将水体中的 转化为
转化为 。对于反应
。对于反应 ,下列说法正确的是
,下列说法正确的是A.其他条件相同,增大 ,NO的转化率下降 ,NO的转化率下降 |
B.反应的平衡常数可表示为 |
| C.使用高效催化剂能降低反应的焓变 |
D.该反应的 , , |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】Burns和Dainton研究发现C12与CO合成COCl2的反应机理如下:
①C12(g) 2C1•(g)快
2C1•(g)快
②CO(g)+C1•(g) COC1•(g)快
COC1•(g)快
③COC1•(g)+C12(g) COC12(g)+C1•(g)慢
COC12(g)+C1•(g)慢
其中反应②存在v正=k正[CO][C1•]、v逆=k逆[COC1•]
下列说法正确的是( )
①C12(g)
 2C1•(g)快
2C1•(g)快②CO(g)+C1•(g)
 COC1•(g)快
COC1•(g)快③COC1•(g)+C12(g)
 COC12(g)+C1•(g)慢
COC12(g)+C1•(g)慢其中反应②存在v正=k正[CO][C1•]、v逆=k逆[COC1•]
下列说法正确的是( )
| A.反应①的活化能大于反应③的 |
B.反应②的平衡常数K=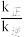 |
| C.要提高合成COCl2的速率,关键是提高反应②的速率 |
| D.选择合适的催化剂能加快该反应的速率,并提高COC12的平衡产率 |
您最近一年使用:0次

 H2(g)+I2(g)平衡体系增加压强使颜色变深
H2(g)+I2(g)平衡体系增加压强使颜色变深

