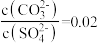下列说法正确的是
| A.0.1molAgCl和0.1 molAgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) |
| B.常温下,向饱和CaCO3溶液中加入Na2CO3粉末,CaCO3的溶解度不变 |
| C.25 ℃时,Ksp[ Mg(OH)2 ]=5.61 × 10-12、Ksp(MgF2)=7.12 ×10-11,该温度下饱和 Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+) 大 |
| D.常温下Ksp(Ag2SO4)=1. 4× 10-5,向10mL 0.1mol/L的Na2SO4溶液中加入10 mL0.1 mol/L的AgNO3溶液,有白色沉淀生成 |
更新时间:2019-01-30 12:57:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定温度下,两种钙盐的沉淀溶解平衡曲线如图所示(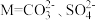 ,p表示以10为底的负对数)。已知:相同温度下,碳酸钙比硫酸钙更难溶。下列说法错误的是
,p表示以10为底的负对数)。已知:相同温度下,碳酸钙比硫酸钙更难溶。下列说法错误的是
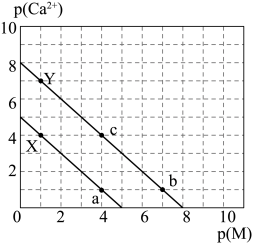
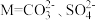 ,p表示以10为底的负对数)。已知:相同温度下,碳酸钙比硫酸钙更难溶。下列说法错误的是
,p表示以10为底的负对数)。已知:相同温度下,碳酸钙比硫酸钙更难溶。下列说法错误的是
A.该温度下,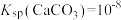 |
B.欲使反应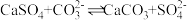 正向进行,需满足 正向进行,需满足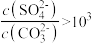 |
C.欲使c点移动到b点,可向c点的饱和溶液中加入适量 固体 固体 |
D.生活中,用饱和碳酸钠溶液浸泡硫酸钙后的滤液中一定存在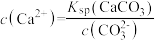 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】难溶盐CaCO3在下列溶液中溶解度最大的是( )
| A.0.1 mol·L-1CH3COOH | B.0.10 mol·L-1CaSO4 | C.纯水 | D.1.0 mol·L-1Na2CO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法不正确的是
A.用碳酸钠溶液处理锅炉水垢:CaSO4(s)+CO ⇌CaCO3(s)+SO ⇌CaCO3(s)+SO |
B.湿润的淀粉碘化钾试纸遇氯气变蓝:3Cl2+I-+3H2O=6Cl-+IO +6H+ +6H+ |
C.铝粉和氧化铁组成的铝热剂用于焊接钢轨:2Al+Fe2O3 Al2O3+2Fe Al2O3+2Fe |
| D.淡黄色的过氧化钠敞口放置变成白色:2Na2O2+2CO2=2Na2CO3+O2;2Na2O2+2H2O=4NaOH+O2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温时,下列各溶液的叙述中正确的是
| A.将AgCl与AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,析出的AgCl沉淀少于AgBr沉淀 |
| B.已知酸性:HF>CH3COOH,pH相等的NaF与CH3COOK溶液中:[c(Na+)-c(F-)]<[c(K+)-c(CH3COO-) ] |
| C.0.1mol/L的氨水的pH=a,0.01mol/L的氨水的pH=b,则a-1>b |
| D.0.10mol·L-1CH3COONa溶液中通入HCl至溶液的pH恰好等于7,则c(Na+)>c(CH3COOH)=c(Cl-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作及现象和所得结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用干燥的pH试纸测 溶液和 溶液和 溶液的pH 溶液的pH | 醋酸钠溶液约为9, 溶液约为8 溶液约为8 |  电离出 电离出 的能力比 的能力比 的强 的强 |
| B | 向 与MgO混合物中加入足量NaOH溶液 与MgO混合物中加入足量NaOH溶液 | 固体部分溶解 | 可用NaOH溶液除去MgO中混有的 |
| C | 向等体积等浓度的稀硫酸中分别加入少量等物质的量的ZnS和CuS固体 | ZnS溶解而CuS不溶解 |  |
| D | 相同条件下,分别测量0.1mol/L和0.01mol/L醋酸溶液的导电性 | 前者的导电性强 | 醋酸浓度越大,电离程度越大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关说法正确的是
| A.向20mL0.5mol/LFeBr2(ap)中通入224mLCl2(标准状况):2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| B.25℃时,向2mL0.1mol﹒L-1Na2S溶液中滴入几滴0.1mol﹒L-1ZnSO4溶液,有白色沉淀生成;再滴加几滴0.1mol﹒L-1CuSO4溶液,则又有黑色沉淀生成,可以得出结论:Ksp(ZnS)>Ksp(CuS) |
| C.向30mL0.5mol/LNaOH(aq)中通入224mLCO2(标准状况):3OH-+2CO2=CO32-+HCO3-+H2O |
| D.已知25℃时,CH3COOH的Ka=1.8×10-5,HClO的Ka=3.0×10-8,等浓度的CH3COONa和NaClO溶液混合后,溶液中各离子浓度的大小关系是:C(Na+)> C(ClO-)> C(CH3COO-)> C(OH-)> C(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】向湿法炼锌的电解液中同时加入Cu和CuSO4,可生成CuCl沉淀除去Cl-,降低对电解的影响,反应原理如下:
Cu(s)+Cu2+(aq) 2Cu+(aq) ΔH1=a kJ·mol-1
2Cu+(aq) ΔH1=a kJ·mol-1
Cl—(aq)+Cu+(aq) CuCl(s) ΔH2=b kJ·mol-1
CuCl(s) ΔH2=b kJ·mol-1
实验测得电解液pH对溶液中残留c(Cl-)的影响如图所示。下列说法正确的是

Cu(s)+Cu2+(aq)
 2Cu+(aq) ΔH1=a kJ·mol-1
2Cu+(aq) ΔH1=a kJ·mol-1Cl—(aq)+Cu+(aq)
 CuCl(s) ΔH2=b kJ·mol-1
CuCl(s) ΔH2=b kJ·mol-1实验测得电解液pH对溶液中残留c(Cl-)的影响如图所示。下列说法正确的是

| A.向电解液中加入稀硫酸,有利于Cl-的去除 |
| B.溶液pH越大,Ksp(CuCl)增大 |
| C.反应达到平衡增大c(Cu2+),c(Cl-)减小 |
D.1/2 Cu(s)+ 1/2 Cu2+(aq)+Cl-(aq) CuCl(s) ΔH=(a+2b) kJ·mol-1 CuCl(s) ΔH=(a+2b) kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知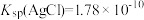 ,
,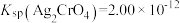 。在只含有KCl、
。在只含有KCl、 的混合溶液中滴加
的混合溶液中滴加 的
的 溶液,当AgCl与
溶液,当AgCl与 共存时,测得溶液中
共存时,测得溶液中 的浓度是
的浓度是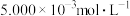 ,此时溶液中
,此时溶液中 的物质的量浓度是
的物质的量浓度是
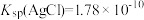 ,
,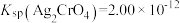 。在只含有KCl、
。在只含有KCl、 的混合溶液中滴加
的混合溶液中滴加 的
的 溶液,当AgCl与
溶液,当AgCl与 共存时,测得溶液中
共存时,测得溶液中 的浓度是
的浓度是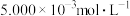 ,此时溶液中
,此时溶液中 的物质的量浓度是
的物质的量浓度是A. | B.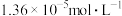 |
C.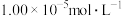 | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】T℃时,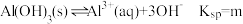 。当
。当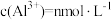 时,溶液的pH等于(已知:该温度下,水的离子积常数
时,溶液的pH等于(已知:该温度下,水的离子积常数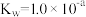 )
)
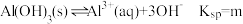 。当
。当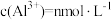 时,溶液的pH等于(已知:该温度下,水的离子积常数
时,溶液的pH等于(已知:该温度下,水的离子积常数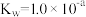 )
)A.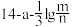 | B.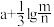 | C.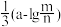 | D.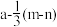 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是25 ℃时某些盐的溶度积常数和弱酸的电离平衡常数。下列说法正确的是
| 化学式 | HCN | CH3COOH | H2CO3 | AgCl | Ag2CrO4 |
| Ka或Ksp | Ka=4.9×10-10 | Ka=1.75×10-5 | Ka1=4.5×10-7,Ka2=4.7×10-11 | Ksp=1.8×10-10 | Ksp=2.0×10-12 |
A.常温下,相同浓度的①CH3COONH4、②NH4HCO3、③NH4HSO4溶液中,c(NH )由大到小的顺序是①>②>③ )由大到小的顺序是①>②>③ |
B.25℃时,等物质的量浓度的各溶液pH关系为:pH(CH3COOH )> pH(H2CO3 )>pH( ) ) |
| C.相同物质的量浓度的CH3COONa和NaCN的混合溶液中,各离子浓度大小关系为:c(Na+)>c( CH3COO-)>c(CN-)>c(OH-) >c(H+) |
D.向浓度均为1×10-3 mol·L-1的KCl和K2CrO4的混合溶液中滴加1×10-3 mol·L-1的AgNO3溶液, 先形成沉淀 先形成沉淀 |
您最近一年使用:0次

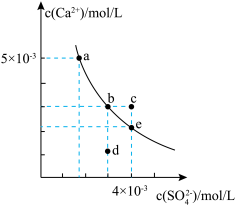
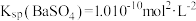 ,
,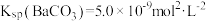 。下列说法中正确的是
。下列说法中正确的是 固体的溶液中,一定有
固体的溶液中,一定有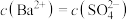
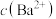 增大
增大 固体至
固体至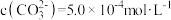 时,
时, 沉淀转化
沉淀转化 的混合溶液中加入
的混合溶液中加入 溶液,当生成
溶液,当生成