我国自主研制的C919大型客机的机身大量采用第三代铝锂合金减重并提高刚度。某铝锂合金成分(质量百分比)如下(Bal指剩余的百分含量):

为了使合金具有高耐腐性能,通常先用酸腐蚀除去铝锂合金表面的氧化层,再进行氧化处理,并进行适当封闭,以提高合金表面耐腐蚀性能。仔细阅读上述信息,回答下列问题:
(1)铝锂合金可用于制造飞机,铝锂合金材料的主要特点是______________________________ 。
(2)铝元素原子核外有_____ 种不同运动状态的电子,最外层电子排布式为___________ 。
(3)碱腐蚀工艺采用40~60g/L的NaOH溶液,在40~55℃下处理0.5~2min时间。写出碱腐蚀主要反应的化学方程式_____________________________ (写一个即可)。
(4) 镁与铝也是构成轻合金的两种常见金属,请从原子结构角度分析比较它们金属性的强弱_____________
(5) 向镁铝合金滴入盐酸至恰好全部溶解,再逐渐滴入氢氧化钠溶液至过量,在滴氢氧化钠过程中观察到的现象有:______________________________________ ;写出其现象中的一个离子方程式_________________ 。

| 成分 | Si | Fe | Cu | Mn | Mg | Zn | Ti | Li | Al |
| 含量 | 0.08 | 0.1 | 2.9~3.5 | 0.5 | 0.25~0.8 | 0.25 | 0.1 | 0.8~1.1 | Bal |
(1)铝锂合金可用于制造飞机,铝锂合金材料的主要特点是
(2)铝元素原子核外有
(3)碱腐蚀工艺采用40~60g/L的NaOH溶液,在40~55℃下处理0.5~2min时间。写出碱腐蚀主要反应的化学方程式
(4) 镁与铝也是构成轻合金的两种常见金属,请从原子结构角度分析比较它们金属性的强弱
(5) 向镁铝合金滴入盐酸至恰好全部溶解,再逐渐滴入氢氧化钠溶液至过量,在滴氢氧化钠过程中观察到的现象有:
更新时间:2019-04-02 20:43:06
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】书写化学方程式
(1)过氧化钠和二氧化碳反应:________
(2)向氯化铝溶液中逐滴滴入氢氧化钠溶液:
a____________ b______________
(1)过氧化钠和二氧化碳反应:
(2)向氯化铝溶液中逐滴滴入氢氧化钠溶液:
a
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】向20 mL某物质的量浓度的AlCl3溶液中滴入2 mol·L-1NaOH溶液时,得到的Al(OH)3沉淀质量与所滴加的NaOH溶液的体积(mL)关系如图所示,试回答下列问题:

(1)图中A点表示的意义是_________________________ 。
(2)图中B点表示的意义是_________________________ 。
(3)上述两步反应用总的离子方程式可表示为:____________________________ 。
(4)若所得Al(OH)3沉淀0.39 g,则此时用去NaOH溶液的体积为______________ 。

(1)图中A点表示的意义是
(2)图中B点表示的意义是
(3)上述两步反应用总的离子方程式可表示为:
(4)若所得Al(OH)3沉淀0.39 g,则此时用去NaOH溶液的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)书写氢氧化铝的电离方程式:___ 。
(2)书写明矾净水的离子方程式:___ 。
(3)铝与氢氧化钠溶液反应的化学反应方程式:___ 。
(4)用一个化学反应方程式来证明氯元素的非金属性比硫元素强:___ 。
(5)书写铁和水反应的化学方程式:___ 。
(2)书写明矾净水的离子方程式:
(3)铝与氢氧化钠溶液反应的化学反应方程式:
(4)用一个化学反应方程式来证明氯元素的非金属性比硫元素强:
(5)书写铁和水反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】如表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在这些元素中,金属性最强的元素是__ ;
(2)化学性质最不活泼的元素其原子的原子结构示意图为__ ;
(3)元素的最高价氧化物对应的水化物中酸性最强的是__ ,碱性最强的是__ ,呈两性的氢氧化物是__ ;
(4)在③~⑦元素中,原子半径最大的是__ ;
(5)在⑦与⑩的单质中,化学性质较活泼的是____ ,可用什么化学反应说明该事实(写出反应的化学方程式):____ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(1)在这些元素中,金属性最强的元素是
(2)化学性质最不活泼的元素其原子的原子结构示意图为
(3)元素的最高价氧化物对应的水化物中酸性最强的是
(4)在③~⑦元素中,原子半径最大的是
(5)在⑦与⑩的单质中,化学性质较活泼的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】海洋是巨大的化学资源宝库。从海水中可以制取氯、溴、镁等多种化工产品。
(1)Mg在元素周期表中的位置是第_______ 周期、第IIA族。
(2)Cl的最高价氧化物对应的水化物为HClO4,其中氯元素的化合价是_______ 。
(3)金属性Na强于Mg,用原子结构解释原因:Na和Mg位于同一周期,原子核外电子层数相同,_______ ,原子半径Na大于Mg,失电子能力Na强于Mg。
(4)在元素周期表中,溴(Br)位于第4周期,与Cl同主族。下列实验或事实能说明得电子能力Cl强于Br的是_______ (填字母)。
a.将Cl2通入KBr溶液中可制得Br2
b.常温常压下,Cl2为气态,Br2为液态
c.HBr约500℃开始分解,HCl约1000℃开始缓慢分解
(1)Mg在元素周期表中的位置是第
(2)Cl的最高价氧化物对应的水化物为HClO4,其中氯元素的化合价是
(3)金属性Na强于Mg,用原子结构解释原因:Na和Mg位于同一周期,原子核外电子层数相同,
(4)在元素周期表中,溴(Br)位于第4周期,与Cl同主族。下列实验或事实能说明得电子能力Cl强于Br的是
a.将Cl2通入KBr溶液中可制得Br2
b.常温常压下,Cl2为气态,Br2为液态
c.HBr约500℃开始分解,HCl约1000℃开始缓慢分解
您最近一年使用:0次
【推荐1】据报道,某些花岗岩会释放氡 ,对人体造成伤害。
,对人体造成伤害。
(1)氡原子的核外电子数是___________ ,中子数是___________ 。
(2)请将Rn的原子结构示意图补全___________ 。
(3)请根据Rn的原子结构预测氡气的化学性质___________
(4)研究发现,镭能蜕变为 ,故将
,故将 称为镭射气;钍能蜕变为
称为镭射气;钍能蜕变为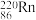 ,故将
,故将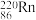 称为钍射气;锕能蜕变为
称为钍射气;锕能蜕变为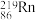 ,
,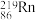 故将称为锕射气。
故将称为锕射气。 、
、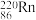 、
、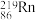
___________ 。
A.属于同种元素B.互为同位素C.属于同种核素D.属于同种原子
判断依据:___________ 决定元素种类,___________ 决定核素种类。
 ,对人体造成伤害。
,对人体造成伤害。(1)氡原子的核外电子数是
(2)请将Rn的原子结构示意图补全

(3)请根据Rn的原子结构预测氡气的化学性质___________
| A.非常活泼,容易与氧气等非金属单质反应 |
| B.比较活泼,能与钠等金属反应 |
| C.不太活泼,与氮气性质相似 |
| D.很难与其他物质发生反应 |
 ,故将
,故将 称为镭射气;钍能蜕变为
称为镭射气;钍能蜕变为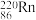 ,故将
,故将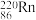 称为钍射气;锕能蜕变为
称为钍射气;锕能蜕变为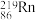 ,
,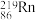 故将称为锕射气。
故将称为锕射气。 、
、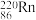 、
、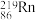
A.属于同种元素B.互为同位素C.属于同种核素D.属于同种原子
判断依据:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】硼矿是无机盐工业的重要原料,硼镁石用硫酸分解的反应式为2MgO·B2O3·H2O+2H2SO4→2H3BO3+2MgSO4。
(1)上述反应中,核外电子排布式相同的离子有__ ;原子核外具有五种不同能量电子的元素名称是__ 。
(2)硼元素在元素周期表中的位置是__ ;已知BF3分子的空间构型为平面正三角形,则BF3属于__ 分子(填“极性”或“非极性”)。
(3)Mg元素的原子结构示意图为__ 。Mg(OH)2碱性比Ca(OH)2__ (填“强”或“弱”)。
(4)硼酸[H3BO3或B(OH)3]是一元弱酸,它的水溶液之所以呈弱酸性并非本身电离出H+,而是硼酸与水作用时,与水电离产生的OH-结合,导致溶液中c(H+)>c(OH-)。用离子方程式表示硼酸呈酸性的原因__ 。
(1)上述反应中,核外电子排布式相同的离子有
(2)硼元素在元素周期表中的位置是
(3)Mg元素的原子结构示意图为
(4)硼酸[H3BO3或B(OH)3]是一元弱酸,它的水溶液之所以呈弱酸性并非本身电离出H+,而是硼酸与水作用时,与水电离产生的OH-结合,导致溶液中c(H+)>c(OH-)。用离子方程式表示硼酸呈酸性的原因
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】食盐是有钠元素和氯元素组成的日常生活中使用最为广泛的调味品。从海水得到的粗食盐水中常含Ca2+、Mg2+、 ,需要分离提纯。现有含少量杂质(主要为少量泥沙、CaCl2、MgCl2、Na2SO4等)的粗盐制取较纯净的食盐、某学生小组设计的提纯操作步骤和加入试剂的情况如图。
,需要分离提纯。现有含少量杂质(主要为少量泥沙、CaCl2、MgCl2、Na2SO4等)的粗盐制取较纯净的食盐、某学生小组设计的提纯操作步骤和加入试剂的情况如图。
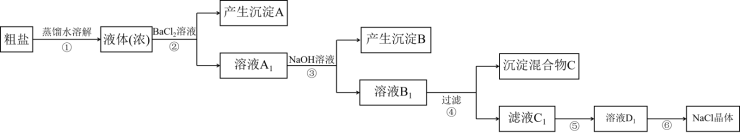
(1)第①步蒸馏水溶解粗盐后,获得“液体(浓)”的操作名称为___________ ,沉淀A的化学式___________ 。
(2)写出第⑤步操作中可能发生反应的离子方程式:___________ ;___________ 。
(3)请写出操作第④、⑤步所加试剂名称:④___________ ;⑤___________ 。
(4)有同学认为上述实验设计步骤可以简化,请你提出一种设想;___________ 。
 ,需要分离提纯。现有含少量杂质(主要为少量泥沙、CaCl2、MgCl2、Na2SO4等)的粗盐制取较纯净的食盐、某学生小组设计的提纯操作步骤和加入试剂的情况如图。
,需要分离提纯。现有含少量杂质(主要为少量泥沙、CaCl2、MgCl2、Na2SO4等)的粗盐制取较纯净的食盐、某学生小组设计的提纯操作步骤和加入试剂的情况如图。
(1)第①步蒸馏水溶解粗盐后,获得“液体(浓)”的操作名称为
(2)写出第⑤步操作中可能发生反应的离子方程式:
(3)请写出操作第④、⑤步所加试剂名称:④
(4)有同学认为上述实验设计步骤可以简化,请你提出一种设想;
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如下:

(1)步骤(I)中生成的气体是___________ ,溶液A和沉淀分离的操作名称是___________ 。
(2)步骤(II)中加入H2O2溶液后,反应生成Fe2(SO4)3,该反应___________ (填“属于”或“不属于”)氧化还原反应。
(3)步骤(III)中生成Fe(OH)3沉淀的颜色是___________ (填“白色”或“红褐色”)。
(4)步骤(IV)中Fe(OH)3受热分解生成Fe2O3和H2O的化学方程式为___________ 。

(1)步骤(I)中生成的气体是
(2)步骤(II)中加入H2O2溶液后,反应生成Fe2(SO4)3,该反应
(3)步骤(III)中生成Fe(OH)3沉淀的颜色是
(4)步骤(IV)中Fe(OH)3受热分解生成Fe2O3和H2O的化学方程式为
您最近一年使用:0次



