2004年4月15日,重庆某化工厂氯气泄漏并发生爆炸,爆炸现场弥漫着黄色烟雾,这起事故共造成7人丧生,并致使近15万群众紧急疏散。问题:
(1)爆炸现场弥漫的黄色烟雾,除氯气外,形成雾的主要原因是Cl2与水反应,反应的化学方程式为___________________________________ ;形成烟的成分包含Cl2与Fe反应的产物___________ ,Cl2是一种有毒气体,为消除毒气,消防部门用消防用水与碱液在外围50米处形成两道水幕进行稀释,写出Cl2与强碱溶液反应的离子方程式__________________________________ 。
(2)Cl2及其无机产品常用做消毒剂,如“84消毒液”(NaClO)、“漂白粉”等,它们的消毒原理都是在潮湿的空气中与CO2和水蒸气反应生成了次氯酸,请写出“84消毒液”(NaClO)在空气中发生作用的化学方程式:________________________________ 。
(3)用氯气对饮用水消毒已经有百年的历史,这种消毒的方法中氯气会与水中的有机物发生氯代生成对人体有害的的氯代物,于是世界环保联盟建议推广广谱高效消毒剂二氧化氯(ClO2),制取二氧化氯的其中一种方法是:Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O,该反应中氧化剂是_______ ,还原剂是_______ ,氧化剂与还原剂的物质的量之比为_________ ;若生成1mol ClO2则转移电子数为____________ (NA表示阿伏伽德罗常数)。
(1)爆炸现场弥漫的黄色烟雾,除氯气外,形成雾的主要原因是Cl2与水反应,反应的化学方程式为
(2)Cl2及其无机产品常用做消毒剂,如“84消毒液”(NaClO)、“漂白粉”等,它们的消毒原理都是在潮湿的空气中与CO2和水蒸气反应生成了次氯酸,请写出“84消毒液”(NaClO)在空气中发生作用的化学方程式:
(3)用氯气对饮用水消毒已经有百年的历史,这种消毒的方法中氯气会与水中的有机物发生氯代生成对人体有害的的氯代物,于是世界环保联盟建议推广广谱高效消毒剂二氧化氯(ClO2),制取二氧化氯的其中一种方法是:Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O,该反应中氧化剂是
更新时间:2019-04-08 17:55:37
|
相似题推荐
【推荐1】回答下列问题:
(1)氯酸钾和浓盐酸之间有下列反应: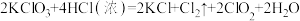 。该反应中发生还原反应的物质是
。该反应中发生还原反应的物质是___________ (填化学式。下同),氧化产物是___________ ;用双线桥标出方程式中的电子的转移情况:___________ 。
(2) 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(
可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾( ),氧化性比Cl2、O2、ClO2、
),氧化性比Cl2、O2、ClO2、 还强,主要反应:
还强,主要反应: 。
。
①上述反应中作还原剂的是___________ (填化学式)。
②简要说明 作为水处理剂时所起的作用
作为水处理剂时所起的作用___________ (写出一点即可)。
③在上述反应过程中可生成一种 白色沉淀,该沉淀极易被空气中的氧气氧化,反应的化学方程式为
白色沉淀,该沉淀极易被空气中的氧气氧化,反应的化学方程式为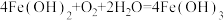 (红褐色沉淀),该反应属于四大基本反应中的
(红褐色沉淀),该反应属于四大基本反应中的___________ (填反应类型名称),每当有1 mol O2参与反应转移的电子数为___________ 个。
(1)氯酸钾和浓盐酸之间有下列反应:
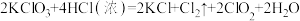 。该反应中发生还原反应的物质是
。该反应中发生还原反应的物质是(2)
 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(
可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾( ),氧化性比Cl2、O2、ClO2、
),氧化性比Cl2、O2、ClO2、 还强,主要反应:
还强,主要反应: 。
。①上述反应中作还原剂的是
②简要说明
 作为水处理剂时所起的作用
作为水处理剂时所起的作用③在上述反应过程中可生成一种
 白色沉淀,该沉淀极易被空气中的氧气氧化,反应的化学方程式为
白色沉淀,该沉淀极易被空气中的氧气氧化,反应的化学方程式为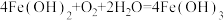 (红褐色沉淀),该反应属于四大基本反应中的
(红褐色沉淀),该反应属于四大基本反应中的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮,磷,硫,氯等非金属元素的单质和化合物在工农业生产中有重要应用。回答下列问题:
(1)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为___________ ,某厂废液中含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为N2的是___________ (填标号)。
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为___________ 。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4 :1,则氧化产物为____ (填化学式)。
(3)硫代硫酸钠晶体(Na2S2O3·5H2O),又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式___________ 。
(4)氯气与氢氧化钠在70℃时反应,生成物中NaClO3和NaClO的物质的量之比为3 :1的离子方程式为___________ 。
(1)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4 :1,则氧化产物为
(3)硫代硫酸钠晶体(Na2S2O3·5H2O),又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式
(4)氯气与氢氧化钠在70℃时反应,生成物中NaClO3和NaClO的物质的量之比为3 :1的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系________ (填“属于”或“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为_____ (填“酸”或“碱”)性,表示该试样酸碱性的c(H+)或c(OH-)=______ mol·L-1。
Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(3)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C______ 具有(填“氧化性”或“还原性”)。
(4)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中每生成1molClO2分子,转移电子的数目为_____ 。
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_____ 。
A.O2 B.FeCl2 C.KCl D.KMnO4
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(3)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C
(4)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中每生成1molClO2分子,转移电子的数目为
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KCl D.KMnO4
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。能导电的是___ (填序号,下同);属于电解质的是___ ;属于非电解质的是___ 。
(2)1.204×1024个H2SO4分子的物质的量为___ mol,共含___ 个氢原子。将上述H2SO4溶于水配成600mL溶液,再加水稀释到1000mL,稀释后溶液的物质的量浓度为___ mol/L。
(3)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO 浓度为0.9mol/L,则K+的物质的量浓度为
浓度为0.9mol/L,则K+的物质的量浓度为___ mol/L。
(4)写出铁在氯气中燃烧的化学方程式为___ ;过氧化钠与二氧化碳反应的化学方程式为___ 。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。能导电的是
(2)1.204×1024个H2SO4分子的物质的量为
(3)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO
 浓度为0.9mol/L,则K+的物质的量浓度为
浓度为0.9mol/L,则K+的物质的量浓度为(4)写出铁在氯气中燃烧的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)新制氯水中含有的微粒:H2O、HClO、Cl2、H+、Cl-、ClO-、___ 。
(2)判断:可以用pH试纸测定新制氯水的pH。___ (打“√”或“×”)
(3)久置氯水与碳酸氢钠溶液反应的化学方程式___ 。
(4)写出铁在氯气中燃烧的化学方程式:___ 。
(5)写出电解饱和食盐水的化学方程式:___ 。
(2)判断:可以用pH试纸测定新制氯水的pH。
(3)久置氯水与碳酸氢钠溶液反应的化学方程式
(4)写出铁在氯气中燃烧的化学方程式:
(5)写出电解饱和食盐水的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】填空:
(1)将一小块钠投入到硫酸铜溶液中,观察到与钠跟水反应相同的 现象是___________ ;还可以观察到的现象是___________ 。写出有关的化学方程式:___________ 、___________ 。
(2)灼烧后的铜丝立即插入充满氯气的集气瓶中观察到的现象是___________ ,集气瓶中注入少量水看到的现象是___________ 。
(3)将点燃的氢气伸入盛有氯气的集气瓶中观察到的现象是___________ 。
(1)将一小块钠投入到硫酸铜溶液中,观察到与钠跟水反应
(2)灼烧后的铜丝立即插入充满氯气的集气瓶中观察到的现象是
(3)将点燃的氢气伸入盛有氯气的集气瓶中观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氯是海水中含量最丰富的元素,氯的单质及其化合物在生成、生活领域应用广泛。
(1)自来水厂常用液氯进行杀菌消毒。氯气溶于水发生的可逆反应为_____________ (用离子方程式表示)。
(2)用液氯消毒会产生微量有机氯代物,危害人体健康,可以使用二氧化氯(ClO2)代替液氯。工业上以二硫化亚铁(FeS2)、氯酸钠(NaClO3)和硫酸溶液混合制备二氧化氯气体。已知黄铁矿中的硫元素最终氧化成 ,写出制备二氧化氯的离子方程式
,写出制备二氧化氯的离子方程式_______ 。
(3)生产漂白粉工厂的主要设备是氯化塔,塔从上到下分为四层,如图为生产流程示意图。生产漂白粉反应的化学方程式为_______ 。实际生产中,将石灰乳(含有3%~6%水分的熟石灰)从塔顶喷洒而下,氯气从塔的最底层通入。这样加料的目的是_______ 。
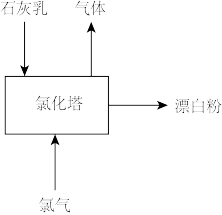
(1)自来水厂常用液氯进行杀菌消毒。氯气溶于水发生的可逆反应为
(2)用液氯消毒会产生微量有机氯代物,危害人体健康,可以使用二氧化氯(ClO2)代替液氯。工业上以二硫化亚铁(FeS2)、氯酸钠(NaClO3)和硫酸溶液混合制备二氧化氯气体。已知黄铁矿中的硫元素最终氧化成
 ,写出制备二氧化氯的离子方程式
,写出制备二氧化氯的离子方程式(3)生产漂白粉工厂的主要设备是氯化塔,塔从上到下分为四层,如图为生产流程示意图。生产漂白粉反应的化学方程式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】液氯和氯水有什么区别?_____________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】非金属元素在生活、生产中扮演着非常重要的角色。请根据题意填空。
(1)木棍放在浓硫酸中变黑,体现了浓硫酸的______ (填“脱水性”或“氧化性”)。
(2)已知玻璃中的成分有SiO2,实验室盛放碱溶液的试剂瓶应使用______ (填“玻璃塞”或“橡胶塞”)的试剂瓶。
(3)Cl2可与水反应,请写出该反应的离子方程式:_____ 。
(1)木棍放在浓硫酸中变黑,体现了浓硫酸的
(2)已知玻璃中的成分有SiO2,实验室盛放碱溶液的试剂瓶应使用
(3)Cl2可与水反应,请写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求写出化学方程式。
(1)Na和H2O反应:_______
(2)Na2O2和CO2反应:_______
(3)Na2O2和H2O反应:_______
(4)Fe在Cl2中燃烧:_______
(5)Fe和H2O(g)的反应:_______
(6)Fe和FeCl3(aq)的反应:_______
(7)Cl2和NaOH(aq)的反应:_______
(1)Na和H2O反应:
(2)Na2O2和CO2反应:
(3)Na2O2和H2O反应:
(4)Fe在Cl2中燃烧:
(5)Fe和H2O(g)的反应:
(6)Fe和FeCl3(aq)的反应:
(7)Cl2和NaOH(aq)的反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】疫情防控期间的消毒工作含氯消毒剂功不可没,研究消毒剂的性质意义重大。回答下列问题:
(1)2016年巴西奥运会游泳池变绿是因为84消毒液与过氧化氢消毒剂混用,写出该反应的化学方程式_______ ,转移电子数为3NA时,理论上生成标况下气体体积是________ 。
(2) 、HClO和
、HClO和 三种微粒的物质的量分数随pH变化的关系如图所示。
三种微粒的物质的量分数随pH变化的关系如图所示。
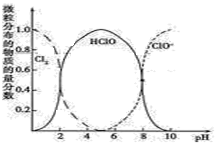
回答问题:
①使用84消毒液时为增强消毒效果常调节 ,原因是
,原因是___________ 。
②通常购买的84消毒液pH在12左右,此时主要成分是___________ (化学式),为增强消毒效果可向其中滴加___________ (填字母序号)。
A.可口可乐 B.稀 C.食醋 D.浓盐酸
C.食醋 D.浓盐酸
(3)实验室将 通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为NA,计算此时所得溶液中NaClO的质量分数为
通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为NA,计算此时所得溶液中NaClO的质量分数为___________ %。
(1)2016年巴西奥运会游泳池变绿是因为84消毒液与过氧化氢消毒剂混用,写出该反应的化学方程式
(2)
 、HClO和
、HClO和 三种微粒的物质的量分数随pH变化的关系如图所示。
三种微粒的物质的量分数随pH变化的关系如图所示。
回答问题:
①使用84消毒液时为增强消毒效果常调节
 ,原因是
,原因是②通常购买的84消毒液pH在12左右,此时主要成分是
A.可口可乐 B.稀
 C.食醋 D.浓盐酸
C.食醋 D.浓盐酸(3)实验室将
 通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为NA,计算此时所得溶液中NaClO的质量分数为
通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为NA,计算此时所得溶液中NaClO的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】新冠疫情的发生,消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,而氯气是制取消毒液的重要原料之一。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式___________________________________ ,若收集到标准状况下3.36LCl2,则被氧化的HCl的物质的量为_____________ mol。
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式_______________________________________ ,若要制取1.5L 2 mol/L的84消毒液,则需要标准状况下___________ L 氯气。
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因__________________________________ (用化学方程式表示), 该反应中氧化剂是______________ 。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因
您最近一年使用:0次



