实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为:
______ KMnO4+______ HCl(浓) =______ KCl+______ MnCl2+______ Cl2↑+______ H2O
(1)请配平化学方程式(将化学计量数填入括号内)。
(2)请将上述配平的化学方程式改写为离子方程式________________ 。
(3)浓盐酸在反应中显示出来的性质是________________ (填写编号,多选倒扣)。
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(4)产生0.5molCl2,则转移的电子的物质的量为______ mol。
(5)已知反应CuS+4HNO3=Cu(NO3)2+2NO2↑+S↓+2H2O,当转移电子数为1.806×1023时,被还原的硝酸的物质的量是__________ ,产生标况NO2的体积为____________ 。
(1)请配平化学方程式(将化学计量数填入括号内)。
(2)请将上述配平的化学方程式改写为离子方程式
(3)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(4)产生0.5molCl2,则转移的电子的物质的量为
(5)已知反应CuS+4HNO3=Cu(NO3)2+2NO2↑+S↓+2H2O,当转移电子数为1.806×1023时,被还原的硝酸的物质的量是
11-12高一上·黑龙江·期中 查看更多[1]
(已下线)2011-2012学年黑龙江省哈三中高一上学期期中考试化学试卷
更新时间:2011-11-12 11:12:29
|
相似题推荐
【推荐1】高锰酸钾是一种典型的强氧化剂。
(1)在用 KMnO4 酸性溶液处理固体 Cu2S 时,发生的反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
①还原产物为_____ 。
②被氧化的元素是_____
③氧化剂与还原剂的物质的量之比为_____
④每生成 2.24 L(标况下)SO2,转移电子数目是_____
(2)用 KMnO4 酸性溶液处理固体 CuS 时,也可将 CuS 反应成 Cu2+和 SO2。写出该离子反应方程式_____
(3)15.8g KMnO4,加热分解后剩余固体 15.0 g。该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体 A,产物中锰元素以 Mn2+存在,则气体 A 的物质的量为_____ mol。
(1)在用 KMnO4 酸性溶液处理固体 Cu2S 时,发生的反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
①还原产物为
②被氧化的元素是
③氧化剂与还原剂的物质的量之比为
④每生成 2.24 L(标况下)SO2,转移电子数目是
(2)用 KMnO4 酸性溶液处理固体 CuS 时,也可将 CuS 反应成 Cu2+和 SO2。写出该离子反应方程式
(3)15.8g KMnO4,加热分解后剩余固体 15.0 g。该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体 A,产物中锰元素以 Mn2+存在,则气体 A 的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】Cu2S能与硝酸反应。与稀硝酸反应的化学方程式为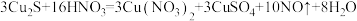 ,反应中的还原剂是
,反应中的还原剂是_______ 。当有160g 反应时,转移的电子总数约为
反应时,转移的电子总数约为_______ 。
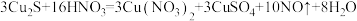 ,反应中的还原剂是
,反应中的还原剂是 反应时,转移的电子总数约为
反应时,转移的电子总数约为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】一个体重50 kg的健康人身体中含铁2 g。铁在人体中不是以游离态的形式存在,而是以Fe2+和Fe3+形式存在。Fe2+易被吸收,给贫血者补充铁时,应给予含Fe2+的盐,如硫酸亚铁(FeSO4)。人体中经常进行Fe2+和Fe3+的转化,服用维生素C,可使食物中的Fe3+转化为Fe2+”,说明维生素C具有__________ 性。
(2)羟胺(NH2OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是_________________ 。
(2)羟胺(NH2OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓) = MnCl2+Cl2↑+2H2O。若产生的氯气在标准状况下的体积为11.2L。请完成下列问题:
(1)用双线桥表示法标出该反应的电子转移情况______ 。
(2)参加反应的MnO2的质量______ 。
(3)参加反应的HCl的物质的量______ 。
(4)反应中氧化剂与还原剂的物质的量之比______ 。
(1)用双线桥表示法标出该反应的电子转移情况
(2)参加反应的MnO2的质量
(3)参加反应的HCl的物质的量
(4)反应中氧化剂与还原剂的物质的量之比
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)在标准状况下,11.2L氢气含有氢原子的数目为__ 个(NA约为6.02×1023mol-1);某金属氯化物MCl257g,含有1.20molCl-,则该氯化物的摩尔质量为__ ;同温同压下的N2和H2,其密度比为__ ;同温同压下,质量相同的N2和H2的体积之比为___ 。
(2)在KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O的反应中,氧化剂是__ ,若有0.5mol电子转移,则产生的Cl2在标准状况下的体积为___ L。
(3)铜与稀硝酸反应可生成一氧化氮(NO)气体,其反应方程式如下,用双线桥法在下面的反应式上标出电子转移的方向与数目。__
3Cu+8HNO3(稀)=3Cu(NO3)2+4H2O+2NO↑
(2)在KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O的反应中,氧化剂是
(3)铜与稀硝酸反应可生成一氧化氮(NO)气体,其反应方程式如下,用双线桥法在下面的反应式上标出电子转移的方向与数目。
3Cu+8HNO3(稀)=3Cu(NO3)2+4H2O+2NO↑
您最近一年使用:0次
【推荐3】已知:i.用毛笔蘸取少量30%的FeCl3溶液在铜片上写一个“Cu”,放置片刻后用少量蒸馏水冲洗铜片后,在铜片上会出现凹凸的“Cu”。
ii.Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O。
(1)写出i中反应的离子方程式:___________ 。
(2)反应ii中氧化剂与还原剂的物质的量之比为___________ ,用双线桥法标出电子转移的方向与数目:___________ ,当反应中有0.6 mol电子转移时,生成NO的体积为___________ L(标准状况)。
(3)向含有0.2 mol FeCl3、0.2 mol CuCl2的混合溶液中加入0.1 mol Zn,充分反应后溶液中没有固体存在,则溶液中的金属阳离子有Zn2+、___________ 。
(4)HNO3、Fe3+、Cu2+的氧化性由强到弱的顺序为___________ 。
ii.Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O。
(1)写出i中反应的离子方程式:
(2)反应ii中氧化剂与还原剂的物质的量之比为
(3)向含有0.2 mol FeCl3、0.2 mol CuCl2的混合溶液中加入0.1 mol Zn,充分反应后溶液中没有固体存在,则溶液中的金属阳离子有Zn2+、
(4)HNO3、Fe3+、Cu2+的氧化性由强到弱的顺序为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I−完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
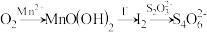
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:__________ 。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L−1 Na2S2O3标准溶液13.50 mL。(已知反应:I2+2S2O32-=2I-+S4O62-)计算该水样中的溶解氧(以mg·L−1表示),写出计算过程__________ 。
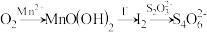
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L−1 Na2S2O3标准溶液13.50 mL。(已知反应:I2+2S2O32-=2I-+S4O62-)计算该水样中的溶解氧(以mg·L−1表示),写出计算过程
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】无机化合物 A 和 NaH 都是重要的还原剂,遇水都强烈反应。一定条件下,2.4g NaH 与气体 B 反应生成 3.9g 化合物 A 和 2.24L(已折算成标准状况)的 H2。已知气体 B 可使湿润红色石蕊试纸变蓝。请回答下列问题:
(1)B 的化学式是_____ 。
(2)NaH 与气体 B 反应生成化合物 A 的化学方程式_____ 。该反应中 A 是_____ 。
A.氧化产物 B.还原产物 C.既不是氧化产物也不是还原产物
(3)0.1molA 与足量盐酸发生非氧化还原反应最多消耗 HCl_____ mol
(4)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,同时得到混合气体, 测得其平均摩尔质量为 25 g/mol,写出该反应的化学方程式_____ 。
(1)B 的化学式是
(2)NaH 与气体 B 反应生成化合物 A 的化学方程式
A.氧化产物 B.还原产物 C.既不是氧化产物也不是还原产物
(3)0.1molA 与足量盐酸发生非氧化还原反应最多消耗 HCl
(4)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,同时得到混合气体, 测得其平均摩尔质量为 25 g/mol,写出该反应的化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)配平反应的离子方程式:_____ XeO3+____ Mn2++_____ H2O →____ MnO4-+____ Xe↑+___ H+
(2)反应现象为:①有气泡产生,②______________________ 。
(3)发生氧化反应的物质(或微粒)是_______________ 。
(4)将适量的XeO3投入30mL 0.1mol⋅L−1 Mn2+的水溶液中,刚好完全反应。
①此时转移电子_____________ mol。
②将反应后的溶液稀释至90mL,所得溶液的pH=________ 。
(2)反应现象为:①有气泡产生,②
(3)发生氧化反应的物质(或微粒)是
(4)将适量的XeO3投入30mL 0.1mol⋅L−1 Mn2+的水溶液中,刚好完全反应。
①此时转移电子
②将反应后的溶液稀释至90mL,所得溶液的pH=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
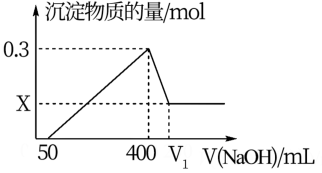
【推荐1】把7.5 g镁铝合金的粉末放入200ml 4mol/L的盐酸中,往充分反应后的混合溶液中逐渐滴入一定物质的量浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积的关系如图所示。
(1)合金中镁的物质的量为_______ 。
(2)氢氧化钠的物质的量浓度为_______ mol/L。
(3)V1=_______ mL。
(4)写出该合金溶于足量NaOH溶液的化学方程式为_________ 。
(1)合金中镁的物质的量为
(2)氢氧化钠的物质的量浓度为
(3)V1=
(4)写出该合金溶于足量NaOH溶液的化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】Cl2与NaOH溶液反应可生成NaCl、NaClO和NaClO3、c(Cl-)和c(ClO-)的比值与反应温度有关。用48 g NaOH配成的500 mL溶液,与Cl2恰好完全反应(忽略Cl2与水的反应、盐类的水解及溶液体积变化)。
(1)NaOH溶液的物质的量浓度___ mol/L
(2)某温度下,反应后溶液中c(Cl-)=3c(ClO-), 则溶液在c(ClO-)=_____ mol/L。
(1)NaOH溶液的物质的量浓度
(2)某温度下,反应后溶液中c(Cl-)=3c(ClO-), 则溶液在c(ClO-)=
您最近一年使用:0次

 溶液的pH=
溶液的pH= 溶液的pH=
溶液的pH= 混合气体在标准状况下的体积为11.2L,请回答:
混合气体在标准状况下的体积为11.2L,请回答: 。
。


