已知硼酸(分子式为H3BO3)对人体的受伤组织有缓和防腐作用,故可以用于医药和食品防腐等方面。试回答下列问题:
(1)已知硼酸分子中H只与O成键,则其分子结构式为____________ ,由其结构可推知硼酸应属于______ 酸(选填“弱”或“强”)。
(2)已知硼酸晶体呈片状,具有类似石墨那样的片层结构,片层之间作用较弱,有滑腻感,可做润滑剂。则层内H3BO3分子之间的作用力是________ ,层与层间的作用力是______ 。
(3)已知0.01mol硼酸可以被20mL 0.5mol·L-1NaOH溶液恰好完全中和,据此推知硼酸属____ 元酸。研究表明:在大多数情况下,元素的原子在形成分子或离子时,其最外层有达到8电子稳定结构的趋向,如 。写出硼酸与NaOH溶液反应的离子方程式:
。写出硼酸与NaOH溶液反应的离子方程式:____________ 。
(1)已知硼酸分子中H只与O成键,则其分子结构式为
(2)已知硼酸晶体呈片状,具有类似石墨那样的片层结构,片层之间作用较弱,有滑腻感,可做润滑剂。则层内H3BO3分子之间的作用力是
(3)已知0.01mol硼酸可以被20mL 0.5mol·L-1NaOH溶液恰好完全中和,据此推知硼酸属
 。写出硼酸与NaOH溶液反应的离子方程式:
。写出硼酸与NaOH溶液反应的离子方程式:
11-12高二上·湖北黄冈·期中 查看更多[1]
(已下线)2011-2012年湖北省黄冈中学高二上学期期中考试化学试卷
更新时间:2016-12-09 02:18:18
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】写出下列离子方程式:
①钠投入水中__________
②少量稀的三氯化铝溶液中 滴入足量浓的烧碱溶液中________
③纯碱溶液中通入CO2_________
④铝在烧碱溶液中溶解____________
⑤小苏打溶液中加食醋:____________
①钠投入水中
②少量稀的三氯化铝溶液中 滴入足量浓的烧碱溶液中
③纯碱溶液中通入CO2
④铝在烧碱溶液中溶解
⑤小苏打溶液中加食醋:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)我国是世界上最早使用湿法炼铜的国家。湿法炼铜的原理是Fe+CuSO4=FeSO4+Cu,其中CuSO4被_______ (填“氧化”或“还原”),铁作_______ (填“氧化剂”或“还原剂”)。在该反应中,若生成了32 g Cu,消耗Fe的物质的量是_______ 。
(2)某学习小组设计下图所示装置观察氧化还原反应中电子的转移。
①实验Ⅰ中,Fe与CuSO4溶液反应的离子方程式是_______ 。
②根据实验Ⅰ的原理,推测实验Ⅱ中:锌片上发生_______ (填“氧化反应”或“还原反应”);铜片上的实验现象是_______ 。
(1)我国是世界上最早使用湿法炼铜的国家。湿法炼铜的原理是Fe+CuSO4=FeSO4+Cu,其中CuSO4被
(2)某学习小组设计下图所示装置观察氧化还原反应中电子的转移。
| 实验I | 实验II | |
| 装置 | 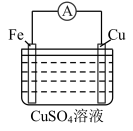 | 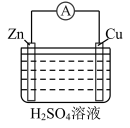 |
| 现象 | 电流计指针向右偏转;铁片溶解;铜片上有红色物质(铜)析出,铜片质量增加 | 电流计指针向右偏转;…… |
②根据实验Ⅰ的原理,推测实验Ⅱ中:锌片上发生
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】往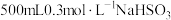 溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
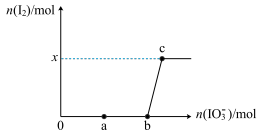
回答下列问题:
(1)NaHSO3在水中的电离方程式为___________ 。
(2)a点溶液的pH___________ (填“>”、“<”或“=”)7,判断的理由为___________ (用离子方程式表示)。
(3)b点溶液中所含的阳离子有___________ (填离子符号)。
(4)b→c的离子方程式为___________ 。
(5)往c点溶液中加入淀粉溶液,可以观察到的现象为___________ 。
(6)x=___________ 。
 溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
回答下列问题:
(1)NaHSO3在水中的电离方程式为
(2)a点溶液的pH
(3)b点溶液中所含的阳离子有
(4)b→c的离子方程式为
(5)往c点溶液中加入淀粉溶液,可以观察到的现象为
(6)x=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在研究弱电解质的电离、盐类的水解和溶液中离子浓度大小比较中,某师生共同做了这样一个实验:常温下,向20.0mL,0.1mol/L CH3COOH溶液中逐滴加入0.01mol/L NaOH溶液,并在滴加过程中不断用pH计测量混合溶液的pH,绘出pH—V(NaOH)图像,如图所示。请分析:
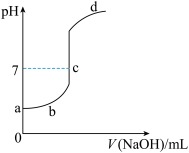
(1)在滴加NaOH溶液至过量过程中的溶液中溶质的变化情况,a、b、c、d各点的溶质各是什么( ) ( ) ( ) ( ) ?
(2)CH3COOH与NaOH恰好完全反应的点在图像中的位置在________ (填:pH>7或pH<7或 pH=7)区域内,由此可验证CH3COOH为___________ (填:弱酸或强酸),此时共滴加V(NaOH)=_____________ mL。
(3)若将此实验改为中和滴定实验应用__________ 作为指示剂。
(4)随着NaOH的加入,水的电离受到一定的影响,当水的电离达到最大时溶液中的溶质为_____________ 。
(5)当测得pH为7时共用去V(NaOH)=VmL,请用V的表达式表示此时CH3COOH的电离平衡常数_____ 。

(1)在滴加NaOH溶液至过量过程中的溶液中溶质的变化情况,a、b、c、d各点的溶质各是什么
(2)CH3COOH与NaOH恰好完全反应的点在图像中的位置在
(3)若将此实验改为中和滴定实验应用
(4)随着NaOH的加入,水的电离受到一定的影响,当水的电离达到最大时溶液中的溶质为
(5)当测得pH为7时共用去V(NaOH)=VmL,请用V的表达式表示此时CH3COOH的电离平衡常数
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据表中数据(室温),回答下列问题:
已知氢氟酸、醋酸、次氯酸(HClO)、碳酸的电离常数分别为:
(1)写出以下反应的离子方程式:
①足量的氢氟酸与碳酸钠溶液混合:___________ ;
②少量的CO2通入NaClO溶液:___________ 。
(2)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)___________ mol/L(填精确值), =
=___________ 。
(3)25℃时,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,充分混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为___________ 。
(4)室温下pH=9的NaOH溶液和pH=10的CH3COONa溶液,设由水电离产生的OH﹣的物质的量浓度分别为A和B,则A/B等于___________ 。
(5)甲醇与CO可以生成醋酸,常温下将amol/L的醋酸与bmol∙L-1Ba(OH)2溶液以2∶1体积比混合,混合溶液中2c(Ba2+)=c(CH3COO-),则醋酸的电离平衡常数为_______ (用含a和b的代数式表示)。
已知氢氟酸、醋酸、次氯酸(HClO)、碳酸的电离常数分别为:
| HF | Ka=6.8×10-4mol•L-1 |
| CH3COOH | Ka=1.7×10-5mol•L-1 |
| HClO | Ka=2.9×10-8mol•L-1 |
| H2CO3 | Ka1=4.4×10-7mol•L-1 Ka2=4.7×10-11mol•L-1 |
①足量的氢氟酸与碳酸钠溶液混合:
②少量的CO2通入NaClO溶液:
(2)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)
 =
=(3)25℃时,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,充分混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为
(4)室温下pH=9的NaOH溶液和pH=10的CH3COONa溶液,设由水电离产生的OH﹣的物质的量浓度分别为A和B,则A/B等于
(5)甲醇与CO可以生成醋酸,常温下将amol/L的醋酸与bmol∙L-1Ba(OH)2溶液以2∶1体积比混合,混合溶液中2c(Ba2+)=c(CH3COO-),则醋酸的电离平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填写下列相关内容:
(1)实验表明,液氨也能像水那样进行自耦电离(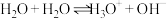 ),写出液氨自耦电离的方程式
),写出液氨自耦电离的方程式___________ 。
(2)室温下,在48mL 的醋酸溶液中加入12mL0.4mol/L的KOH溶液,所得溶液呈
的醋酸溶液中加入12mL0.4mol/L的KOH溶液,所得溶液呈___________ (填“酸性”、“碱性”或“中性”)。
(3)常温下, 的下列溶液中,水电离出的
的下列溶液中,水电离出的 由大到小的顺序是
由大到小的顺序是___________ (填序号,下同),pH由大到小的顺序是___________ 。
①HNO3 ②H2SO4 ③CH3COOH(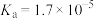 ) ④
) ④ (
( ) ⑤NaOH ⑥
) ⑤NaOH ⑥
(4)某温度时,0.1mol/L的NaOH溶液的pH是11,在此温度下,将 的盐酸溶液
的盐酸溶液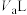 与
与 的NaOH溶液
的NaOH溶液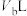 混合,所得混合液为中性,若
混合,所得混合液为中性,若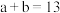 ,则
,则
___________ 。
(5)H2A在水溶液中的电离如下: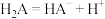 ,
, ,
,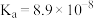 向H2A溶液中滴加少量氨水,该反应的离子方程式为
向H2A溶液中滴加少量氨水,该反应的离子方程式为___________ 。
(6)已知甲酸在一定条件下发生此反应: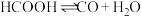 ,正反应速率方程为:
,正反应速率方程为: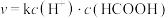 ,k为反应速率常数。
,k为反应速率常数。 温度下,HCOOH电离平衡常数为
温度下,HCOOH电离平衡常数为 ,当HCOOH平衡浓度为xmol/L时,
,当HCOOH平衡浓度为xmol/L时, 浓度为
浓度为___________ mol/L,此时反应速率
___________  (用含
(用含 、x和k的代数式表示)。
、x和k的代数式表示)。
(1)实验表明,液氨也能像水那样进行自耦电离(
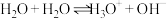 ),写出液氨自耦电离的方程式
),写出液氨自耦电离的方程式(2)室温下,在48mL
 的醋酸溶液中加入12mL0.4mol/L的KOH溶液,所得溶液呈
的醋酸溶液中加入12mL0.4mol/L的KOH溶液,所得溶液呈(3)常温下,
 的下列溶液中,水电离出的
的下列溶液中,水电离出的 由大到小的顺序是
由大到小的顺序是①HNO3 ②H2SO4 ③CH3COOH(
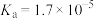 ) ④
) ④ (
( ) ⑤NaOH ⑥
) ⑤NaOH ⑥
(4)某温度时,0.1mol/L的NaOH溶液的pH是11,在此温度下,将
 的盐酸溶液
的盐酸溶液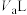 与
与 的NaOH溶液
的NaOH溶液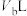 混合,所得混合液为中性,若
混合,所得混合液为中性,若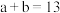 ,则
,则
(5)H2A在水溶液中的电离如下:
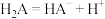 ,
, ,
,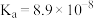 向H2A溶液中滴加少量氨水,该反应的离子方程式为
向H2A溶液中滴加少量氨水,该反应的离子方程式为(6)已知甲酸在一定条件下发生此反应:
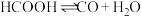 ,正反应速率方程为:
,正反应速率方程为: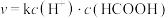 ,k为反应速率常数。
,k为反应速率常数。 温度下,HCOOH电离平衡常数为
温度下,HCOOH电离平衡常数为 ,当HCOOH平衡浓度为xmol/L时,
,当HCOOH平衡浓度为xmol/L时, 浓度为
浓度为
 (用含
(用含 、x和k的代数式表示)。
、x和k的代数式表示)。
您最近一年使用:0次
【推荐1】光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可做太阳电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CuInSe等。
(1)已知Se在周期表的位置为_____ ,基态Ga原子核外电子占据的最高能级为_____ 。
(2)P、S、Ga电负性从大到小的顺序为_____ 。
(3)与Al元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,[B(OH)4]-的结构式为____ (标出配位键)
(4)已知[Cu(H2O)4]2+具有对称的空间构型,[Cu(H2O)4]2+中的2个H2O被Cl-取代,能得到2种不同结构的产物,则[Cu(H2O)4]2+的空间构型为_____ 。请画出该离子中配位键的结合形式__ 。
(1)已知Se在周期表的位置为
(2)P、S、Ga电负性从大到小的顺序为
(3)与Al元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,[B(OH)4]-的结构式为
(4)已知[Cu(H2O)4]2+具有对称的空间构型,[Cu(H2O)4]2+中的2个H2O被Cl-取代,能得到2种不同结构的产物,则[Cu(H2O)4]2+的空间构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硼砂是含结晶水的四硼酸钠。以硼砂为原料,可以得到BF3、BN和硼酸等重要化合物,请根据下列信息回答有关问题。
(1)硼砂中阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示,则在Xm-中,2号硼原子的杂化类型为____ ;4号硼原子是否参与形成配位键?____ (填“是”或“否”)。

(2)BN中B的化合价为____ ,请解释原因:____ 。
(3)BF3和过量NaF作用可生成NaBF4,BF 的空间结构为
的空间结构为____ 。
(1)硼砂中阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示,则在Xm-中,2号硼原子的杂化类型为

(2)BN中B的化合价为
(3)BF3和过量NaF作用可生成NaBF4,BF
 的空间结构为
的空间结构为
您最近一年使用:0次
【推荐1】氧族元素的单质及其化合物对人类的生活、生产有着举足轻重的影响。如氧气、水、二氧化硫等。
(1)氧族元素原子最外层电子数与次外层中p亚层电子数相同的元素名称是___ ;硫单质常见形式是S8,它的摩尔质量是___ ;Se是人体不可或缺的微量元素,它在周期表中的位置是___ ,Se原子最外层轨道表示式___ 。
(2)在氧、硫、硒(Se)、碲(Te)元素原子形成的简单阴离子中,其离子半径由大到小的顺序为__ (用离子符号表示)。用化学方程式表示SO2形成硫酸型酸雨的反应__ 。
(3)氧族元素的单质及其化合物的性质存在着相似性和递变性。下列有关说法正确的是___
A.氧族元素气态氢化物的稳定性按H2O、H2S、H2Se、H2Te的顺序依次减弱
B.其氢化物中的键长按O—H、S—H、Se—H、Te—H的顺序依次减小
C.其阴离子的还原性按O2–、S2–、Se2–、Te2–的顺序依次增强
D.其最高价氧化物的水化物酸性按H2SO4、H2SeO4、H2TeO4顺序依次增强
(4)亚硫酸钠和碘酸钾在酸性溶液里反应生成硫酸钠、硫酸钾、碘和水。
__ Na2SO3+__ KIO3+__ H2SO4
__ Na2SO4+__ K2SO4+__ I2+_ H2O配平该反应,若反应中有0.5mol电子转移,则生成的碘是___ g。
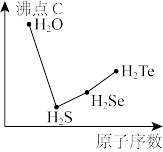
(5)从图中可知氧族元素氢化物的沸点变化规律是__ 。
(1)氧族元素原子最外层电子数与次外层中p亚层电子数相同的元素名称是
(2)在氧、硫、硒(Se)、碲(Te)元素原子形成的简单阴离子中,其离子半径由大到小的顺序为
(3)氧族元素的单质及其化合物的性质存在着相似性和递变性。下列有关说法正确的是
A.氧族元素气态氢化物的稳定性按H2O、H2S、H2Se、H2Te的顺序依次减弱
B.其氢化物中的键长按O—H、S—H、Se—H、Te—H的顺序依次减小
C.其阴离子的还原性按O2–、S2–、Se2–、Te2–的顺序依次增强
D.其最高价氧化物的水化物酸性按H2SO4、H2SeO4、H2TeO4顺序依次增强
(4)亚硫酸钠和碘酸钾在酸性溶液里反应生成硫酸钠、硫酸钾、碘和水。

(5)从图中可知氧族元素氢化物的沸点变化规律是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】正误判断。
1.在周期表里,主族元素所在的族序数等于原子核外电子数。______
2.元素的原子序数越大,其原子半径也越大。______
3.在周期表里,元素所在的周期数等于原子核外电子层数。______
4.氢键是化学键。______
5.碘化氢的沸点比氯化氢的沸点高是由于碘化氢分子之间存在氢键。______
6.乙醇分子跟水分子之间只存在范德华力。______
1.在周期表里,主族元素所在的族序数等于原子核外电子数。
2.元素的原子序数越大,其原子半径也越大。
3.在周期表里,元素所在的周期数等于原子核外电子层数。
4.氢键是化学键。
5.碘化氢的沸点比氯化氢的沸点高是由于碘化氢分子之间存在氢键。
6.乙醇分子跟水分子之间只存在范德华力。
您最近一年使用:0次

 是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:
是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题: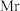 )的晶胞结构如图a所示,阿伏加德罗常数为
)的晶胞结构如图a所示,阿伏加德罗常数为 ,则
,则 (列计算式),图b为
(列计算式),图b为 原子沿z轴方向向
原子沿z轴方向向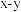 平面投影的位置,在图b中画出S原子在该方向的投影位置
平面投影的位置,在图b中画出S原子在该方向的投影位置
 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸) ,下列叙述正确的有
,下列叙述正确的有

