下列判断中一定正确的是
A.若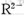 和M+的电子层结构相同,则原子序数:R〉M 和M+的电子层结构相同,则原子序数:R〉M |
| B.若X、Y都是气态氢化物,且相对分子质量:X〉Y,则沸点:X〉Y |
| C.若M、N是同主族元素,且原子序数:M〉N,则非金属性:M>N |
| D.若X、Y属于同主族元素,且相对原子质量:X〉Y,则X失电子能力比Y的强 |
11-12高三上·湖南·阶段练习 查看更多[1]
(已下线)2012届湖南省长郡中学高三上学期第二次月考化学试卷
更新时间:2016-12-09 02:19:04
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】已知M2+有2个电子层,则M在元素周期表中的位置是
| A.第2周期0族 | B.第2周期Ⅷ族 | C.第2周期ⅡA族 | D.第3周期ⅡA族 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】X、Y、Z、W为原子序数依次增大的4种短周期主族元素,X和W同主族,Z与W相邻,X的最外层电子数是内层的两倍,Y的最高价氧化物的水化物是一元酸。下列说法不正确 的是
A.最简单氢化物的沸点: | B.简单离子的半径: |
C.元素非金属性: | D.Z的单质能与NaOH溶液反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】现有三种元素的基态原子的电子排布式如下:
① ②
② ③1s22s22p63s23p4
③1s22s22p63s23p4
下列有关比较中正确的是
①
 ②
② ③1s22s22p63s23p4
③1s22s22p63s23p4下列有关比较中正确的是
| A.原子半径:③>②>① | B.非金属性:③>②>① |
| C.电负性:①>②>③ | D.第一电离能:①>②>③ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】利用CO2是实现“碳中和”的重要途径,CO2光催化转化为CH4的方法入选了2020年世界十大科技进展,其原理为CO2+4H2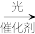 CH4+2H2O。下列有关CO2、CH4的说法正确的是
CH4+2H2O。下列有关CO2、CH4的说法正确的是
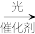 CH4+2H2O。下列有关CO2、CH4的说法正确的是
CH4+2H2O。下列有关CO2、CH4的说法正确的是| A.CO2的空间构型是V形 | B.CH4是极性分子 |
| C.非金属性:O>C>H | D.CO2转化为CH4体现了CO2的还原性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】X、Y是元素周期表中的两种元素。下列叙述中能说明X的非金属性比Y强的是
| A.X氢化物水溶液的酸性比Y的氢化物水溶液的酸性强 |
| B.达8电子结构时X原子得到电子数比Y多 |
| C.X的氧化物的水化物的酸性比Y的氧化物的水化物的酸性强 |
| D.X的单质能将Y从NaY 的溶液中置换出来 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】V、W、X、Y是元素周期表中短周期元素,在周期表中的位置关系如下图所示:
Z为第四周期常见的元素,该元素是人体血液中血红蛋白的组成金属元素。V的最简单氢化物为甲,W的气态氢化物为乙,甲、乙混合时有白烟生成,甲能使湿润的红色石蕊试纸变蓝,W与Z可形成化合物ZW3。下列说法正确的是( )
| Y | V | …… | ||
| X | …… | W |
| A.原子半径:X>Y>V>W |
| B.甲、乙混合时所生成的白烟为离子化合物,但其中含有共价键 |
| C.X、W的质子数之和与最外层电子数之和的比值为 2∶1 |
| D.在足量的沸水中滴入含有16.25 g ZW3的溶液可得到0.1 mol Z(OH)3胶粒 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知几种短周期元素的原子半径、常见的最高价和最低价如下表,下列说法下不正确的是( )
| 元素性质 | 元素编号 | ||||||
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
| 原子半径(nm) | 0.073 | 0.075 | 0.152 | 0.110 | 0.099 | 0.186 | 0.143 |
| 最高正化合价 | 无 | +5 | +1 | +5 | +7 | +1 | +3 |
| 最低负化合价 | ﹣2 | ﹣3 | 无 | ﹣3 | ﹣1 | 无 | 无 |
| A.⑦的简单离子不是同周期元素离子半径最小的 |
| B.气态氢化物的稳定性①>② |
| C.②的气态氢化物浓溶液可用于检验氯气管道的泄漏 |
| D.阴离子的还原性④大于⑤,最高价氧化物的水化物的碱性③小于⑥ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】一种在工业生产中有广泛用途的有机高分子结构片段如图。下列关于该高分子的说法正确的是
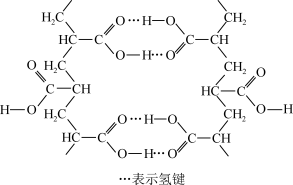

| A.能水解成小分子 | B.该分子中所有碳原子可能共平面 |
| C.氢键可增大该分子熔点 | D.单体可发生氧化、取代、消去反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】a、b、c、d、e是原子序数依次增大的五种短周期主族元素。b、c、e最外层电子数之和为10;a原子核外最外层电子数是次外层的2倍;c是同周期中原子半径最大的元素;工业上一般通过电解氧化物的方法制备d的单质;e的单质是制备太阳能电池的重要材料。下列说法正确的是
| A.a、e的常见氧化物都属于酸性氧化物 |
| B.b元素的气态氧化物易液化,是因为其分子间能形成氢键 |
| C.工业上不用电解氯化物的方法制备单质d是由于其氯化物的熔点高 |
| D.相同质量的c和d单质分别与足量稀盐酸反应,前者生成的氢气多 |
您最近一年使用:0次

 分子。下列说法不正确的是
分子。下列说法不正确的是

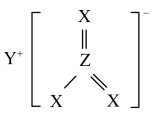

 含有配位键
含有配位键

