下列说法正确的是
| A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以增大生成氢气的速率 |
| B.100mL 2mol·L-1盐酸与锌片反应,加入适量的氯化钠溶液,反应速率不变 |
| C.二氧化硫的催化氧化是一个放热反应,升高温度,反应速率降低 |
| D.汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,使用催化剂可以增大反应速率 |
更新时间:2019-06-06 07:44:56
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
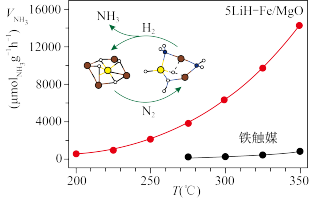
【推荐1】中国科学家在合成氨(N2+3H2 2NH3△H<0)反应机理研究中取得新进展,首次报道了LiH-3d过渡金属这一复合催化剂体系,并提出了“氮转移”催化机理,如图所示。下列说法不正确的是( )
2NH3△H<0)反应机理研究中取得新进展,首次报道了LiH-3d过渡金属这一复合催化剂体系,并提出了“氮转移”催化机理,如图所示。下列说法不正确的是( )
 2NH3△H<0)反应机理研究中取得新进展,首次报道了LiH-3d过渡金属这一复合催化剂体系,并提出了“氮转移”催化机理,如图所示。下列说法不正确的是( )
2NH3△H<0)反应机理研究中取得新进展,首次报道了LiH-3d过渡金属这一复合催化剂体系,并提出了“氮转移”催化机理,如图所示。下列说法不正确的是( )
| A.过程中有极性键形成 |
| B.复合催化剂降低了反应的活化能 |
| C.复合催化剂能降低合成氨反应的焓变 |
| D.350℃,催化效率:5LiH-Fe/MgO>铁触媒 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关反应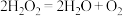 的说法中不正确的是
的说法中不正确的是
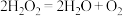 的说法中不正确的是
的说法中不正确的是A.生成标准状况下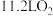 转移 转移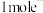 | B. 溶液能催化该反应 溶液能催化该反应 |
C.该反应的熵变 | D.该反应在任意温度下均能自发进行 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】100mL 2 mol·L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的量,可采用的方法是
| A.加入数滴CuCl2溶液 | B.加入适量的6mol·L-1的盐酸 |
| C.加入适量蒸馏水 | D.加入适量的NaCl溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】实验室中,用20mL浓度为3mol/L的稀硫酸与过量的锌粒在一定温度下发生反应制取氢气,为了降低反应速率,但又不影响生成氢气的总量,下列措施能达到目的的是
A.向稀硫酸中加 溶液 溶液 | B.将锌粒制成薄锌片 |
C.向稀硫酸中加 固体 固体 | D.向稀硫酸中加 溶液 溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】NO和CO都是汽车排放尾气中的有害物质,它们能缓慢地反应,生成N2和CO2,对此反应下列叙述正确的
| A.使用催化剂并不能改变反应速率 | B.使用催化剂可以加快反应速率 |
| C.降低压强能加快反应速率 | D.降温可以加快反应速率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】某温度下,在恒容密闭容器中进行反应: 。下列叙述正确的是
。下列叙述正确的是
 。下列叙述正确的是
。下列叙述正确的是| A.当容器中气体压强不变时,反应达到平衡 |
| B.升高温度,正反应速率增大,逆反应速率减小 |
| C.加入少量Z,逆反应速率增大 |
D.平衡后,加入Y,该反应的 增大 增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列关于化学反应速率的说法正确的是
①恒温时,增大压强,化学反应速率一定加快
②其他条件不变,温度越高化学反应速率越快
③使用催化剂可改变反应速率,从而改变该反应过程中吸收或放出的热量
④3mol/(L·s)的反应速率一定比1mol/(L·s)的反应速率大
⑤有气体参加的化学反应,若增大压强 即缩小反应容器的体积
即缩小反应容器的体积 ,可增加单位体积内活化分子数,从而使反应速率增大
,可增加单位体积内活化分子数,从而使反应速率增大
①恒温时,增大压强,化学反应速率一定加快
②其他条件不变,温度越高化学反应速率越快
③使用催化剂可改变反应速率,从而改变该反应过程中吸收或放出的热量
④3mol/(L·s)的反应速率一定比1mol/(L·s)的反应速率大
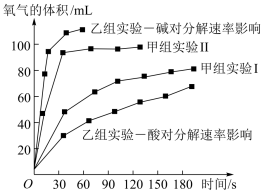
⑤有气体参加的化学反应,若增大压强
 即缩小反应容器的体积
即缩小反应容器的体积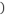 ,可增加单位体积内活化分子数,从而使反应速率增大
,可增加单位体积内活化分子数,从而使反应速率增大| A.②③ | B.②⑤ | C.①②⑤ | D.②④⑤ |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】一定量的锌与过量的稀H2SO4反应制取氢气,一定温度下为减慢反应速率而又不影响产生氢气的量,可向其中加入( )
| A.CH3COOK固体 | B.CuCl2固体 | C.KNO3溶液 | D.铁粉 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】100 mL 6 mol•L﹣1的H2SO4跟过量的锌反应,在一定温度下,为减缓反应速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
| A.硫酸钠固体 | B.水 | C.2 mol•L﹣1硫酸溶液 | D.硝酸钾溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】现有甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素(仅一个条件改变)。甲小组有如下实验设计方案。
甲、乙两小组得出如图数据:
关于该实验下列叙述不正确 的是
| 实验编号 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 25℃ | 三氧化二铁 | 10mL 5%H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |

关于该实验下列叙述
A.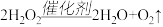 中,O2是氧化产物 中,O2是氧化产物 |
| B.甲小组实验得出的结论是Fe2O3比MnO2催化效率更高 |
| C.甲小组实验也可以测定25℃时,在相同时间内产生氧气的体积 |
| D.乙组研究的影响因素的数据分析,相同条件下H2O2在碱性环境下放出气体速率较快 |
您最近一年使用:0次

 的核聚变释放的能量属于清洁能源
的核聚变释放的能量属于清洁能源 制甲酸
制甲酸

