在普通铝中加入少量Cu和Mg后,形成一种称为拉维斯相的MgCu2微小晶粒,其分散在Al中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要材料。回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是____________ (填标号)。
A. B.
B.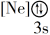 C.
C. D.
D.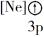
(2)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是__________ 、__________ 。乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是__________ ,其中与乙二胺形成的化合物稳定性相对较高的是__________ (填“Mg2+”或“Cu2+”)。
(3)一些氧化物的熔点如下表所示:
解释表中氧化物之间熔点差异的原因__________ 。
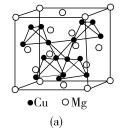
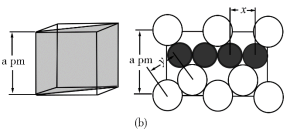
(4)图(a)是MgCu2的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图(b)是沿立方格子对角面取得的截图。可见,Cu原子之间最短距离x=__________ pm,Mg原子之间最短距离y=__________ pm。设阿伏加 德罗常数的值为NA,则MgCu2的密度是__________ g·cm−3(列出计算表达式)。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是
A.
 B.
B.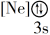 C.
C. D.
D.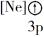
(2)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是
(3)一些氧化物的熔点如下表所示:
| 氧化物 | Li2O | MgO | P4O6 | SO2 |
| 熔点/°C | 1570 | 2800 | 23.8 | −75.5 |
(4)图(a)是MgCu2的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图(b)是沿立方格子对角面取得的截图。可见,Cu原子之间最短距离x=


2019·全国·高考真题 查看更多[13]
2019年全国统一考试化学试题(新课标Ⅰ)吉林省延边市第二中学2020届高三入学考试化学试题(已下线)专题6.4 物质结构与性质(选考)(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)押全国卷理综第35题 物质结构与性质-备战2021年高考化学临考题号押题2020年全国卷Ⅰ理综化学高考真题变式题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)押全国卷理综第35题 物质结构与性质-备战2022年高考化学临考题号押题(课标全国卷)(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题20 结构与性质(已下线)T35-物质结构与性质
更新时间:2019-06-09 10:58:44
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件。
(1)基态铜原子的价电子排布式为________ 。
(2)磷化铜与水作用产生有毒的磷化氢(PH3)。
①PH3分子中的中心原子的杂化方式是________ 。
②P与N同主族,其最高价氧化物对应水化物的酸性:HNO3________ H3PO4(填“>”或“<”),从结构的角度说明理由:________ 。
(3)磷青铜中的锡、磷两种元素电负性的大小为Sn________ P(填“>”“<”或“=”)。
(4)某磷青铜晶胞结构如下图所示。

①则其化学式为________ 。
②该晶体中距离Cu原子最近的Sn原子有________ 个,这些Sn原子所呈现的构型为________ 。
(1)基态铜原子的价电子排布式为
(2)磷化铜与水作用产生有毒的磷化氢(PH3)。
①PH3分子中的中心原子的杂化方式是
②P与N同主族,其最高价氧化物对应水化物的酸性:HNO3
(3)磷青铜中的锡、磷两种元素电负性的大小为Sn
(4)某磷青铜晶胞结构如下图所示。

①则其化学式为
②该晶体中距离Cu原子最近的Sn原子有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】2022年4月16日神舟13号载人飞行任务取得圆满成功,高性能金属材料铝合金、钛合金、镁合金、超强度钢等作用功不可没。回答下列问题:
(1)铁元素在周期表中的位置是_______ ,基态 的价电于排布式为
的价电于排布式为_______ 。
(2)镁与同周期相邻的两种元素的第一电离能由大到小排列顺序为_______ 。
(3)常温下, 是无色液体,其熔点为250K,沸点为409K。通过与铵盐反应可生成
是无色液体,其熔点为250K,沸点为409K。通过与铵盐反应可生成 。
。
① 的熔点低于
的熔点低于 的原因是
的原因是_______ 。
② 中,
中,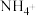 的空间构型是
的空间构型是_______ 。
(4) 是金红石的主要成分,其晶胞结构如图所示,设Ti和O原子半径分别为
是金红石的主要成分,其晶胞结构如图所示,设Ti和O原子半径分别为 和
和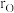 (单位:pm),晶胞的长宽高分别为a、b、c(单位:cm),则晶胞中原子的空间利用率为
(单位:pm),晶胞的长宽高分别为a、b、c(单位:cm),则晶胞中原子的空间利用率为_______ (列出计算表达式)。(空间利用率指构成晶体的原子、离子或分子在整个晶体空间中所占有的体积百分比)

(1)铁元素在周期表中的位置是
 的价电于排布式为
的价电于排布式为(2)镁与同周期相邻的两种元素的第一电离能由大到小排列顺序为
(3)常温下,
 是无色液体,其熔点为250K,沸点为409K。通过与铵盐反应可生成
是无色液体,其熔点为250K,沸点为409K。通过与铵盐反应可生成 。
。①
 的熔点低于
的熔点低于 的原因是
的原因是②
 中,
中,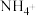 的空间构型是
的空间构型是(4)
 是金红石的主要成分,其晶胞结构如图所示,设Ti和O原子半径分别为
是金红石的主要成分,其晶胞结构如图所示,设Ti和O原子半径分别为 和
和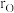 (单位:pm),晶胞的长宽高分别为a、b、c(单位:cm),则晶胞中原子的空间利用率为
(单位:pm),晶胞的长宽高分别为a、b、c(单位:cm),则晶胞中原子的空间利用率为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钡的化合物在生产、生活中有重要的应用。
回答下列问题:
(1)钡元素是第六周期的碱土金属元素,其基态原子的最外层电子轨道表示式为___________ 。
(2)钡元素在自然界中主要以重晶石形式存在,其成分为 ,其中所含三种元素的电负性从大到小的顺序为
,其中所含三种元素的电负性从大到小的顺序为___________ (用元素符号表示); 的空间构型为
的空间构型为___________ ,其中S原子的杂化方式为___________ 。
(3)BaO与MgO相比,熔点较高的为___________ (填“BaO”或“MgO”),原因为___________ 。
(4)氯化钡的玻恩哈伯循环如图所示:

①由图可知,Cl-Cl键的键能为___________ 。
②由图可知,Ba的第一电离能 ,第二电离能
,第二电离能 ,从微观结构角度解释
,从微观结构角度解释 的原因:
的原因:___________ 。
③元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能( ),则Cl的第一电子亲和能
),则Cl的第一电子亲和能
___________ 。
(5)氟化钡的晶胞结构如图所示。其中 的配位数为
的配位数为___________ ;若相邻两个 的核间距离为apm,
的核间距离为apm, 表示阿伏加德罗常数的值,则氟化钡的密度
表示阿伏加德罗常数的值,则氟化钡的密度
___________  (用含a、
(用含a、 的代数式表示,列出计算式即可)。
的代数式表示,列出计算式即可)。

回答下列问题:
(1)钡元素是第六周期的碱土金属元素,其基态原子的最外层电子轨道表示式为
(2)钡元素在自然界中主要以重晶石形式存在,其成分为
 ,其中所含三种元素的电负性从大到小的顺序为
,其中所含三种元素的电负性从大到小的顺序为 的空间构型为
的空间构型为(3)BaO与MgO相比,熔点较高的为
(4)氯化钡的玻恩哈伯循环如图所示:

①由图可知,Cl-Cl键的键能为
②由图可知,Ba的第一电离能
 ,第二电离能
,第二电离能 ,从微观结构角度解释
,从微观结构角度解释 的原因:
的原因:③元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(
 ),则Cl的第一电子亲和能
),则Cl的第一电子亲和能
(5)氟化钡的晶胞结构如图所示。其中
 的配位数为
的配位数为 的核间距离为apm,
的核间距离为apm, 表示阿伏加德罗常数的值,则氟化钡的密度
表示阿伏加德罗常数的值,则氟化钡的密度
 (用含a、
(用含a、 的代数式表示,列出计算式即可)。
的代数式表示,列出计算式即可)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】硫酸四氨合铜晶体( )常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备
)常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备 的流程如下:
的流程如下:
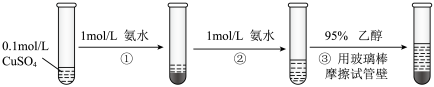
请回答:
(1)写出过程②发生反应的离子方程式_______ 。
(2)过程③加入95%乙醇的作用是_______ 。
(3)根据①→②→③的现象,给出相应微粒与 结合由弱到强的排序
结合由弱到强的排序_______ 。
(4) 具有对称的空间构型,若其中两个
具有对称的空间构型,若其中两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为_______ 。
(5)下列说法正确的是_______。
 )常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备
)常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备 的流程如下:
的流程如下:
请回答:
(1)写出过程②发生反应的离子方程式
(2)过程③加入95%乙醇的作用是
(3)根据①→②→③的现象,给出相应微粒与
 结合由弱到强的排序
结合由弱到强的排序(4)
 具有对称的空间构型,若其中两个
具有对称的空间构型,若其中两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为(5)下列说法正确的是_______。
A.③中发生反应的离子方程式为: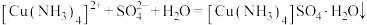 |
| B.③中用玻璃棒摩擦器壁可以促进晶体析出 |
C. 晶体中存在共价键、配位键、离子键和氢键 晶体中存在共价键、配位键、离子键和氢键 |
D.硫酸四氨合铜晶体在水中的电离方程式为: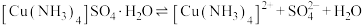 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铜和锌在工业中有重要作用。回答下列问题:
(1)已知氢氧化铜能溶于氨水形成[Cu(NH3)4]2+,则1mol[Cu(NH3)4]2+中含有______ 个σ键。
(2)CuO和Cu2O都能溶于盐酸,且Cu2O易发生歧化反应,写出Cu2O与盐酸反应的离子方程式________ 。
(3)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_______ Ⅰ1(Cu)(填“大于”或“小于”),原因是_______________________ 。
(4)ZnF2具有较高的熔点(872℃),而ZnCl2、ZnBr2、ZnI2熔点都比较低,原因是________________ 。
(5)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为_____________ ,C原子的杂化形式为_____________ 。
(1)已知氢氧化铜能溶于氨水形成[Cu(NH3)4]2+,则1mol[Cu(NH3)4]2+中含有
(2)CuO和Cu2O都能溶于盐酸,且Cu2O易发生歧化反应,写出Cu2O与盐酸反应的离子方程式
(3)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)
(4)ZnF2具有较高的熔点(872℃),而ZnCl2、ZnBr2、ZnI2熔点都比较低,原因是
(5)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】我国科学家制备了一种 太阳电池,其结构示意图如下。
太阳电池,其结构示意图如下。
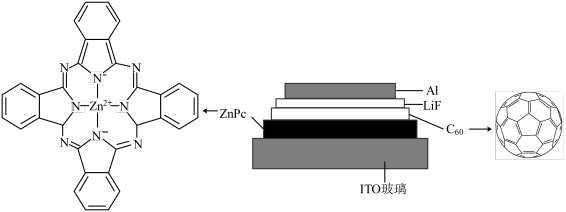
(1)铝元素属于______ 区(填“s”“d”“ds”或“p”)。
(2) 分子中60个碳原子都是等价的,均以近似
分子中60个碳原子都是等价的,均以近似_____ 杂化的方式形成3个不共平面的 键,余下的1个p轨道电子互相重叠形成闭壳层电子结构,
键,余下的1个p轨道电子互相重叠形成闭壳层电子结构, 电子云分布在
电子云分布在 分子笼的内外层表面上。循环伏安测试表明:
分子笼的内外层表面上。循环伏安测试表明: 在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。
在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。
(3)① 中基态
中基态 的电子排布式为
的电子排布式为_______ 。
② 中存在配位键的原因是
中存在配位键的原因是________ 。
(4)某溶剂中, 可以和
可以和 形成分子间电荷转移复合物,反应方程式可表示为:
形成分子间电荷转移复合物,反应方程式可表示为: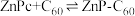 ,不同温度下生成电荷转移复合物的平衡常数如下表。
,不同温度下生成电荷转移复合物的平衡常数如下表。
反应: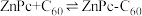

____ 0(填“>”或。“<”),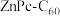 中
中 是电子
是电子_____ (填“给体”或“受体”)。
(5) 晶体结构属于氯化钠型,其晶胞结构如图所示。
晶体结构属于氯化钠型,其晶胞结构如图所示。

① 的熔点和沸点比
的熔点和沸点比 的高,请解释原因
的高,请解释原因________ 。
② 晶体的密度约为
晶体的密度约为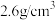 ,
, 晶胞的体积约为
晶胞的体积约为______  (计算结果保留一位有效数字)。
(计算结果保留一位有效数字)。
③一种 的晶胞如图所示。
的晶胞如图所示。
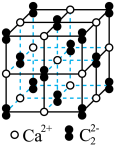
 晶体属于
晶体属于_____ (填晶体类型)晶体,每个 在
在____ 个阴离子构成的多面体中心。一个 晶胞中,含有
晶胞中,含有____ 个 键和
键和____ 个 键。
键。
 太阳电池,其结构示意图如下。
太阳电池,其结构示意图如下。
(1)铝元素属于
(2)
 分子中60个碳原子都是等价的,均以近似
分子中60个碳原子都是等价的,均以近似 键,余下的1个p轨道电子互相重叠形成闭壳层电子结构,
键,余下的1个p轨道电子互相重叠形成闭壳层电子结构, 电子云分布在
电子云分布在 分子笼的内外层表面上。循环伏安测试表明:
分子笼的内外层表面上。循环伏安测试表明: 在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。
在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。(3)①
 中基态
中基态 的电子排布式为
的电子排布式为②
 中存在配位键的原因是
中存在配位键的原因是(4)某溶剂中,
 可以和
可以和 形成分子间电荷转移复合物,反应方程式可表示为:
形成分子间电荷转移复合物,反应方程式可表示为: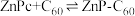 ,不同温度下生成电荷转移复合物的平衡常数如下表。
,不同温度下生成电荷转移复合物的平衡常数如下表。| 温度 | 生成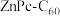 的K 的K |
 | 1.2329 |
 | 0.9674 |
 | 0.4923 |
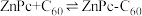

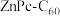 中
中 是电子
是电子(5)
 晶体结构属于氯化钠型,其晶胞结构如图所示。
晶体结构属于氯化钠型,其晶胞结构如图所示。
①
 的熔点和沸点比
的熔点和沸点比 的高,请解释原因
的高,请解释原因②
 晶体的密度约为
晶体的密度约为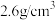 ,
, 晶胞的体积约为
晶胞的体积约为 (计算结果保留一位有效数字)。
(计算结果保留一位有效数字)。③一种
 的晶胞如图所示。
的晶胞如图所示。
 晶体属于
晶体属于 在
在 晶胞中,含有
晶胞中,含有 键和
键和 键。
键。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1) 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 中的阴离子空间构型是
中的阴离子空间构型是_______ 、中心原子的杂化形式为_______ 。
(2)①根据价层电子对互斥理论,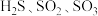 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是_______ 。
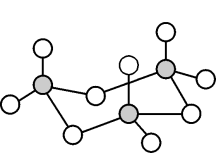
②气态三氧化硫以单分子形式存在,其分子的立体构型为_______ 形,其中共价键的类型有_______ 种;固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为_______ 。
(3)《中华本草》等中医典籍中,记载了炉甘石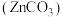 入药,可用于治疗皮肤炎症或表面创伤。
入药,可用于治疗皮肤炎症或表面创伤。 中,阴离子空间构型为
中,阴离子空间构型为_______ ,C原子的杂化形式为_______ 。
(1)
 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 中的阴离子空间构型是
中的阴离子空间构型是(2)①根据价层电子对互斥理论,
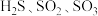 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是②气态三氧化硫以单分子形式存在,其分子的立体构型为

(3)《中华本草》等中医典籍中,记载了炉甘石
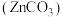 入药,可用于治疗皮肤炎症或表面创伤。
入药,可用于治疗皮肤炎症或表面创伤。 中,阴离子空间构型为
中,阴离子空间构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为_______ 。
(2)Ti的四卤化物熔点如下表所示,自TiCl4至TiI4熔点依次升高,原因是_______ 。
(3)CaTiO3的晶胞如图(a)所示,其组成元素的电负性大小顺序是_______ ;金属离子与氧离子间的作用力为_______ ,Ca2+紧邻的O2-有_______ 个。
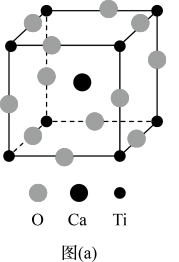
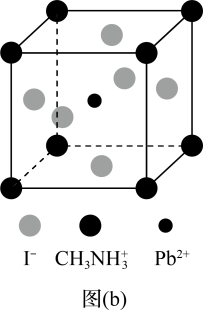
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I﹣和有机碱离子 ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中_______ 的空间位置相同,有机碱 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是_______ ;若晶胞参数为a nm,则晶体密度为_______ g·cm-3(列出计算式)。
(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如下表所示,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | ﹣24.12 | 38.3 | 155 |

(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I﹣和有机碱离子
 ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】La2CuO4在传感器、汽车尾气催化净化、氮氧化物催化消除、中温固体氧化物燃料电池等领域具有良好的应用前景,回答下列问题:
(1)基态Cu原子的核外电子排布式为___________ 。
(2)缩二脲[HN(CONH2)2]是一种有机化合物,分子中氮、碳的杂化类型分别是___________ 、___________ 。1 mol缩二脲中含有σ键的数目为___________ ,缩二脲能与Cu2+形成稳定离子,其原因是___________ 。
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系La2CuO4的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。
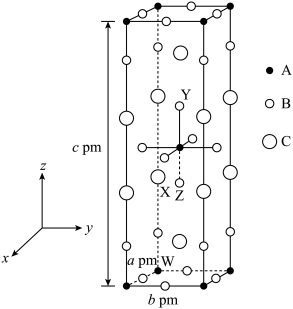
①B原子代表___________ ,C原子代表___________ ,与A原子距离最近的氧原子个数为___________ 。
②Z用分数坐标表示为___________ 。
③设阿伏加德罗常数的值为NA,则La2CuO4的密度是___________ g·cm-3(列出计算表达式)。
(1)基态Cu原子的核外电子排布式为
(2)缩二脲[HN(CONH2)2]是一种有机化合物,分子中氮、碳的杂化类型分别是
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系La2CuO4的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。

分数坐标 原子 | x | y | z |
| W | 0 | 0 | 0 |
| X | 0 | 0 |  |
| Y |  |  |  |
②Z用分数坐标表示为
③设阿伏加德罗常数的值为NA,则La2CuO4的密度是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】氢能是一种极具发展潜力的清洁能源,下列物质都是具有广阔应用前景的储氢材料。回答下列问题:
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原产物为_____ 。
(2)Ti-Fe合金室温下吸、放氢的速率快,Ti元素在周期表中的位置是____ 。
(3) (氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成。
进行合成。
① 中涉及的元素H、B、N电负性最大的是
中涉及的元素H、B、N电负性最大的是______ 。
②键角:
_____  (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是_______ 。
(4)Fe-Mg合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
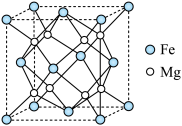
①距离Mg原子最近的Fe原子个数是___________ 。
②若该晶胞的棱长为anm,阿伏加德罗常数的值为 ,则该合金的密度为
,则该合金的密度为___________  。
。
③若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下 的体积约为
的体积约为___________ L。
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原产物为
(2)Ti-Fe合金室温下吸、放氢的速率快,Ti元素在周期表中的位置是
(3)
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成。
进行合成。①
 中涉及的元素H、B、N电负性最大的是
中涉及的元素H、B、N电负性最大的是②键角:

 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是(4)Fe-Mg合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离Mg原子最近的Fe原子个数是
②若该晶胞的棱长为anm,阿伏加德罗常数的值为
 ,则该合金的密度为
,则该合金的密度为 。
。③若该晶体储氢时,
 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下 的体积约为
的体积约为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】第一代半导体材料(Si、Ge等) 与第二代半导体材料(GaAs、 InSb等)一起,将人类推进了信息时代。近年来,以碳化硅(SiC)、氮化镓(GaN)为代表的第三代半导体材料的出现,开辟了人类资源和能源节约型社会的新发展,也成为了科学家研究的热点。
(1)N、P、AS位于同一主族,基态氮原子的核外共有___ 种不同运动状态的电子,N2O的空间构型为_______ 。
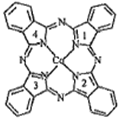
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学中的光敏剂、催化剂等方面得到广泛的应用,其结构如图所示,中心离子为钴离子。 酞菁钻中碳原子的杂化轨道类型为___ ;与钴离子通过配位键结合的氮原子的编号是_______ 。
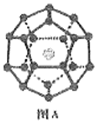
(3)C与N处于同周期相邻元素,C形成的一种重要物质可燃冰是天然气水合物,具有笼形结构如图A (表面的小球是水分子,内部的大球是甲烷分子)。图A 中最小的环中连接的原子总数是_______ 。 可燃冰晶体具有多种笼状结构,其中一种由1个图A所示笼分别用2 个面与另外两个相同的笼共面而成,则中间笼实际占有____ 个水分子。
(4)已知PH3分子的键角约为94%,而AsH3分子的键角约为91.8°,试用价层电子对互斥理论解释PH3的键角比AsH3的键角大的原因________________ 。
(5) 第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素有____ 。
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示;试从结构的角度分析它们熔点不同的原因__________________ 。
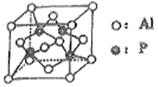
(7)磷化铝晶胞如图所示,若两个铝原子之间的最近距离为dpm,NA代表阿伏伽德罗常数的值,则磷化铝晶体的密度p=_____ g/cm3。
(1)N、P、AS位于同一主族,基态氮原子的核外共有
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学中的光敏剂、催化剂等方面得到广泛的应用,其结构如图所示,中心离子为钴离子。 酞菁钻中碳原子的杂化轨道类型为

(3)C与N处于同周期相邻元素,C形成的一种重要物质可燃冰是天然气水合物,具有笼形结构如图A (表面的小球是水分子,内部的大球是甲烷分子)。图A 中最小的环中连接的原子总数是

(4)已知PH3分子的键角约为94%,而AsH3分子的键角约为91.8°,试用价层电子对互斥理论解释PH3的键角比AsH3的键角大的原因
(5) 第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素有
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示;试从结构的角度分析它们熔点不同的原因
| 物质 | BN | AIN | GaN |
| 熔点/℃ | 3000 | 2200 | 1700 |
(7)磷化铝晶胞如图所示,若两个铝原子之间的最近距离为dpm,NA代表阿伏伽德罗常数的值,则磷化铝晶体的密度p=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】含镓(Ga)化合物在半导体材料、医药行业等领域发挥重要作用。回答下列问题:
(1)基态镓原子最外层的电子排布图为___________ 。
(2)Ga与Zn的第一电离能大小关系为:Ga___________ Zn(填“>”“<”或“=”)。
(3) 的熔沸点如下表所示。
的熔沸点如下表所示。
①100℃, 、
、 和
和 呈液态的是
呈液态的是___________ (填化学式),沸点依次升高的原因是___________ 。
② 的熔点约1000℃,远高于
的熔点约1000℃,远高于 的熔点,原因是
的熔点,原因是___________ 。
(4)镓配合物具有高的反应活性和良好的选择性。在药物领域得到广泛的关注。 与2-甲基8-羟基喹啉(
与2-甲基8-羟基喹啉( )在一定条件下反应可以得到一种喹啉类镓配合物(M),其结构如图所示。2-甲基-8-羟基喹啉分子中碳原子的杂化轨道类型为
)在一定条件下反应可以得到一种喹啉类镓配合物(M),其结构如图所示。2-甲基-8-羟基喹啉分子中碳原子的杂化轨道类型为___________ ;H、C、N的原子半径由大到小的顺序为___________ 。

(5)作为第二代半导体,砷化镓单晶因其价格昂贵而素有“半导体贵族”之称。砷化镓是由 和
和 在一定条件下制备得到,同时得到另一物质,该物质分子是
在一定条件下制备得到,同时得到另一物质,该物质分子是___________ (填“极性分子”或“非极性分子”),  分子的空间形状为
分子的空间形状为___________ 。
(6)GaN是制造LED的重要材料,被誉为“第三代半导体材料”。其晶体结构如图所示:

①在GaN晶体中,距离每个Ga原子最近的Ga原子有___________ 个,N原子的配位数为___________ 。
②GaN的密度为___________  。(设阿伏加德罗常数的值为
。(设阿伏加德罗常数的值为 ,用含a、c、
,用含a、c、 的代数式表示)
的代数式表示)
(1)基态镓原子最外层的电子排布图为
(2)Ga与Zn的第一电离能大小关系为:Ga
(3)
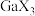 的熔沸点如下表所示。
的熔沸点如下表所示。| 镓的卤化物 |  | 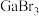 |  |
| 熔点/℃ | 77.75 | 122.3 | 211.5 |
| 沸点/℃ | 201.2 | 279 | 346 |
 、
、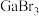 和
和 呈液态的是
呈液态的是②
 的熔点约1000℃,远高于
的熔点约1000℃,远高于 的熔点,原因是
的熔点,原因是(4)镓配合物具有高的反应活性和良好的选择性。在药物领域得到广泛的关注。
 与2-甲基8-羟基喹啉(
与2-甲基8-羟基喹啉( )在一定条件下反应可以得到一种喹啉类镓配合物(M),其结构如图所示。2-甲基-8-羟基喹啉分子中碳原子的杂化轨道类型为
)在一定条件下反应可以得到一种喹啉类镓配合物(M),其结构如图所示。2-甲基-8-羟基喹啉分子中碳原子的杂化轨道类型为
(5)作为第二代半导体,砷化镓单晶因其价格昂贵而素有“半导体贵族”之称。砷化镓是由
 和
和 在一定条件下制备得到,同时得到另一物质,该物质分子是
在一定条件下制备得到,同时得到另一物质,该物质分子是 分子的空间形状为
分子的空间形状为(6)GaN是制造LED的重要材料,被誉为“第三代半导体材料”。其晶体结构如图所示:

①在GaN晶体中,距离每个Ga原子最近的Ga原子有
②GaN的密度为
 。(设阿伏加德罗常数的值为
。(设阿伏加德罗常数的值为 ,用含a、c、
,用含a、c、 的代数式表示)
的代数式表示)
您最近一年使用:0次



