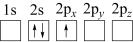
根据电子排布三原理,填写下列空白。
(1)基态Mn2+的核外电子排布式为________ 。
(2)磷原子外围电子排布式为________ 。
(3)氧元素基态原子核外未成对电子数为________ 个。
(1)基态Mn2+的核外电子排布式为
(2)磷原子外围电子排布式为
(3)氧元素基态原子核外未成对电子数为
更新时间:2019-06-20 03:40:54
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)写出基态P原子的价电子排布式:_____ 。基态Fe2+与Fe3+化学性质相对稳定的是____ (填离子符号),解释原因:____ 。
(2)浓磷酸在常温下呈黏稠状,原因是____ ,浓磷酸在200~300℃时脱水生成焦磷酸(化学式:H4P2O7),焦磷酸的结构简式为____ ,其中P的价电子对数为____ ,杂化轨道类型为____ 。
(1)写出基态P原子的价电子排布式:
(2)浓磷酸在常温下呈黏稠状,原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】磷是地壳中含量较为丰富的非金属元素,它的单质和化合物在工农业生产中应用广泛。白磷可通过反应2Ca3(PO4)2+10C→6CaO+P4+10CO获得。完成下列填空:
(1)磷原子的最外层电子排布式是_____ ,氧原子核外有_____ 种不同运动状态的电子。白磷在空气中露置时间长了会因温度达到着火点而自燃,使白磷升温的热量主要来自_____ 。
(2)N和P在周期表中位于_____ 族,PH3分子的空间构型为_____ ,是_____ 分子(填“极性”或“非极性”)。下列能说明N和P非金属性相对强弱的是_____ (填编号)。
a.NH3的稳定性比PH3强 b.NH3的沸点比PH3高
c.硝酸酸性比磷酸强 d.N原子半径比P原子小
铜既能与浓硝酸反应,也能与稀硝酸反应,当铜与一定浓度硝酸反应时,可将化学方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O(未配平,不考虑2NO2 N2O4)。完成下列填空:
N2O4)。完成下列填空:
(3)3Cu+10HNO3→ Cu(NO3)2+
Cu(NO3)2+ NO↑+
NO↑+ NO2↑+
NO2↑+ H2O。配平上述化学方程式,用单线桥法标出电子转移方向和数目。
H2O。配平上述化学方程式,用单线桥法标出电子转移方向和数目。______
(4)0.3molCu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是______ 。
(1)磷原子的最外层电子排布式是
(2)N和P在周期表中位于
a.NH3的稳定性比PH3强 b.NH3的沸点比PH3高
c.硝酸酸性比磷酸强 d.N原子半径比P原子小
铜既能与浓硝酸反应,也能与稀硝酸反应,当铜与一定浓度硝酸反应时,可将化学方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O(未配平,不考虑2NO2
 N2O4)。完成下列填空:
N2O4)。完成下列填空:(3)3Cu+10HNO3→
 Cu(NO3)2+
Cu(NO3)2+ NO↑+
NO↑+ NO2↑+
NO2↑+ H2O。配平上述化学方程式,用单线桥法标出电子转移方向和数目。
H2O。配平上述化学方程式,用单线桥法标出电子转移方向和数目。(4)0.3molCu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同族,它们原子的最外层电子排布式为ns1。B和D也属同族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子的最外层电子数等于D原子的最外层电子数的一半。请回答下列问题:
(1)B是________ ,E是________ 。(用元素符号表示)
(2)写出C元素基态原子的电子排布式:________________________ 。
(3)元素B与D的电负性的大小关系是B____________ D (填“>”“<”或“=”,下同),E与C的第一电离能大小关系是E________ C。
(4)写出元素E和C的最高价氧化物对应的水化物之间反应的离子方程式:_____________ 。
(1)B是
(2)写出C元素基态原子的电子排布式:
(3)元素B与D的电负性的大小关系是B
(4)写出元素E和C的最高价氧化物对应的水化物之间反应的离子方程式:
您最近半年使用:0次
【推荐1】研究含氮化合物对消除环境污染,能源结构的改变,食品添加剂的研究等有重要意义。
(1)甘氨酸锌常用于食品的添加剂,也可代替甘油作烟丝的加香、防冻。一水合甘氨酸锌结构简式如图所示。

①在H、N、O、C、 元素中,不属于P区元素的有:
元素中,不属于P区元素的有:_______
②基态O原子最高能级的原子轨道形状是_______
(2)“中国制造2025”是中国政府实施制造强国战略第一个十年行动领。氮化铬在现代工业中发挥了重要的作用。
①基态N原子的价层电子的轨道表示式为_______ 。
②基态 原子的价层电子排布式为
原子的价层电子排布式为_______ 。
(3) 在空气中存在如下反应:
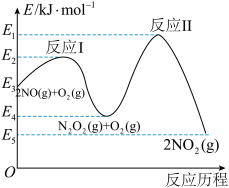
在空气中存在如下反应: ,该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为:
,该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为:_______
(4)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物( 、
、 、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。发生以下反应:
、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。发生以下反应:
Ⅰ.
II.
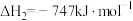
若 的燃烧热为283.5
的燃烧热为283.5 ,则反应Ⅰ的
,则反应Ⅰ的
_______ 
(5)已知1 化学键断开吸收或生成时释放的能量如下:
化学键断开吸收或生成时释放的能量如下: 436
436 ,
, 193
193 ,
, 946
946 。已知:
。已知: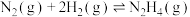
 ,则生成1
,则生成1
 释放的能量是
释放的能量是_______  。
。
(1)甘氨酸锌常用于食品的添加剂,也可代替甘油作烟丝的加香、防冻。一水合甘氨酸锌结构简式如图所示。

①在H、N、O、C、
 元素中,不属于P区元素的有:
元素中,不属于P区元素的有:②基态O原子最高能级的原子轨道形状是
(2)“中国制造2025”是中国政府实施制造强国战略第一个十年行动领。氮化铬在现代工业中发挥了重要的作用。
①基态N原子的价层电子的轨道表示式为
②基态
 原子的价层电子排布式为
原子的价层电子排布式为(3)
 在空气中存在如下反应:
在空气中存在如下反应: ,该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为:
,该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为:
(4)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(
 、
、 、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。发生以下反应:
、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。发生以下反应:Ⅰ.

II.

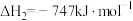
若
 的燃烧热为283.5
的燃烧热为283.5 ,则反应Ⅰ的
,则反应Ⅰ的

(5)已知1
 化学键断开吸收或生成时释放的能量如下:
化学键断开吸收或生成时释放的能量如下: 436
436 ,
, 193
193 ,
, 946
946 。已知:
。已知: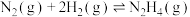
 ,则生成1
,则生成1
 释放的能量是
释放的能量是 。
。
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铜矿资源是金属矿产资源之一,我国具有丰富的铜矿资源,主要有斑岩型、硅卡岩型、砂岩型、火山岩型、铜镍型等。回答下列问题:
(1)焰火中的绿色是铜的焰色,基态铜原子在灼烧时价电子发生了_______ 而变为激发态。
(2)基态Cu原子的价电子排布式为_______ ,基态镍原子的价电子轨道表示式为_______ 。
(3)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。Zn的第一电离能_______ (填“大于”或“小于”)Cu的第一电离能﹐原因是_______ 。
(1)焰火中的绿色是铜的焰色,基态铜原子在灼烧时价电子发生了
(2)基态Cu原子的价电子排布式为
(3)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。Zn的第一电离能
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)Fe成为阳离子时首先失去___ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___ 。
(2)Cu2+基态核外电子排布式为___ 。
(3)Mn位于元素周期表中第四周期___ 族,基态Mn原子核外未成对电子有___ 个。
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___ 、__ (填标号)。
(2)Cu2+基态核外电子排布式为
(3)Mn位于元素周期表中第四周期
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
B.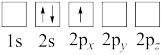
C.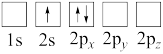
D.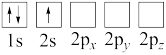
您最近半年使用:0次
【推荐2】向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
Ⅰ.在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
(1)写出H2O分子的电子式:________ 。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是________ 。
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
Ⅱ.胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、花卉上。
(3)写出铜原子价电子层的电子排布式:_____ ,与铜同一周期副族元素的基态原子中最外层电子数与铜原子相同的元素有________ (填元素符号)。
(4)实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有________ 。
(5)实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是_________________________ 。
Ⅰ.在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
(1)写出H2O分子的电子式:
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
Ⅱ.胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、花卉上。
(3)写出铜原子价电子层的电子排布式:
(4)实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有
(5)实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是
您最近半年使用:0次
【推荐3】地球上的元素大多数是金属,Na、Mg、Al是常见的主族金属元素,Fe和Cu是常见的过渡金属元素。它们在化学中占有极其重要的地位。
(1)①Na、Mg、Al三种元素第一电离能由大到小的顺序为___________
②金属钠原子的堆积方式是体心立方,其配位数为___________
(2)选修三课本第42页实验2-2:向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
①硫酸铜溶液中呈___________ 色的物质是水合铜离子,请写出它的结构简式,并标明其中配位键___________
②请写出难溶物溶解得到深蓝色的透明溶液的离子方程式___________
③结构测定的实验证明,无论在氨水溶液中还是在晶体中,深蓝色都是由于存在某种离子,1mol该离子含有___________ molσ键。
(3)写出少量Na2O2与氯化铁溶液反应的离子反应方程式:___________ (要求:仅写1个总的离子方程式)
(1)①Na、Mg、Al三种元素第一电离能由大到小的顺序为
②金属钠原子的堆积方式是体心立方,其配位数为
(2)选修三课本第42页实验2-2:向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
①硫酸铜溶液中呈
②请写出难溶物溶解得到深蓝色的透明溶液的离子方程式
③结构测定的实验证明,无论在氨水溶液中还是在晶体中,深蓝色都是由于存在某种离子,1mol该离子含有
(3)写出少量Na2O2与氯化铁溶液反应的离子反应方程式:
您最近半年使用:0次