回答下列问题:
(1)写出基态P原子的价电子排布式:_____ 。基态Fe2+与Fe3+化学性质相对稳定的是____ (填离子符号),解释原因:____ 。
(2)浓磷酸在常温下呈黏稠状,原因是____ ,浓磷酸在200~300℃时脱水生成焦磷酸(化学式:H4P2O7),焦磷酸的结构简式为____ ,其中P的价电子对数为____ ,杂化轨道类型为____ 。
(1)写出基态P原子的价电子排布式:
(2)浓磷酸在常温下呈黏稠状,原因是
21-22高二·全国·单元测试 查看更多[1]
更新时间:2022-08-25 14:39:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】《上海市排水“十四五”规划》提出到“十四五”末期,新增污水处理规模约280万立方米/日。聚合氯化铝(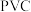 )是一种高效絮凝剂,广泛用于城市给排水净化。工业上制备
)是一种高效絮凝剂,广泛用于城市给排水净化。工业上制备 的一种方法:
的一种方法: 。
。
(1)上述反应所涉及的第二周期元素中,未成对电子数相等的元素有___________ ,能说明两者非金属性强弱的事实是___________ 。
(2)常压、180℃时, 升华形成的二聚体(
升华形成的二聚体( )的结构如图所示,试用“→”标出其中的配位键
)的结构如图所示,试用“→”标出其中的配位键___________ ,其杂化方式为___________ 。

(3)美国科学家宣布发现了铝的某种超原子结构( )具有40个价电子时处于相对稳定状态。请预测稳定的
)具有40个价电子时处于相对稳定状态。请预测稳定的 所带的电荷数为__________。
所带的电荷数为__________。
(4)铝的“超级原子”结构有 、
、 等。这类超级原子和
等。这类超级原子和 类似,最外层电子数为40时处于相对稳定状态,下列说法正确的是__________。
类似,最外层电子数为40时处于相对稳定状态,下列说法正确的是__________。
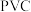 )是一种高效絮凝剂,广泛用于城市给排水净化。工业上制备
)是一种高效絮凝剂,广泛用于城市给排水净化。工业上制备 的一种方法:
的一种方法: 。
。(1)上述反应所涉及的第二周期元素中,未成对电子数相等的元素有
(2)常压、180℃时,
 升华形成的二聚体(
升华形成的二聚体( )的结构如图所示,试用“→”标出其中的配位键
)的结构如图所示,试用“→”标出其中的配位键
(3)美国科学家宣布发现了铝的某种超原子结构(
 )具有40个价电子时处于相对稳定状态。请预测稳定的
)具有40个价电子时处于相对稳定状态。请预测稳定的 所带的电荷数为__________。
所带的电荷数为__________。| A.-1 | B.+2 | C.0 | D.+3 |
(4)铝的“超级原子”结构有
 、
、 等。这类超级原子和
等。这类超级原子和 类似,最外层电子数为40时处于相对稳定状态,下列说法正确的是__________。
类似,最外层电子数为40时处于相对稳定状态,下列说法正确的是__________。A. 与盐酸反应的化学方程式可表示为: 与盐酸反应的化学方程式可表示为: |
B. 和 和 互为同位素 互为同位素 |
C. 和 和 都具有较强的还原性,容易失去电子生成阳离子 都具有较强的还原性,容易失去电子生成阳离子 |
D. 超原子中 超原子中 原子间通过离子键结合 原子间通过离子键结合 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、钴、硼、镓、硒等。已知铜的配合物A结构如图。请回答下列问题:

(1)基态二价铜离子的电子排布式为_________ ,已知高温下Cu2O比CuO更稳定,试从核外电子排布角度解释_________ 。
(2)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和π键数目之比是_________ ;N2O与CO2互为等电子体,则N2O的电子式为_________ 。
(3)铜与(SCN)2反应生成Cu(SCN)2,1mol(SCN)2中含有π键的数目为_________ (用NA表示),HSCN结构有两种,硫氰酸(H—S—C≡N)的沸点低于异硫氰酸(H—N=C=S)的原因是_________ 。
(4)六方氮化硼晶体结构与石墨晶体相似,层间相互作用力为_________ 。六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构、硬度与金刚石相似,其晶胞如图,晶胞边长为361.5pm,立方氮化硼的密度是_________ g·cm-3(只列算式,NA为阿伏加德罗常数的值)。

(5)关于两种晶体的说法正确的是_________ (填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体

(1)基态二价铜离子的电子排布式为
(2)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和π键数目之比是
(3)铜与(SCN)2反应生成Cu(SCN)2,1mol(SCN)2中含有π键的数目为
(4)六方氮化硼晶体结构与石墨晶体相似,层间相互作用力为

(5)关于两种晶体的说法正确的是
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据已学知识,回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是____ ,占据该能层电子的电子云轮廓图形状为____ 。
(2)写出3p轨道上有2个未成对电子的元素的符号____ 或____ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是____ 。
(4)已知铁是26号元素,写出Fe的价层电子排布式____ ;在元素周期表中,该元素在____ (填“s”“p”“d”“f”或“ds”)区。
(5)写出与N同主族的As的基态原子的核外电子排布式____ 。
(6)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为____ 。
(7)写出Fe2+的核外电子排布式:____ 。
(8)Zn2+的核外电子排布式为____ 。
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出Fe的价层电子排布式
(5)写出与N同主族的As的基态原子的核外电子排布式
(6)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(7)写出Fe2+的核外电子排布式:
(8)Zn2+的核外电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】填空。
(1) 中的化学键从形成过程来看,属于
中的化学键从形成过程来看,属于___________ (填“σ”或“π”)键。
(2) 和
和 分子中C原子的杂化方式分别为
分子中C原子的杂化方式分别为___________ 和___________ 。
(3) 分子的结构式为
分子的结构式为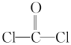 ,每个
,每个 分子内含有的σ键、π键数目分别为___________。
分子内含有的σ键、π键数目分别为___________。
(4)有两种活性反应中间体粒子,它们的粒子中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:
甲: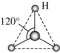
___________ ,乙:
___________ 。
(1)
 中的化学键从形成过程来看,属于
中的化学键从形成过程来看,属于(2)
 和
和 分子中C原子的杂化方式分别为
分子中C原子的杂化方式分别为(3)
 分子的结构式为
分子的结构式为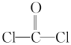 ,每个
,每个 分子内含有的σ键、π键数目分别为___________。
分子内含有的σ键、π键数目分别为___________。| A.4个σ键 | B.2个σ键、2个π键 |
| C.2个σ键、1个π键 | D.3个σ键、1个π键 |
甲:


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】第ⅢA、ⅤA原元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似.Ga原子的电子排布式为________ .在GaN晶体中,每个Ga原子与________ 个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为________ .在四大晶体类型中,GaN属于______ 晶体.
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】储氢材料的研究和应用是科学家努力攻克的课题。钛锰合金即是一种金属氢化物储氢材料。
(1)锰原子在基态时,核外电子排布式为______________________ ;
(2)一种钛的氧化物晶胞结构如图,则该化合物的化学式为___________ ;

(3)钙钛矿(CaTiO3)是典型的立方晶胞:Ca2+处于立方晶胞中心,Ti3+处于立方晶胞顶点,由于O2-处于立方晶胞的______ 形成两种不同的结构。相应的两种结构中每个Ti3+分别与______ 或_____ 个O2-配位。
(4)科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:
NaHCO3+H2 HCOONa+H2O
HCOONa+H2O
1 mol NaHCO3中含有δ键的数目为________ ;
HCOONa中碳原子轨道的杂化类型是________ 。
(1)锰原子在基态时,核外电子排布式为
(2)一种钛的氧化物晶胞结构如图,则该化合物的化学式为

(3)钙钛矿(CaTiO3)是典型的立方晶胞:Ca2+处于立方晶胞中心,Ti3+处于立方晶胞顶点,由于O2-处于立方晶胞的
(4)科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:
NaHCO3+H2
 HCOONa+H2O
HCOONa+H2O1 mol NaHCO3中含有δ键的数目为
HCOONa中碳原子轨道的杂化类型是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】N元素有多种化合物,它们之间可以发生转化,如:N2H4+HNO2=2H2O+HN3。请回答下列问题:
(1)N与C第一电离能较大的是________ 。
(2)NaN3的晶体类型是________ 。
(3)N的基态原子的电子排布中,有________ 个运动状态不同的未成对电子。
(4)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8 K,主要原因是____________ 。
(5)HNO2中的N原子的杂化类型是________ 。
(6)NO2-离子是一种很好的配位体,能提供孤电子对的是________ 。
A.氧原子 B.氮原子 C.两者都可以
NO2-与钴盐通过配位键形成的[Co(NO2)6]3-能与K+离子结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+离子,写出该配合物中钴离子的电子排布式:______________ 。
(7)N2H4分子中________ (填“含”或“不含”)π键。
(1)N与C第一电离能较大的是
(2)NaN3的晶体类型是
(3)N的基态原子的电子排布中,有
(4)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8 K,主要原因是
(5)HNO2中的N原子的杂化类型是
(6)NO2-离子是一种很好的配位体,能提供孤电子对的是
A.氧原子 B.氮原子 C.两者都可以
NO2-与钴盐通过配位键形成的[Co(NO2)6]3-能与K+离子结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+离子,写出该配合物中钴离子的电子排布式:
(7)N2H4分子中
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知A、B、C、D四种分子所含原子的数目依次为1、3、6、2,且都含有18个电子,B、C是由两种元素的原子组成,且分子中两种原子的个数比均为1∶2。D物质的氢化物能刻蚀玻璃。
(1)A的分子式是________ ,写出A原子的价层电子排布式________ 。
(2)B分子的中心原子的杂化类型是________ ,分子空间构型是________ ,该分子属于________ 分子(填“极性”或“非极性”)。
(3)C的化学式是________ ,分子中含有的化学键类型是________ 。
(4)D物质的氢化物的沸点比HCl的沸点高,其主要原因是___________________ 。
(1)A的分子式是
(2)B分子的中心原子的杂化类型是
(3)C的化学式是
(4)D物质的氢化物的沸点比HCl的沸点高,其主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】绿芦笋中含有天门冬氨酸(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。回答下列问题:___________ ,其中N原子的杂化轨道类型为___________ ,图中O—C—C的键角___________ C—C—N的键角(填“大于”或“小于”)。
(2) 和
和 热稳定性较好的是
热稳定性较好的是___________ ,从分子结构角度解释其原因:___________ 。
(3)分子结构修饰在药物设计与合成中有广泛的应用。若将天门冬氨酸中的 ,换成
,换成 ,得到的新物质的酸性会增强,原因是
,得到的新物质的酸性会增强,原因是___________ 。
(4)四个主族元素部分简单氢化物沸点随周期序数的变化如图所示。其中表示第VIIA族元素简单氢化物沸点变化的是曲线___________ (填字母),O—H…O的键能小于F—H…F,但水的沸点高于HF的原因可能是___________ 。

(2)
 和
和 热稳定性较好的是
热稳定性较好的是(3)分子结构修饰在药物设计与合成中有广泛的应用。若将天门冬氨酸中的
 ,换成
,换成 ,得到的新物质的酸性会增强,原因是
,得到的新物质的酸性会增强,原因是(4)四个主族元素部分简单氢化物沸点随周期序数的变化如图所示。其中表示第VIIA族元素简单氢化物沸点变化的是曲线

您最近一年使用:0次



