B、N、Ti、Fe都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)基态Fe2+的电子排布式为_____ ;Ti原子核外共有________ 种运动状态不同的电子。
(2)BH3分子与NH3分子的空间结构分别为_________ ;BH3与NH3反应生成的BH3·NH3分子中含有的化学键类型有_______ ,在BH3·NH3中B原子的杂化方式为________ 。
(3)N和P同主族。科学家目前合成了N4分子,该分子中N—N—N键的键角为________ ;N4分解后能产生N2并释放出大量能量,推测其用途___________ 。(写出一种即可)
(4)NH3与Cu2+可形成[Cu(NH3)4]2+配离子。已知NF3与NH3具有相同的空间构型,但NF3不易与Cu2+形成配离子,其原因是____ 。
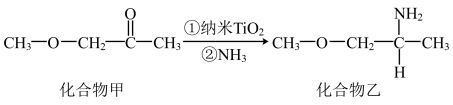
(5)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如图所示。化合物乙的沸点明显高于化合物甲,主要原因是______ 。化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为________ 。
(1)基态Fe2+的电子排布式为
(2)BH3分子与NH3分子的空间结构分别为
(3)N和P同主族。科学家目前合成了N4分子,该分子中N—N—N键的键角为
(4)NH3与Cu2+可形成[Cu(NH3)4]2+配离子。已知NF3与NH3具有相同的空间构型,但NF3不易与Cu2+形成配离子,其原因是
(5)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如图所示。化合物乙的沸点明显高于化合物甲,主要原因是

更新时间:2019-07-22 16:42:32
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)写出基态Р原子价电子排布式___ 。基态Fe2+与Fe3+离子化学性质相对稳定的是___ (填离子符号),解释原因___ 。
(2)浓磷酸在常温下呈粘稠状,原因___ ,浓磷酸在200~300℃时脱水生成焦磷酸(化学式:H4P2O7),焦磷酸的结构式为___ ,其中Р的价层电子对数为___ ,杂化轨道类型为___ 。
(3)LiFePO4的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。图(a)晶胞参数单位为pm,NA表示阿伏加德罗常数数值,其密度为___ g·cm-3。

电池充电时,LiFePO4脱出部分Li+,形成Li1-xFePO4,结构示意图如(b)所示,则x=___ ,n(Fe2+):n(Fe3+)=___ 。
(1)写出基态Р原子价电子排布式
(2)浓磷酸在常温下呈粘稠状,原因
(3)LiFePO4的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。图(a)晶胞参数单位为pm,NA表示阿伏加德罗常数数值,其密度为

电池充电时,LiFePO4脱出部分Li+,形成Li1-xFePO4,结构示意图如(b)所示,则x=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】依据物质结构知识,回答下列问题。
I.硒是一种非金属,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为___________ 。
(2)根据价层电子对互斥理论,可以推知 的空间构型为
的空间构型为___________ ,其中Se原子采用的轨道杂化方式为___________ 。
(3)已知 与
与 结构相似,①
结构相似,① 分子内的键角
分子内的键角 、②
、② 分子内的键角
分子内的键角 、③
、③ 分子内的键角
分子内的键角 ,三种键角由大到小的顺序为
,三种键角由大到小的顺序为___________ (填序号)。
Ⅱ.碳是一种重要元素,可形成多种单质及化合物。
(4) 分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则一个
分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则一个 分子中
分子中 键的数目为
键的数目为___________ ,含五边形数目是___________ 。
(5)已知 与
与 结构相似,推算HCN分子中
结构相似,推算HCN分子中 键与
键与 键数目之比为
键数目之比为___________ 。氨基氰( )为原料可制得类石墨相氮化碳(
)为原料可制得类石墨相氮化碳( ),氨基氰(
),氨基氰( )分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为
)分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为___________ 。
(6)铁触媒是以铁为主体的多成分催化剂,还含有MgO、Cr2O3等氧化物。Cr原子的价电子排布图为___________ ,处于元素周期表中___________ 区。
I.硒是一种非金属,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为
(2)根据价层电子对互斥理论,可以推知
 的空间构型为
的空间构型为(3)已知
 与
与 结构相似,①
结构相似,① 分子内的键角
分子内的键角 、②
、② 分子内的键角
分子内的键角 、③
、③ 分子内的键角
分子内的键角 ,三种键角由大到小的顺序为
,三种键角由大到小的顺序为Ⅱ.碳是一种重要元素,可形成多种单质及化合物。
(4)
 分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则一个
分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则一个 分子中
分子中 键的数目为
键的数目为(5)已知
 与
与 结构相似,推算HCN分子中
结构相似,推算HCN分子中 键与
键与 键数目之比为
键数目之比为 )为原料可制得类石墨相氮化碳(
)为原料可制得类石墨相氮化碳( ),氨基氰(
),氨基氰( )分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为
)分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为(6)铁触媒是以铁为主体的多成分催化剂,还含有MgO、Cr2O3等氧化物。Cr原子的价电子排布图为
您最近一年使用:0次
【推荐3】金属钛被誉为“未来金属”,钛及其化合物被广泛应用于飞机、火箭、卫星、舰艇、医疗等领域。
(1)钛位于周期表的___________ 区,基态钛原子价电子排布式为___________ 。
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。请写出一个与BH 互为等电子体的微粒
互为等电子体的微粒___________ (化学式)。
(3)钛的某配合物可用于催化环烯烃聚合,其结构如图所示。

①该配合物中碳原子的杂化类型为___________ ;
②该配合物中存在的化学键有___________ (填标号)。
a.共价键 b.金属键 c.配位键 d.氢键
(4)钛与卤素形成的化合物TiF4、TiCl4、TiBr4、TiI4熔点依次为377℃、-24℃、38.3℃、153℃,其中TiCl4、TiBr4、TiI4熔点依次升高的原因是___________ 。
(5)CaTiO3的晶胞如图所示,Ti4+的配位数为___________ ,若Ca2+位于晶胞顶点,则O2-位于晶胞___________ 位置,若晶胞参数为anm,则晶体密度为___________ g·cm-3(列出计算式,阿伏加德罗常数用NA表示)。

(1)钛位于周期表的
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。请写出一个与BH
 互为等电子体的微粒
互为等电子体的微粒(3)钛的某配合物可用于催化环烯烃聚合,其结构如图所示。

①该配合物中碳原子的杂化类型为
②该配合物中存在的化学键有
a.共价键 b.金属键 c.配位键 d.氢键
(4)钛与卤素形成的化合物TiF4、TiCl4、TiBr4、TiI4熔点依次为377℃、-24℃、38.3℃、153℃,其中TiCl4、TiBr4、TiI4熔点依次升高的原因是
(5)CaTiO3的晶胞如图所示,Ti4+的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】碳元素形成的单质和化合物在化工、材料、医学等领域应用广泛,回答下列问题:
(1)区分金刚石和无定形碳最可靠的科学方法为___________ 。基态C原子核外未成对电子的数目为_____________ 。
(2)咖啡因结构为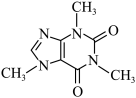 。
。
①咖啡因中C原子的杂化形式为_________________ 。
②1 mol咖啡因中所含 键数目为
键数目为_________________ 。
③咖啡因通常在水中的溶解度较小,加入适量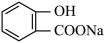 能增大其在水中溶解度的原因为
能增大其在水中溶解度的原因为_________________ 。
④CH3+(甲基正离子)的立体构型为_________________ 。
(3)CO、NO、H2S均为生命体系气体信号分子。其中H、C、O、S的电负性由大到小的顺序为____________ ;N、O、S的第一电离能由大到小的顺序为________________ 。
(4)干冰可用于人工降雨。其熔点低于金刚石的原因为___________ ;若干冰的密度为1.56 g/cm3,立方晶胞参数为0.57 nm,则每个晶胞实际占用CO2的数目为_______ 。
(1)区分金刚石和无定形碳最可靠的科学方法为
(2)咖啡因结构为
 。
。①咖啡因中C原子的杂化形式为
②1 mol咖啡因中所含
 键数目为
键数目为③咖啡因通常在水中的溶解度较小,加入适量
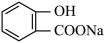 能增大其在水中溶解度的原因为
能增大其在水中溶解度的原因为④CH3+(甲基正离子)的立体构型为
(3)CO、NO、H2S均为生命体系气体信号分子。其中H、C、O、S的电负性由大到小的顺序为
(4)干冰可用于人工降雨。其熔点低于金刚石的原因为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E五种10电子微粒所含原子数目依次为2、5、3、4、4,E能使湿润的红色石蕊试纸变蓝,它们的转化关系如图。

回答下列问题:
(1)A的电子式为_______ 。B的空间构型为_______ 。
(2)C的中心原子的杂化方式为_______ ,与C互为等电子体的阴离子是_______ (填化学式)。
(3)D的键角比C的键角大,可能的原因是_______ 。
(4)上述五种微粒中存在配位键的是_______ (填微粒符号)。

回答下列问题:
(1)A的电子式为
(2)C的中心原子的杂化方式为
(3)D的键角比C的键角大,可能的原因是
(4)上述五种微粒中存在配位键的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】近日,南开大学化学院先进能源材料实验室发布:在缬氨酸做表面配体时制备出了一种可广泛用于电学和光学领域的新型钙钛矿型材料(CsPbBr3),该研究成果大大推进了材料化学的发展。
回答下列问题:
(1)基态Ti原子的外围电子排布式为__ ,基态Ti原子核外电子的空间运动状态有__ 种。
(2)标准大气压下,液态溴获得能量后,能发生如图所示的变化。
Br2(l)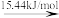 Br2(g)
Br2(g)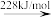 2Br(g)
2Br(g)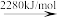 2Br+(g)
2Br+(g)
Br—Br键的键能为___ kJ/mol,Br的第一电离能为__ kJ/mol。
(3)缬氨酸的结构简式为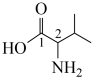 ,其中碳原子的杂化方式为
,其中碳原子的杂化方式为__ ,键角1__ 键角2(填“>”“<”或“=”)。
(4)金属钙的熔点为850℃,金属钛的熔点为1720℃,金属钛的熔点更高的原因为__ 。
(5)CsPbBr3晶胞结构如图a所示,Cs+沿晶胞体对角线的投影图如图b所示。

①Pb2+的配位数为__ ,若A原子的坐标参数为(0,0,0),B原子的坐标参数为(0,0, ),则C原子的坐标参数为
),则C原子的坐标参数为__ 。
②请在图b中画出图a晶胞中所有Br-的投影位置___ 。
③若晶胞参数为apm,NA为阿伏加德罗常数的值,则CsPbBr3晶体的密度为__ g•cm-3(用含a、NA的代数式表示,列出计算式即可)。
回答下列问题:
(1)基态Ti原子的外围电子排布式为
(2)标准大气压下,液态溴获得能量后,能发生如图所示的变化。
Br2(l)
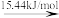 Br2(g)
Br2(g)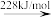 2Br(g)
2Br(g)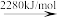 2Br+(g)
2Br+(g)Br—Br键的键能为
(3)缬氨酸的结构简式为
 ,其中碳原子的杂化方式为
,其中碳原子的杂化方式为(4)金属钙的熔点为850℃,金属钛的熔点为1720℃,金属钛的熔点更高的原因为
(5)CsPbBr3晶胞结构如图a所示,Cs+沿晶胞体对角线的投影图如图b所示。

①Pb2+的配位数为
 ),则C原子的坐标参数为
),则C原子的坐标参数为②请在图b中画出图a晶胞中所有Br-的投影位置
③若晶胞参数为apm,NA为阿伏加德罗常数的值,则CsPbBr3晶体的密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表为元素周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区的元素是_______ (填元素名称),其形成的常见阳离子中化学性质较稳定的是_______ (填离子符号)。
(2)e基态原子中能量最高的电子,其电子云轮廓图的取向有_______ 个。
(3)离子化合物da5中的阳离子是NH ,猜测da5的电子式为
,猜测da5的电子式为_______ 。
(4)与k同周期的所有元素的基态原子中未成对电子数最多的是_______ (填元素符号),写出该元素的基态原子的价电子排布式:_______ 。
(5)常温下,液态化合物geh2与水剧烈反应,产生能使品红溶液褪色的ge2气体,向反应后的溶液中加入AgNO3溶液,有不溶于稀硝酸的白色沉淀析出。根据实验现象,写出geh2与水反应的化学方程式_______ 。
(6)碱性条件下,ca4燃料电池的负极反应式为:_______ 。
(7)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为_______ ,下列对XeF2中心原子杂化方式推断合理的是_______ (填标号)。
A.sp B.sp2 C.sp3 D.sp3d

请回答下列问题:
(1)表中属于d区的元素是
(2)e基态原子中能量最高的电子,其电子云轮廓图的取向有
(3)离子化合物da5中的阳离子是NH
 ,猜测da5的电子式为
,猜测da5的电子式为(4)与k同周期的所有元素的基态原子中未成对电子数最多的是
(5)常温下,液态化合物geh2与水剧烈反应,产生能使品红溶液褪色的ge2气体,向反应后的溶液中加入AgNO3溶液,有不溶于稀硝酸的白色沉淀析出。根据实验现象,写出geh2与水反应的化学方程式
(6)碱性条件下,ca4燃料电池的负极反应式为:
(7)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
A.sp B.sp2 C.sp3 D.sp3d
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氧族元素包括氧、硫、硒、碲、钋。
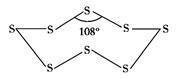
(1)单质硫的同素异形体很多,最常见的是斜方晶硫和单斜晶硫,经过测定,这两种硫的单质都是由S8构成的。S8分子的构型如图所示。S—S键的键角为108°,8个S原子形成两层,每层4个S原子。S8分子中S原子通过_______ 杂化与其他原子成键,斜方晶硫和单斜晶硫中S8分子之间靠_______ 结合在一起。
(2)氧及与其同周期的碳、氮、氟四种原子的第一电离能由大到小的顺序是_____ 。
(3)用元素原子电负性的理论判断,H2O中的O—H键的键角_______ (填“>”、“=”或“<”)H2S中的S—H键的键角。
(4)硒是人体生命活动不可缺少的微量元素,适量的硒能够增强人体免疫力,延缓衰老,清除人体内的有害物质。如图是硒(Se)化锶(Sr)的晶胞模型,据此可知,每个硒化锶晶胞中含有的硒离子为_______ 个,其化学式为_______ 。

(1)单质硫的同素异形体很多,最常见的是斜方晶硫和单斜晶硫,经过测定,这两种硫的单质都是由S8构成的。S8分子的构型如图所示。S—S键的键角为108°,8个S原子形成两层,每层4个S原子。S8分子中S原子通过

(2)氧及与其同周期的碳、氮、氟四种原子的第一电离能由大到小的顺序是
(3)用元素原子电负性的理论判断,H2O中的O—H键的键角
(4)硒是人体生命活动不可缺少的微量元素,适量的硒能够增强人体免疫力,延缓衰老,清除人体内的有害物质。如图是硒(Se)化锶(Sr)的晶胞模型,据此可知,每个硒化锶晶胞中含有的硒离子为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵((NH4)3Fe(C6H5O7)2)。
(1)Fe 基态原子核外电子排布式为_____________ ;[ Fe(H2O)6]2+中与Fe2+配位的原子是_____ 。
(2)NH3分子中氮原子的轨道杂化类型是_______ ;与 NH 互为等电子体的一种分子为
互为等电子体的一种分子为_____ (填化学式)。
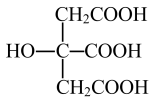
(3)柠檬酸的结构简式见图。1 mol 柠檬酸分子中碳原子与氧原子形成的σ键的数目为_______ mol。
(4)CaCN2是离子化合物,各原子均满足 8 电子稳定结构,CaCN2的电子式是_____ 。
(1)Fe 基态原子核外电子排布式为
(2)NH3分子中氮原子的轨道杂化类型是
 互为等电子体的一种分子为
互为等电子体的一种分子为(3)柠檬酸的结构简式见图。1 mol 柠檬酸分子中碳原子与氧原子形成的σ键的数目为

(4)CaCN2是离子化合物,各原子均满足 8 电子稳定结构,CaCN2的电子式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】图A所示的转化关系中(具体反应条件已略去),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物。a元素原子的2p轨道只有2个未成对的电子,i的溶液为常见的酸。

回答下列问题:
(1)写出a+H2O→b+f的化学方程式为____ 。
(2)d中元素的价层电子轨道表达式为____ 。
(3)图A中由两种元素组成的物质中,沸点最高的是____ ,原因是____ ,该物质的分子构型为_____ 。
(4)图A的双原子分子中,极性最大的分子是____ 。
(5)f与d发生化合反应生成k,则k的分子式为____ ,中心原子的杂化轨道类型为___ ,属于____ 分子(填“极性”或“非极性”)。
(6)Cu与d形成化合物的晶胞如图B所示。该晶体的化学式为____ 。

回答下列问题:
(1)写出a+H2O→b+f的化学方程式为
(2)d中元素的价层电子轨道表达式为
(3)图A中由两种元素组成的物质中,沸点最高的是
(4)图A的双原子分子中,极性最大的分子是
(5)f与d发生化合反应生成k,则k的分子式为
(6)Cu与d形成化合物的晶胞如图B所示。该晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】磷酸氯喹在细胞水平上能有效抑制新型冠状病毒(SARS-CoV-2)的感染。磷酸氯喹的结构如图所示,据此回答下列问题。_____ 。
(2)C、N、O三种元素电负性从大到小的顺序为_____ ;第一电离能I1(P)_____ I1(Cl)(填“>”或“<”)。
(3)钴的一种化合物的晶胞结构如图所示,已知A点的原子坐标参数为(0,0,0),B点为( ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为_____ 。_____ (用化学式表示)。_____ 。

(2)C、N、O三种元素电负性从大到小的顺序为
(3)钴的一种化合物的晶胞结构如图所示,已知A点的原子坐标参数为(0,0,0),B点为(
 ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为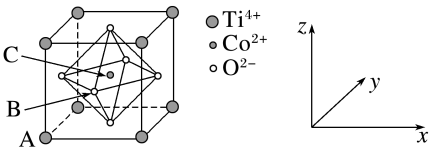

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】据文献报道:用作锂离子电池正极材料的磷酸亚铁锂(LiFePO4)可采用FeCl3、NH4H2PO4、LiCl和苯胺( )等作为原料制备。回答下列问题:
)等作为原料制备。回答下列问题:
(1)在元素周期表中,Li属于_______ 区元素,与Li的化学性质最相似的邻族元素是_______ ,该元素基态原子核外M层电子的自旋状态_______ (填“相同”或“相反”)。
(2)在NH4H2PO4中,电负性值最高的元素是_______ ;P原子的_______ 杂化轨道与O原子的2p轨道形成_______ 键。
(3)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为_______ 。
(4)苯胺的晶体类型是_______ ,苯胺与甲苯的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ 。
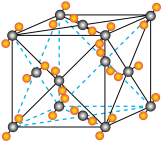
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,记为原子坐标。已知LiCl·3H2O属正交晶系(长方体形),晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的晶胞中所有Cl原子的分布图和原子坐标。据此可推断该晶胞中Cl原子的数目为_______ 。设LiCl·3H2O的摩尔质量为Mg·mol-1,NA为阿伏加德罗常数的值,则LiCl·3H2O晶体的密度为_______ g·cm-3(列出计算表达式,不必化简)。

 )等作为原料制备。回答下列问题:
)等作为原料制备。回答下列问题:(1)在元素周期表中,Li属于
(2)在NH4H2PO4中,电负性值最高的元素是
(3)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为
(4)苯胺的晶体类型是
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,记为原子坐标。已知LiCl·3H2O属正交晶系(长方体形),晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的晶胞中所有Cl原子的分布图和原子坐标。据此可推断该晶胞中Cl原子的数目为

您最近一年使用:0次



