以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸钠和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:

(1)反应I的化学方程式是__________ ,其中 的电子式
的电子式___________ 。
(2)若反应I得到的 ;浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是
;浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是________
(3)反应I需控制反应温度低于35℃,其目的是____________ 。
(4)反应I的反应类型为______________________ 。
(5)反应Ⅲ常被用于电解生产 (过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为
(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为_______ 。
(6)已知煅烧 的化学方程式是
的化学方程式是 ,现煅烧
,现煅烧 的
的 ,得到
,得到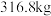 产品。若产品中仅仅有杂质
产品。若产品中仅仅有杂质 ,则该产品中
,则该产品中 的质量是
的质量是________ kg。

(1)反应I的化学方程式是
 的电子式
的电子式(2)若反应I得到的
 ;浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是
;浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是(3)反应I需控制反应温度低于35℃,其目的是
(4)反应I的反应类型为
(5)反应Ⅲ常被用于电解生产
 (过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为
(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为(6)已知煅烧
 的化学方程式是
的化学方程式是 ,现煅烧
,现煅烧 的
的 ,得到
,得到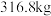 产品。若产品中仅仅有杂质
产品。若产品中仅仅有杂质 ,则该产品中
,则该产品中 的质量是
的质量是
更新时间:2019-06-10 20:32:54
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】连二硫酸锰( )常用于灭菌以及水果、蔬菜的保鲜,利用
)常用于灭菌以及水果、蔬菜的保鲜,利用 悬浊液吸收
悬浊液吸收 气体制取连二硫酸锰的装置(部分夹持、控温仪器已省略)如图所示:
气体制取连二硫酸锰的装置(部分夹持、控温仪器已省略)如图所示:
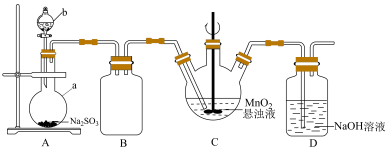
已知:
i. 易溶于水,其在
易溶于水,其在 为2.8~3.5时最稳定,温度超过
为2.8~3.5时最稳定,温度超过 时会快速分解生成易溶于水的
时会快速分解生成易溶于水的 ;
;
ii.连二硫酸的结构式: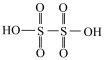 。
。
(1) 中
中 的化合价为
的化合价为___________ 。
(2)仪器a的名称是___________ ,仪器b装入的药品是___________ (填标号)。
A.浓盐酸 B.浓硝酸 C.稀硝酸 D.70%硫酸溶液
(3)装置B的作用为___________ 。
(4)装置C中的反应温度需要控制在左右,实验时需通入稍过量的 ,目的是
,目的是___________ ;表明C中反应已完成的现象是___________ 。
(5)测定产品中 元素的质量分数:称取
元素的质量分数:称取 产品充分加热使其分解为
产品充分加热使其分解为 ,然后加水溶解,用
,然后加水溶解,用 的酸性
的酸性 溶液进行滴定(
溶液进行滴定( 元素均转化为
元素均转化为 )。若多次滴定平均消耗
)。若多次滴定平均消耗 溶液的体积为
溶液的体积为 ,则产品中
,则产品中 元素的质量分数为
元素的质量分数为___________ (用含 、
、 、
、 的代数式表示)。滴定过程中发生反应的离子方程式为
的代数式表示)。滴定过程中发生反应的离子方程式为___________ 。
 )常用于灭菌以及水果、蔬菜的保鲜,利用
)常用于灭菌以及水果、蔬菜的保鲜,利用 悬浊液吸收
悬浊液吸收 气体制取连二硫酸锰的装置(部分夹持、控温仪器已省略)如图所示:
气体制取连二硫酸锰的装置(部分夹持、控温仪器已省略)如图所示:
已知:
i.
 易溶于水,其在
易溶于水,其在 为2.8~3.5时最稳定,温度超过
为2.8~3.5时最稳定,温度超过 时会快速分解生成易溶于水的
时会快速分解生成易溶于水的 ;
;ii.连二硫酸的结构式:
 。
。(1)
 中
中 的化合价为
的化合价为(2)仪器a的名称是
A.浓盐酸 B.浓硝酸 C.稀硝酸 D.70%硫酸溶液
(3)装置B的作用为
(4)装置C中的反应温度需要控制在左右,实验时需通入稍过量的
 ,目的是
,目的是(5)测定产品中
 元素的质量分数:称取
元素的质量分数:称取 产品充分加热使其分解为
产品充分加热使其分解为 ,然后加水溶解,用
,然后加水溶解,用 的酸性
的酸性 溶液进行滴定(
溶液进行滴定( 元素均转化为
元素均转化为 )。若多次滴定平均消耗
)。若多次滴定平均消耗 溶液的体积为
溶液的体积为 ,则产品中
,则产品中 元素的质量分数为
元素的质量分数为 、
、 、
、 的代数式表示)。滴定过程中发生反应的离子方程式为
的代数式表示)。滴定过程中发生反应的离子方程式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化氯(ClO2)是一种高效消毒剂,易溶于水,沸点为11.0°C,浓度高时极易爆炸。某研究小组在实验室按如图所示的装置,用干燥的氯气与固体亚氯酸钠制备二氧化氯,请回答下列问题:

(1)B装置使用的试液X为___________ ,其作用是___________ 。
(2)装置E的作用是___________ 。
(3)装置D中冰水的主要作用是___________ ,往D中通入氯气的同时还通入干燥的空气,其主要目的是___________ 。
(4)装置D内发生反应的化学方程式为___________ 。
(5)工业上可在酸性条件下用双氧水与NaClO3反应制备ClO2,该反应的离子方程式为___________ 。

(1)B装置使用的试液X为
(2)装置E的作用是
(3)装置D中冰水的主要作用是
(4)装置D内发生反应的化学方程式为
(5)工业上可在酸性条件下用双氧水与NaClO3反应制备ClO2,该反应的离子方程式为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】某炼锌厂利用含ZnO的烟尘脱除硫酸工艺烟气中的SO2制ZnSO4。
已知:Ⅰ.ZnSO3· H2O微溶于水,ZnSO4易溶于水。
H2O微溶于水,ZnSO4易溶于水。
Ⅱ.25℃时,溶液中S(+4价)各组分的物质的量分数随pH变化曲线如下图。

Ⅲ.O3为强氧化剂,1 mol O3被还原转移2 mol e−,同时生成1 mol O2。
(1)SO2造成的环境问题主要是_____________________ 。
(2)ZnO将SO2转化为ZnSO3· H2O的化学方程式是
H2O的化学方程式是_____________________________ 。
(3)将ZnSO3· H2O悬浊液转化为ZnSO4时,因其被O2氧化的速率很慢,易造成管道堵塞,实验室模拟O3氧化解决该问题。初始时用盐酸将5% ZnSO3悬浊液调至 pH=3.5,以一定的进气流量通入O3,研究O3氧化ZnSO3·
H2O悬浊液转化为ZnSO4时,因其被O2氧化的速率很慢,易造成管道堵塞,实验室模拟O3氧化解决该问题。初始时用盐酸将5% ZnSO3悬浊液调至 pH=3.5,以一定的进气流量通入O3,研究O3氧化ZnSO3· H2O,其中溶液pH随时间变化的曲线如下:
H2O,其中溶液pH随时间变化的曲线如下:
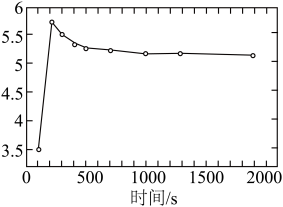
①pH=3.5的溶液中含S(+4价)的离子主要是____________________ 。
②一段时间后,溶液的pH减小,此过程中主要反应的离子方程式是________________ 。
③解释O3氧化可防止管道堵塞的原因:___________________ 。
已知:Ⅰ.ZnSO3·
 H2O微溶于水,ZnSO4易溶于水。
H2O微溶于水,ZnSO4易溶于水。Ⅱ.25℃时,溶液中S(+4价)各组分的物质的量分数随pH变化曲线如下图。

Ⅲ.O3为强氧化剂,1 mol O3被还原转移2 mol e−,同时生成1 mol O2。
(1)SO2造成的环境问题主要是
(2)ZnO将SO2转化为ZnSO3·
 H2O的化学方程式是
H2O的化学方程式是(3)将ZnSO3·
 H2O悬浊液转化为ZnSO4时,因其被O2氧化的速率很慢,易造成管道堵塞,实验室模拟O3氧化解决该问题。初始时用盐酸将5% ZnSO3悬浊液调至 pH=3.5,以一定的进气流量通入O3,研究O3氧化ZnSO3·
H2O悬浊液转化为ZnSO4时,因其被O2氧化的速率很慢,易造成管道堵塞,实验室模拟O3氧化解决该问题。初始时用盐酸将5% ZnSO3悬浊液调至 pH=3.5,以一定的进气流量通入O3,研究O3氧化ZnSO3· H2O,其中溶液pH随时间变化的曲线如下:
H2O,其中溶液pH随时间变化的曲线如下:
①pH=3.5的溶液中含S(+4价)的离子主要是
②一段时间后,溶液的pH减小,此过程中主要反应的离子方程式是
③解释O3氧化可防止管道堵塞的原因:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】纳米 被广泛应用于光催化、精细陶瓷等领域。
被广泛应用于光催化、精细陶瓷等领域。
(1)用 水解法制备纳米
水解法制备纳米 的工艺流程如图所示(成功的控制水解速率是制备纳米
的工艺流程如图所示(成功的控制水解速率是制备纳米 的前提):
的前提):
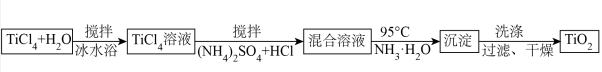
已知: 难溶于冷水,在热水中易水解;
难溶于冷水,在热水中易水解; 的水解按以下三步进行:
的水解按以下三步进行:
第Ⅰ步(水解):
第Ⅱ步(电离):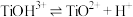
第Ⅲ步(水解):
①第Ⅰ步为快反应,对第Ⅱ、Ⅲ步反应的影响是_______ 。
②流程中加入硫酸铵的目的是_______ 。
③若取上述流程中“混合溶液”加水稀释,会产生少量偏钛酸( )沉淀,该反应的离子方程式为
)沉淀,该反应的离子方程式为_______ 。
(2)测定产品中 纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含
纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含 溶液。加入金属铝,将
溶液。加入金属铝,将 全部转化为
全部转化为 。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
 标准溶液滴定至终点,将
标准溶液滴定至终点,将 氧化为
氧化为 。重复操作2~3次,消耗标准溶液平均体积为20.00mL。
。重复操作2~3次,消耗标准溶液平均体积为20.00mL。
①金属铝还原 的离子方程式为
的离子方程式为_______ 。
②滴定时所用的指示剂为_______ (填编号)。
a.酚酞溶液 b.KSCN溶液 c. 溶液 d.淀粉溶液
溶液 d.淀粉溶液
③样品中 的纯度为
的纯度为_______ 。
(3)纳米 在室温下可有效催化降解空气中的甲醛。
在室温下可有效催化降解空气中的甲醛。 和甲醛都可在催化剂表面吸附,光照时,吸附的
和甲醛都可在催化剂表面吸附,光照时,吸附的 与
与 产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:
产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:_______ 。

 被广泛应用于光催化、精细陶瓷等领域。
被广泛应用于光催化、精细陶瓷等领域。(1)用
 水解法制备纳米
水解法制备纳米 的工艺流程如图所示(成功的控制水解速率是制备纳米
的工艺流程如图所示(成功的控制水解速率是制备纳米 的前提):
的前提):
已知:
 难溶于冷水,在热水中易水解;
难溶于冷水,在热水中易水解; 的水解按以下三步进行:
的水解按以下三步进行:第Ⅰ步(水解):

第Ⅱ步(电离):
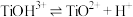
第Ⅲ步(水解):

①第Ⅰ步为快反应,对第Ⅱ、Ⅲ步反应的影响是
②流程中加入硫酸铵的目的是
③若取上述流程中“混合溶液”加水稀释,会产生少量偏钛酸(
 )沉淀,该反应的离子方程式为
)沉淀,该反应的离子方程式为(2)测定产品中
 纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含
纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含 溶液。加入金属铝,将
溶液。加入金属铝,将 全部转化为
全部转化为 。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
 标准溶液滴定至终点,将
标准溶液滴定至终点,将 氧化为
氧化为 。重复操作2~3次,消耗标准溶液平均体积为20.00mL。
。重复操作2~3次,消耗标准溶液平均体积为20.00mL。①金属铝还原
 的离子方程式为
的离子方程式为②滴定时所用的指示剂为
a.酚酞溶液 b.KSCN溶液 c.
 溶液 d.淀粉溶液
溶液 d.淀粉溶液③样品中
 的纯度为
的纯度为(3)纳米
 在室温下可有效催化降解空气中的甲醛。
在室温下可有效催化降解空气中的甲醛。 和甲醛都可在催化剂表面吸附,光照时,吸附的
和甲醛都可在催化剂表面吸附,光照时,吸附的 与
与 产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:
产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如图所示:

(1)“回收S”过程中温度控制在50~60 ℃之间,不宜过高或过低的原因是_______ 。
(2)“保温除铁”过程中,加入CuO的目的是_______ ;“蒸发浓缩、冷却结晶”过程中,要用HNO3溶液调节溶液的pH,其理由是_______ 。

(1)“回收S”过程中温度控制在50~60 ℃之间,不宜过高或过低的原因是
(2)“保温除铁”过程中,加入CuO的目的是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】草酸亚铁( )常用作照相显影剂,新型电池材料等。
)常用作照相显影剂,新型电池材料等。
(1)以 溶液制备草酸亚铁晶体的实验流程如下:
溶液制备草酸亚铁晶体的实验流程如下:

①配制 溶液时往往加入少量铁粉的原因是
溶液时往往加入少量铁粉的原因是___________ 。
②“转化”步骤的化学方程式为___________ 。
③若该流程中需要使用480mL 0.2000 的草酸溶液,则需要称取
的草酸溶液,则需要称取___________ g草酸晶体( ;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及
;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及___________ ,若定容时俯视刻度线,则所配溶液中
___________ 0.2000 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)用草酸亚钦晶体在700℃下焙烧反应制备纳米零价铁,反应的化学方程式:
 。当生成1mol Fe时,转移电子的物质的量为
。当生成1mol Fe时,转移电子的物质的量为___________ 。
(3)写出草酸亚铁溶于足量稀硫酸的离子方程式___________ 。
(4)已知: (M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是
(M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是___________ (填化学式)。

 )常用作照相显影剂,新型电池材料等。
)常用作照相显影剂,新型电池材料等。(1)以
 溶液制备草酸亚铁晶体的实验流程如下:
溶液制备草酸亚铁晶体的实验流程如下:
①配制
 溶液时往往加入少量铁粉的原因是
溶液时往往加入少量铁粉的原因是②“转化”步骤的化学方程式为
③若该流程中需要使用480mL 0.2000
 的草酸溶液,则需要称取
的草酸溶液,则需要称取 ;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及
;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)用草酸亚钦晶体在700℃下焙烧反应制备纳米零价铁,反应的化学方程式:

 。当生成1mol Fe时,转移电子的物质的量为
。当生成1mol Fe时,转移电子的物质的量为(3)写出草酸亚铁溶于足量稀硫酸的离子方程式
(4)已知:
 (M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是
(M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】硼镁泥是一种工业废料,主要成分是MgO( 占40%,还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2 等杂质,以此为原料制取的硫酸镁,可用于印染、选纸、医药等工业。从硼镁泥中提取MgSO4·7H2O 的流程如下:
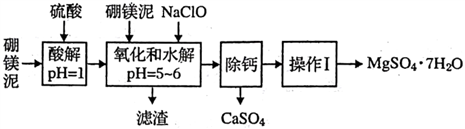
根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸800mL,若用18.4mol/L的浓硫酸来配制,量取浓硫酸时,需使用的量筒的规格为______ 。
A.10mL B.20mL C.50mL D.100mL
(2)加入的NaClO可与Mn2+反应:Mn2+ +ClO-+H2O=MnO2 ↓+2H++Cl-,还有一种离子也会被NaClO 氧化,该反应的离子方程式为____________________ 。
(3)滤渣中除含有Fe(OH)3、A(OH)3 外还有_________________ 。
(4)在“除钙”前,需检验滤波中Fe3+是否被除尽,简述检验方法:_________ 。
(5)已知MeSO4、CaSO4的溶解度如下表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4 除去,根据上表数据,简要说明操作步骤:_________ 。“操作I:是将滤液继续蒸发浓缩,冷却结晶,______ ,便得到了MgSO4·7H2O。
(6)实验中提供的硼镁泥共100g,得到的MgSO4·7H2O为172.2 g,则MgSO4·7H2O的产率为_____________________ 。

根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸800mL,若用18.4mol/L的浓硫酸来配制,量取浓硫酸时,需使用的量筒的规格为
A.10mL B.20mL C.50mL D.100mL
(2)加入的NaClO可与Mn2+反应:Mn2+ +ClO-+H2O=MnO2 ↓+2H++Cl-,还有一种离子也会被NaClO 氧化,该反应的离子方程式为
(3)滤渣中除含有Fe(OH)3、A(OH)3 外还有
(4)在“除钙”前,需检验滤波中Fe3+是否被除尽,简述检验方法:
(5)已知MeSO4、CaSO4的溶解度如下表:
| 温度/℃ | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4 除去,根据上表数据,简要说明操作步骤:
(6)实验中提供的硼镁泥共100g,得到的MgSO4·7H2O为172.2 g,则MgSO4·7H2O的产率为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某工厂的工业废水中含有大量的FeSO4和较多的Fe3+和Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁并探究硫酸亚铁的分解产物。
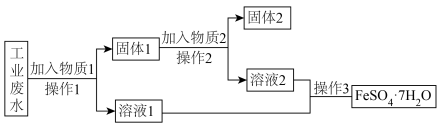
(1)检验废水中的Fe2+的方法是:取少量工业废水,向其中加入铁氰化钾溶液,将会产生现象为_______ ,发生反应的离子方程式为_______ 。
(2)物质1、物质2的化学式分别是_______ 。
(3)为探究硫酸亚铁的分解产物,将上述流程中获得的FeSO4·7H2O置于如图装置A中进行相关实验。
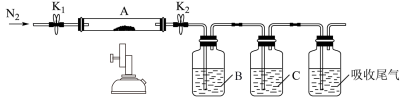
①先打开K1和K2,缓缓通入N2,再加热装置A,其目的是_______ ,实验后反应管中残留固体为红色粉末。
②B、C中的溶液依次为_______ (填标号)。
a.Ba (NO3)2 b.BaCl2 c.Ba(OH)2 d.KMnO4 e.NaOH
③写出FeSO4·7H2O高温分解反应的化学方程式:_______ 。

(1)检验废水中的Fe2+的方法是:取少量工业废水,向其中加入铁氰化钾溶液,将会产生现象为
(2)物质1、物质2的化学式分别是
(3)为探究硫酸亚铁的分解产物,将上述流程中获得的FeSO4·7H2O置于如图装置A中进行相关实验。

①先打开K1和K2,缓缓通入N2,再加热装置A,其目的是
②B、C中的溶液依次为
a.Ba (NO3)2 b.BaCl2 c.Ba(OH)2 d.KMnO4 e.NaOH
③写出FeSO4·7H2O高温分解反应的化学方程式:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】利用某钴矿石(主要成分为 )制取
)制取 粗品及其他工业产品的工艺流程如图甲所示。
粗品及其他工业产品的工艺流程如图甲所示。

已知:“浸出液”中含有的阳离子主要有 、
、 、
、 、
、 、
、 。
。
回答下列问题:
(1)钴矿石浸出时加入 的目的为
的目的为_______ 。
(2)溶液中 (X表示
(X表示 、
、 、
、 、
、 、
、 、
、 )与
)与 的变化关系如图乙所示(离子浓度小于
的变化关系如图乙所示(离子浓度小于 可认为已除尽)。在浸出液中通入空气的目的是
可认为已除尽)。在浸出液中通入空气的目的是_______ ,用熟石灰调 至3.2,过滤1所得滤渣的主要成分为
至3.2,过滤1所得滤渣的主要成分为_______ 。
(3)用氧化镁调滤液1的 为9.1时,得到的氢氧化钴粗品中含有的主要杂质为
为9.1时,得到的氢氧化钴粗品中含有的主要杂质为_______ ,多次洗涤可提高粗产品中钴含量。“过滤2”后所得滤液直接排放会造成水体污染,须进行处理,可用熟石灰调节
_______ 使 完全沉淀。
完全沉淀。
(4)某实验小组利用离子膜电解技术电解氯化钴溶液,调节阴极室电解液的 为9.1~11,可在阴极室直接得到氢氧化钴,其原理如图丙所示。离子交换膜为
为9.1~11,可在阴极室直接得到氢氧化钴,其原理如图丙所示。离子交换膜为_______ (填“阳”或“阴”)离子交换膜,电路中每通过 电子时,两极室溶液质量变化的差值为
电子时,两极室溶液质量变化的差值为_______  。
。

 )制取
)制取 粗品及其他工业产品的工艺流程如图甲所示。
粗品及其他工业产品的工艺流程如图甲所示。
已知:“浸出液”中含有的阳离子主要有
 、
、 、
、 、
、 、
、 。
。回答下列问题:
(1)钴矿石浸出时加入
 的目的为
的目的为(2)溶液中
 (X表示
(X表示 、
、 、
、 、
、 、
、 、
、 )与
)与 的变化关系如图乙所示(离子浓度小于
的变化关系如图乙所示(离子浓度小于 可认为已除尽)。在浸出液中通入空气的目的是
可认为已除尽)。在浸出液中通入空气的目的是 至3.2,过滤1所得滤渣的主要成分为
至3.2,过滤1所得滤渣的主要成分为(3)用氧化镁调滤液1的
 为9.1时,得到的氢氧化钴粗品中含有的主要杂质为
为9.1时,得到的氢氧化钴粗品中含有的主要杂质为
 完全沉淀。
完全沉淀。(4)某实验小组利用离子膜电解技术电解氯化钴溶液,调节阴极室电解液的
 为9.1~11,可在阴极室直接得到氢氧化钴,其原理如图丙所示。离子交换膜为
为9.1~11,可在阴极室直接得到氢氧化钴,其原理如图丙所示。离子交换膜为 电子时,两极室溶液质量变化的差值为
电子时,两极室溶液质量变化的差值为 。
。
您最近半年使用:0次



