用粗制ZnO粉末(含杂质Fe、Ni等)制备高纯ZnO的流程如下:
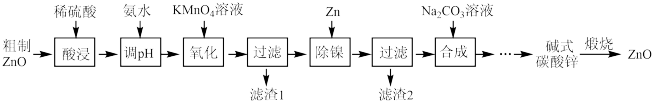
已知:本实验条件下,Ni2+不能被氧化,高锰酸钾还原产物为MnO2;过滤出滤渣1达到除铁目的。
(1)加快酸浸速率可采取的措施_____________________________ 。(任写一条)
(2)写出“除镍”步骤发生的主要反应离子方程式____________________________ 。
(3)“滤渣2”的成分是______ 。
(4)流程中“ ”涉及的操作有
”涉及的操作有______ 、洗涤、______ 。
(5)获得的碱式碳酸锌需要用水洗涤,检验沉淀是否洗涤干净的方法是_____ 。
(6)若碱式碳酸锌的成分是ZnCO3· xZn(OH)2。取干燥后的碱式碳酸锌11.2g,煅烧后可得到产品8.1g,则x等于______ 。

已知:本实验条件下,Ni2+不能被氧化,高锰酸钾还原产物为MnO2;过滤出滤渣1达到除铁目的。
(1)加快酸浸速率可采取的措施
(2)写出“除镍”步骤发生的主要反应离子方程式
(3)“滤渣2”的成分是
(4)流程中“
 ”涉及的操作有
”涉及的操作有(5)获得的碱式碳酸锌需要用水洗涤,检验沉淀是否洗涤干净的方法是
(6)若碱式碳酸锌的成分是ZnCO3· xZn(OH)2。取干燥后的碱式碳酸锌11.2g,煅烧后可得到产品8.1g,则x等于
更新时间:2019-09-11 23:19:00
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料、防腐等工业,它不溶于 、
、 和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[
和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[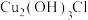 ]。以铜矿粉(含
]。以铜矿粉(含 、
、 、CuS及少量FeS等)为原料制取CuCl的工艺流程如图:
、CuS及少量FeS等)为原料制取CuCl的工艺流程如图:

已知:FeS高温条件下与氧气反应生成FeO; 高温条件下与氧气反应生成
高温条件下与氧气反应生成 ;
; 在酸性条件下会发生歧化反应。回答下列问题:
在酸性条件下会发生歧化反应。回答下列问题:
(1)“酸浸”时 发生反应的化学方程式为
发生反应的化学方程式为___________ 。“搅拌”时加入NaCl粉末的作用是___________ 。
(2)可在上述流程中循环利用的物质有___________ (填化学式),加热时试剂X的作用是___________ 。
(3)洗涤CuCl晶体所用的试剂为___________ (填序号),洗涤后并在真空干燥机内于70℃干燥2小时,冷却,密封包装。于70℃真空干燥的目的是___________ 。
a.饱和 溶液 b.NaOH溶液 c.无水乙醇 d.稀硫酸
溶液 b.NaOH溶液 c.无水乙醇 d.稀硫酸
(4)流程中“滤渣”的主要成分是___________ (填化学式)。
(5)测定产品中氯化亚铜的质量分数,实验过程如下:准确称取制备的氯化亚铜产品0.250g,将其置于足量的 溶液中,待样品全部溶解后,加入适量稀硫酸,用
溶液中,待样品全部溶解后,加入适量稀硫酸,用 的硫酸铈[
的硫酸铈[ ]标准溶液滴定到终点,消耗硫酸铈溶液24.60mL,反应中
]标准溶液滴定到终点,消耗硫酸铈溶液24.60mL,反应中 被还原为
被还原为 (已知
(已知 ),则产品中氯化亚铜的纯度为
),则产品中氯化亚铜的纯度为___________ (保留三位有效数字)。
 、
、 和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[
和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[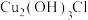 ]。以铜矿粉(含
]。以铜矿粉(含 、
、 、CuS及少量FeS等)为原料制取CuCl的工艺流程如图:
、CuS及少量FeS等)为原料制取CuCl的工艺流程如图:
已知:FeS高温条件下与氧气反应生成FeO;
 高温条件下与氧气反应生成
高温条件下与氧气反应生成 ;
; 在酸性条件下会发生歧化反应。回答下列问题:
在酸性条件下会发生歧化反应。回答下列问题:(1)“酸浸”时
 发生反应的化学方程式为
发生反应的化学方程式为(2)可在上述流程中循环利用的物质有
(3)洗涤CuCl晶体所用的试剂为
a.饱和
 溶液 b.NaOH溶液 c.无水乙醇 d.稀硫酸
溶液 b.NaOH溶液 c.无水乙醇 d.稀硫酸(4)流程中“滤渣”的主要成分是
(5)测定产品中氯化亚铜的质量分数,实验过程如下:准确称取制备的氯化亚铜产品0.250g,将其置于足量的
 溶液中,待样品全部溶解后,加入适量稀硫酸,用
溶液中,待样品全部溶解后,加入适量稀硫酸,用 的硫酸铈[
的硫酸铈[ ]标准溶液滴定到终点,消耗硫酸铈溶液24.60mL,反应中
]标准溶液滴定到终点,消耗硫酸铈溶液24.60mL,反应中 被还原为
被还原为 (已知
(已知 ),则产品中氯化亚铜的纯度为
),则产品中氯化亚铜的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】含钒石煤(含有铁、硅、铝、钙、镁等元素的氧化物)中的钒大部分是以V(Ⅲ)和V(Ⅳ)形式存在,由含矾石煤提钒的一种工艺流程如下所示:

已知:铜铁试剂能与铜、铁、铝、钛等元素形成不溶于水的配合物。
回答下列问题:
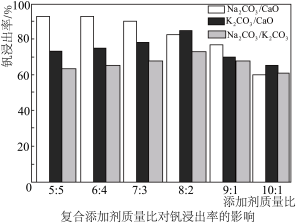
(1)含矾石煤预制时加入复合添加剂对钒浸出率的影响如图所示,其中最佳复合添加剂为__________ ,最佳添加比例为__________ 。
(2)上图为“抽滤”实验原理装置图,“抽滤”时抽气泵的作用是_________ ;“酸浸渣”经“水洗涤”返回“浸出”的目的是______________________________ 。
(3)已知酸浸液中 被H2O2氧化成
被H2O2氧化成 ,其离子方程式为
,其离子方程式为________ 。“净化除杂”时用铜铁试剂除去所含的Al3+、Fe3+等杂质离子而不通过调节酸浸液pH的原因是__________ 。
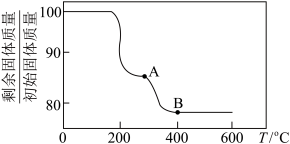
(4)“煅烧”纯净的沉钒产物过程中,固体残留率与温度变化如图所示。已知A点坐标为(260℃,85.47%),则A点对应物质的化学式为____________ ,B点对应的物质为V2O5,则B点坐标为___________ 。

已知:铜铁试剂能与铜、铁、铝、钛等元素形成不溶于水的配合物。
回答下列问题:
(1)含矾石煤预制时加入复合添加剂对钒浸出率的影响如图所示,其中最佳复合添加剂为

(2)上图为“抽滤”实验原理装置图,“抽滤”时抽气泵的作用是
(3)已知酸浸液中
 被H2O2氧化成
被H2O2氧化成 ,其离子方程式为
,其离子方程式为(4)“煅烧”纯净的沉钒产物过程中,固体残留率与温度变化如图所示。已知A点坐标为(260℃,85.47%),则A点对应物质的化学式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】脱除烟气中的氮氧化物(NOx)和SO2不仅可以改善环境,还能变废为宝,实践可持续发展。请回答下列问题:
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为____ 。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为:
NO+NO2+2OH-=2NO +H2O
+H2O
2NO2+2OH-=NO +NO
+NO +H2O
+H2O
吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是____ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是____ (填化学式)。
(3)NO的氧化吸收。在酸性NaClO溶液中,NO被氧化生成Cl-和NO ,其离子方程式为
,其离子方程式为____ 。
(4)某工厂以硝酸为原料生产亚硝酸钠,其工艺流程如图所示:
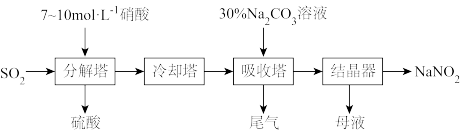
已知:Na2CO3+NO+NO2=2NaNO2+CO2。
“分解塔”中的温度不宜过高,其原因是____ 。
②按一定计量比在“分解塔”中通SO2和喷入硝酸,若反应后生成的NO与NO2物质的量之比恰好1∶1,则“分解塔”中发生反应的化学方程式为____ 。
③“分解塔”中的硝酸浓度不宜过大的原因是____ 。
④为提高氮氧化物的转化率,可向“尾气”中通入一定量的____ (填气体分子式),再通入“吸收塔”中,实现循环吸收。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为:
NO+NO2+2OH-=2NO
 +H2O
+H2O2NO2+2OH-=NO
 +NO
+NO +H2O
+H2O吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是
(3)NO的氧化吸收。在酸性NaClO溶液中,NO被氧化生成Cl-和NO
 ,其离子方程式为
,其离子方程式为(4)某工厂以硝酸为原料生产亚硝酸钠,其工艺流程如图所示:

已知:Na2CO3+NO+NO2=2NaNO2+CO2。
“分解塔”中的温度不宜过高,其原因是
②按一定计量比在“分解塔”中通SO2和喷入硝酸,若反应后生成的NO与NO2物质的量之比恰好1∶1,则“分解塔”中发生反应的化学方程式为
③“分解塔”中的硝酸浓度不宜过大的原因是
④为提高氮氧化物的转化率,可向“尾气”中通入一定量的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氮化锂(Li3N)是有机合成的催化剂,Li3N遇水剧烈反应,金属Li的化学性质与镁相似。某小组设计实验制备氮化锂并测定其纯度,装置如图所示:
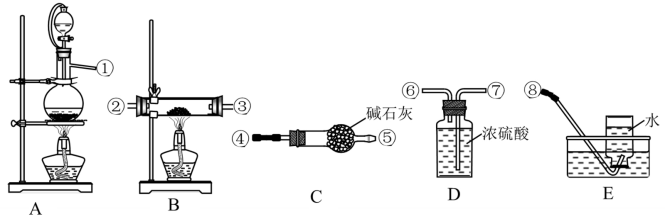
Ⅰ、制备氮化锂:实验室用NH4Cl溶液和NaNO2溶液共热制备N2。选择下图中的装置制备氮化锂(装置可重复使用):
(1)装置的接口连接顺序为____________ (从左至右,填数字序号)。
(2)实验室将锂保存在____ (填“煤油”“石蜡油”或“水”)中。
(3)制备N2的化学方程式为_________ 。
Ⅱ、测定Li3N产品纯度:取a g Li3N产品按如下图所示装置实验。
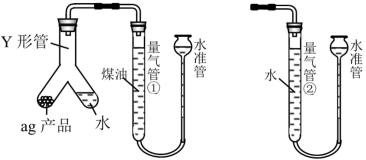
(4)连接好装置后,检查装置气密性的操作是_______ 。装好药品,启动反应的操作是_________ 。
(5)反应完毕并冷却之后,将气体全部排入量气管①中,量气管①的读数为V1 mL(已换算成标准状况,下同),将量气管①中气体缓慢导入量气管②,读数为V2 mL。该样品的纯度为___________ (用含a、V1、V2的代数式表示,不必化简)。若在量气管②中V2读数时,水准管液面高于左侧液面,测得产品纯度将_______ (填“偏高”“偏低”或“无影响”)。

Ⅰ、制备氮化锂:实验室用NH4Cl溶液和NaNO2溶液共热制备N2。选择下图中的装置制备氮化锂(装置可重复使用):
(1)装置的接口连接顺序为
(2)实验室将锂保存在
(3)制备N2的化学方程式为
Ⅱ、测定Li3N产品纯度:取a g Li3N产品按如下图所示装置实验。

(4)连接好装置后,检查装置气密性的操作是
(5)反应完毕并冷却之后,将气体全部排入量气管①中,量气管①的读数为V1 mL(已换算成标准状况,下同),将量气管①中气体缓慢导入量气管②,读数为V2 mL。该样品的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
真题
名校
【推荐2】氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:

回答下列问题:
(1)步骤①中得到的氧化产物是_________ ,溶解温度应控制在60~70度,原因是__________ 。
(2)写出步骤③中主要反应的离子方程式___________ 。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_________ (写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是______________________________ 。
(5)步骤②、④、⑤、⑧都要进行固液分离。工业上常用的固液分离设备有__________ (填字母)
(6)准确称取所制备的氯化亚铜样品m g,将其置于若两的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液b mL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为__________ 。

回答下列问题:
(1)步骤①中得到的氧化产物是
(2)写出步骤③中主要反应的离子方程式
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是
(4)上述工艺中,步骤⑥不能省略,理由是
(5)步骤②、④、⑤、⑧都要进行固液分离。工业上常用的固液分离设备有
| A.分馏塔 | B.离心机 | C.反应釜 | D.框式压滤机 |
(6)准确称取所制备的氯化亚铜样品m g,将其置于若两的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液b mL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铁红( )常用于油漆、油墨及橡胶工业。工业上以一定质量的硫铁矿烧渣(主要成分为
)常用于油漆、油墨及橡胶工业。工业上以一定质量的硫铁矿烧渣(主要成分为 、
、 ,另含少量难溶杂质)为主要原料制备铁红的一种工艺流程如下:
,另含少量难溶杂质)为主要原料制备铁红的一种工艺流程如下:

回答下列问题:
(1)工业常将硫铁矿烧渣经过粉碎后再进行“酸浸”,其目的是_______ 。
(2)“酸浸”时加入的硫酸不宜过量太多的原因是_______ 。“酸浸”过程中主要反应的离子方程式为_______ 。
(3)“过滤1”所得滤液中含有的阳离子有_______ 。
(4)“过滤2”所得滤渣的主要成分为 和
和 ,所得滤液中的主要溶质是
,所得滤液中的主要溶质是_______ (填化学式)。
(5)写出 在空气中焙烧生成铁红的化学方程式:
在空气中焙烧生成铁红的化学方程式:_______ 。
(6)焙烧后的产物铁红中含有 ,欲验证其中存在
,欲验证其中存在 ,应选用的试剂是
,应选用的试剂是_______ 。
 )常用于油漆、油墨及橡胶工业。工业上以一定质量的硫铁矿烧渣(主要成分为
)常用于油漆、油墨及橡胶工业。工业上以一定质量的硫铁矿烧渣(主要成分为 、
、 ,另含少量难溶杂质)为主要原料制备铁红的一种工艺流程如下:
,另含少量难溶杂质)为主要原料制备铁红的一种工艺流程如下:
回答下列问题:
(1)工业常将硫铁矿烧渣经过粉碎后再进行“酸浸”,其目的是
(2)“酸浸”时加入的硫酸不宜过量太多的原因是
(3)“过滤1”所得滤液中含有的阳离子有
(4)“过滤2”所得滤渣的主要成分为
 和
和 ,所得滤液中的主要溶质是
,所得滤液中的主要溶质是(5)写出
 在空气中焙烧生成铁红的化学方程式:
在空气中焙烧生成铁红的化学方程式:(6)焙烧后的产物铁红中含有
 ,欲验证其中存在
,欲验证其中存在 ,应选用的试剂是
,应选用的试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】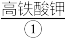 (K2FeO4)是一种高效多功能的新型绿色消毒剂。制备高铁酸钾的方法如下:将
(K2FeO4)是一种高效多功能的新型绿色消毒剂。制备高铁酸钾的方法如下:将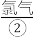 通入
通入 中生成饱和
中生成饱和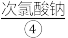 浓碱溶液,缓慢加入
浓碱溶液,缓慢加入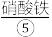 反应生成
反应生成 ,用
,用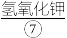 使其转化成高铁酸钾,抽滤得粗品,再用氢氧化钾溶液溶解,重结晶,用
使其转化成高铁酸钾,抽滤得粗品,再用氢氧化钾溶液溶解,重结晶,用 和
和 进行脱碱、
进行脱碱、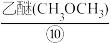 洗涤,干燥制得高铁酸钾。可用如图表示K2FeO4的制备过程:
洗涤,干燥制得高铁酸钾。可用如图表示K2FeO4的制备过程:
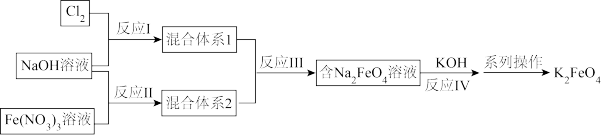
已知反应III的化学方程式为2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O。
请回答下列问题:
(1)在上述标有①~⑩序号的物质中,属于混合物的是____ (填序号,下同);属于盐的是____ ;属于有机物的是____ 。
(2)反应II的反应类型是____ (填四大基本反应类型之一)。
(3)写出Fe(NO3)3的电离方程式:_____ 。
(4)写出反应I的离子方程式:____ 。
(5)若生成166gNa2FeO4,则反应Ⅲ需要消耗4mol•L-1NaOH溶液的体积为____ mL。
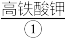 (K2FeO4)是一种高效多功能的新型绿色消毒剂。制备高铁酸钾的方法如下:将
(K2FeO4)是一种高效多功能的新型绿色消毒剂。制备高铁酸钾的方法如下:将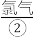 通入
通入 中生成饱和
中生成饱和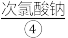 浓碱溶液,缓慢加入
浓碱溶液,缓慢加入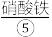 反应生成
反应生成 ,用
,用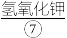 使其转化成高铁酸钾,抽滤得粗品,再用氢氧化钾溶液溶解,重结晶,用
使其转化成高铁酸钾,抽滤得粗品,再用氢氧化钾溶液溶解,重结晶,用 和
和 进行脱碱、
进行脱碱、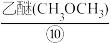 洗涤,干燥制得高铁酸钾。可用如图表示K2FeO4的制备过程:
洗涤,干燥制得高铁酸钾。可用如图表示K2FeO4的制备过程:
已知反应III的化学方程式为2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O。
请回答下列问题:
(1)在上述标有①~⑩序号的物质中,属于混合物的是
(2)反应II的反应类型是
(3)写出Fe(NO3)3的电离方程式:
(4)写出反应I的离子方程式:
(5)若生成166gNa2FeO4,则反应Ⅲ需要消耗4mol•L-1NaOH溶液的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】我们已经学过氢气、氧气、二氧化碳、氯气、二氧化硫、氨气等气体的制备方法和化学性质。以下如图是实验室制备、洗涤、干燥气体及进行尾气处理的常见装置。请结合所学知识回答下列问题:
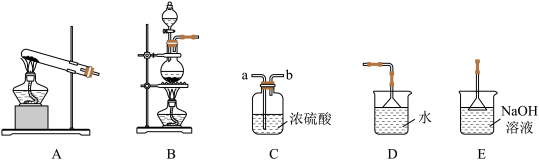
(1)下列气体中,只能用碱石灰干燥的是___________ 。(填字母)
A.H2 B.Cl2 C.SO2 D.NH3 E.O2 F.NO2
(2)实验室用软锰矿主要成分是与浓盐酸混合加热制得氯气,所选制备装置是___________ ,尾气处理装置中发生的离子反应方程式是___________ 。
(3)实验室用氯化铵和熟石灰制取氨气的化学反应方程式为___________ ,收集氨气方法是___________ 。
(4)如图虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,填写下列空白:如果将仪器的连接顺序变为①③②,则可以检出的物质是___________ ;不能检出的物质是___________

(1)下列气体中,只能用碱石灰干燥的是
A.H2 B.Cl2 C.SO2 D.NH3 E.O2 F.NO2
(2)实验室用软锰矿主要成分是与浓盐酸混合加热制得氯气,所选制备装置是
(3)实验室用氯化铵和熟石灰制取氨气的化学反应方程式为
(4)如图虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,填写下列空白:如果将仪器的连接顺序变为①③②,则可以检出的物质是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上用黄铁矿(主要成分为 ,其中硫元素为
,其中硫元素为 价)在高温条件下和氧气反应制备
价)在高温条件下和氧气反应制备 :
: ,该反应中被氧化的元素是
,该反应中被氧化的元素是______ (填元素符号)。当该反应转移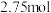 电子时,生成的二氧化硫在标准状况下的体积为
电子时,生成的二氧化硫在标准状况下的体积为______  。
。
(2)实验室中用下列装置测定 被催化氧化为
被催化氧化为 的转化率。(已知
的转化率。(已知 的熔点为
的熔点为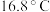 ,假设气体进入装置时均被完全吸收,且忽略空气中
,假设气体进入装置时均被完全吸收,且忽略空气中 的影响)
的影响)

①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作:______ 。
②当停止通入 ,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是______ 。
③实验结束后,若装置 增加的质量为mg,装置
增加的质量为mg,装置 中产生白色沉淀的质量为ng,则此条件下二氧化硫的转化率是
中产生白色沉淀的质量为ng,则此条件下二氧化硫的转化率是______ (用含字母的代数式表示,不用化简)。
(3)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。
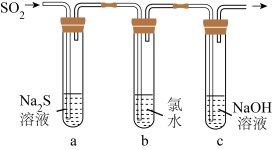
①能说明二氧化硫具有氧化性的实验现象为______ 。
②为验证二氧化硫的还原性,反应一段时间后,取试管 中的溶液分成三份,分别进行如下实验。
中的溶液分成三份,分别进行如下实验。
方案Ⅰ:向第一份溶液中加入 溶液,有白色沉淀生成
溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液中加入 溶液,产生白色沉淀
溶液,产生白色沉淀
上述方案合理的是______ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管 中发生反应的离子方程式为
中发生反应的离子方程式为______ 。
(1)工业上用黄铁矿(主要成分为
 ,其中硫元素为
,其中硫元素为 价)在高温条件下和氧气反应制备
价)在高温条件下和氧气反应制备 :
: ,该反应中被氧化的元素是
,该反应中被氧化的元素是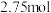 电子时,生成的二氧化硫在标准状况下的体积为
电子时,生成的二氧化硫在标准状况下的体积为 。
。(2)实验室中用下列装置测定
 被催化氧化为
被催化氧化为 的转化率。(已知
的转化率。(已知 的熔点为
的熔点为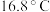 ,假设气体进入装置时均被完全吸收,且忽略空气中
,假设气体进入装置时均被完全吸收,且忽略空气中 的影响)
的影响)
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作:
②当停止通入
 ,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是③实验结束后,若装置
 增加的质量为mg,装置
增加的质量为mg,装置 中产生白色沉淀的质量为ng,则此条件下二氧化硫的转化率是
中产生白色沉淀的质量为ng,则此条件下二氧化硫的转化率是(3)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。

①能说明二氧化硫具有氧化性的实验现象为
②为验证二氧化硫的还原性,反应一段时间后,取试管
 中的溶液分成三份,分别进行如下实验。
中的溶液分成三份,分别进行如下实验。方案Ⅰ:向第一份溶液中加入
 溶液,有白色沉淀生成
溶液,有白色沉淀生成方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液中加入
 溶液,产生白色沉淀
溶液,产生白色沉淀上述方案合理的是
 中发生反应的离子方程式为
中发生反应的离子方程式为
您最近一年使用:0次



