下列说法正确的是 ( )
| A.一定条件下,增加反应物的量,必加快反应速率 |
| B.升高温度对放热反应会减慢反应速率,而对吸热反应才会加快反应速率 |
| C.缩小体积,增大压强,对气体反应都会加快反应速率 |
| D.使用催化剂一定会加快反应速率,并使平衡发生移动 |
更新时间:2019-11-03 10:05:31
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
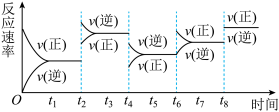
【推荐1】一定条件下,
 。下列有关叙述正确的是
。下列有关叙述正确的是

 。下列有关叙述正确的是
。下列有关叙述正确的是A.升高温度,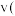 正 正 增大, 增大,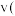 逆 逆 减小 减小 |
B.增大压强,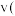 正 正 增大, 增大,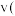 逆 逆 增大 增大 |
C.恒温恒压,再充入 ,反应速率不变 ,反应速率不变 |
D.增加炭的用量,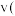 正 正 增大 增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】高能固氮反应条件苛刻,计算机模拟该历程如图所示,在放电的条件下,微量的O2或N2裂解成游离的O或N原子,分别与N2和O2发生以下连续反应生成NO。下列说法错误的
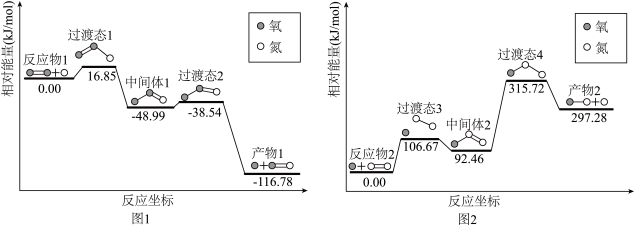

| A.图1中,中间体1到产物1的方程式为O-O=N→O+N=O |
| B.NO的生成速率很慢是因为图2中间体2到过渡态4的能垒较大 |
| C.由O和N2制NO的活化能为215.72kJ•mol-1 |
| D.由N和O2制NO的过程比由O原子和N2制NO的过程速率快 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】合成氨工业中,原料气( 、
、 及少量CO、
及少量CO、 的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
 。以下说法错误的是
。以下说法错误的是
 、
、 及少量CO、
及少量CO、 的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
 。以下说法错误的是
。以下说法错误的是A.原料气中 的体积分数越大,平衡混合物中氨的体积分数也越大 的体积分数越大,平衡混合物中氨的体积分数也越大 |
| B.杂质有可能引发催化剂中毒 |
| C.使用催化剂可降低反应的活化能,大大提高生产效率 |
| D.铜氨液再生的适宜条件是高温低压 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】科学家利用过渡金属氮化物(TMNS)在常温下催化实现氨的合成,其反应机理如图所示。下列有关说法错误的是


| A.TMNS大大降低了合成氨反应的焓变 |
| B.TMNS表面上的N原子最终被还原为氨 |
| C.TMNS表面上氨脱附产生的空位有利于吸附N2 |
| D.用同位素标记后的15N2进行该合成反应,产物中不只有15NH3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】五氯化磷(PCl5)是有机合成中重要的氯化剂,可由如下反应制得:PCl3(g)+Cl2(g)⇌PCl5(g) ΔH=-93.0 kJ/mol。某温度下,在2.0 L的恒容密闭容器中充入2.0 mol PCl3和1.0 mol Cl2,实验数据记录如下。
下列说法正确的是
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl5)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
| A.0~150 s内的υ (PCl3) = 2.4×10-3mol·L-1·s-1 |
B.该温度下,反应的化学平衡常数K = 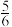 |
| C.升高温度,PCl3的平衡转化率大于20% |
| D.增大压强,活化分子百分数增大,反应速率加快 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关说法中正确的是
| A.影响化学反应速率的主要因素为浓度、温度、压强和催化剂 |
| B.对于Fe与稀H2SO4反应,能加快H2的生成速率的措施可以是将稀硫酸改为98%的浓硫酸 |
C.已达平衡的2NO2(g) N2O4(g)体系,压缩体积,再达平衡时气体颜色比原平衡的深 N2O4(g)体系,压缩体积,再达平衡时气体颜色比原平衡的深 |
D.恒温恒容时,向已达平衡的2HI(g) I2(g)+H2(g)体系中充入HI,HI转化率将升高 I2(g)+H2(g)体系中充入HI,HI转化率将升高 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】从下列实验事实所引出的相应结论正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 其它条件相同,Na2S2O3溶液浓度越大,析出硫沉淀所需时间越短 | 当其他条件不变时,增大反应物浓度化学反应速率加快 |
| B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
| C | H+浓度相同的盐酸和硫酸分别与形状相同的等质量的锌粒反应 | 反应开始时速率不相同 |
| D | 在容积可变的密闭容器中发生反应H2(g)+I2(g)  2HI(g),把容积缩小一倍 2HI(g),把容积缩小一倍 | 反应速率不变 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次

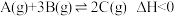 。该反应的速率与时间的关系如图所示:
。该反应的速率与时间的关系如图所示: