下列溶液一定呈中性的是:
| A.pH=7的溶液 | B.Kw=1.0×10-14的溶液 |
| C.c2(OH-)=Kw | D.pH=3的酸与pH=11的碱等体积混合后的溶液 |
更新时间:2019-11-17 13:01:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
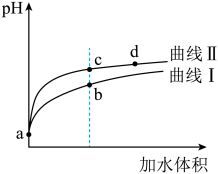
【推荐1】某温度下,HNO2和CH3COOH的电离常数分别为5.0×10-4和1.7×10-5。将 和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
 和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
| A.曲线Ⅰ代表HNO2溶液 |
| B.溶液中水的电离程度:b点>c点 |
| C.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同 |
D.c点到d点,溶液中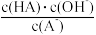 保持不变(HA、A-代表相应的酸和酸根离子) 保持不变(HA、A-代表相应的酸和酸根离子) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列图示与对应的叙述相符的是

A.  图所示的反应,若升高温度,该反应的平衡常数变小 图所示的反应,若升高温度,该反应的平衡常数变小 |
B.  图所示的是 图所示的是 与 与 反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在 反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在 |
C.  表示等pH的盐酸与醋酸中分别加水稀释的pH变化,其中曲线b对应的是盐酸 表示等pH的盐酸与醋酸中分别加水稀释的pH变化,其中曲线b对应的是盐酸 |
D.  表示向 表示向 溶液中逐滴加稀盐酸,生成 溶液中逐滴加稀盐酸,生成 与所甲盐酸物质的量的关系 与所甲盐酸物质的量的关系 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述正确的是
| A.强电解质溶液中一定不存在电离平衡 |
| B.在恒温条件下,增大压强,化学反速率一定加快 |
| C.两种醋酸的物质的量浓度分别为c1和c2,pH分别a和a+1,则c1=10c2 |
| D.常温下,pH=3的醋酸与pH=11的NaOH等体积混合后,溶液pH<7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下 溶液中各含碳粒子的物质的量分数与pH的关系如图1所示。向碳酸钠和碳酸氢钠混合溶液中滴加氯化钡溶液,溶液中
溶液中各含碳粒子的物质的量分数与pH的关系如图1所示。向碳酸钠和碳酸氢钠混合溶液中滴加氯化钡溶液,溶液中 与
与 的关系如图2所示。下列说法正确的是
的关系如图2所示。下列说法正确的是

 溶液中各含碳粒子的物质的量分数与pH的关系如图1所示。向碳酸钠和碳酸氢钠混合溶液中滴加氯化钡溶液,溶液中
溶液中各含碳粒子的物质的量分数与pH的关系如图1所示。向碳酸钠和碳酸氢钠混合溶液中滴加氯化钡溶液,溶液中 与
与 的关系如图2所示。下列说法正确的是
的关系如图2所示。下列说法正确的是
A.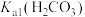 的数量级为 的数量级为 |
B.a对应的溶液中存在: |
C.a→b的过程中,溶液中 一直增大 一直增大 |
| D.b点对应溶液的pH为8.25 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度下,将pH和体积均相同的HCl和CH3COOH溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述正确的是


| A.曲线II代表HCl的稀释过程 |
| B.溶液中水的电离程度:b点>c点 |
C.从b点到d点,溶液中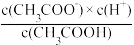 保持不变 保持不变 |
| D.该温度下,b点Kw的数值比e点大 |
您最近一年使用:0次
【推荐2】下列有关图示说法不正确的是( )


| A.图甲表示水中c(H+)和c(OH-)的关系,则XZ线上任意点均表示溶液呈中性 |
| B.图乙表示由2 mol A(g)和4 mol B(g)形成4 mol A—B键放出E2 kJ能量 |
| C.25℃时向l00mL0.1mol/L NH4HSO4溶液中滴加0.lmol/L NaOH溶液的pH与NaOH溶液体积关系曲线如图丙,则a点到b点过程中,溶液导电能力增强 |
| D.图丁装置(电极均为惰性电极)可吸收SO2,其阴极反应式为2HSO3-+2e-+2H+=S2O42-+2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度时水的离子积常数Kw=10-13,将此温度下将同浓度的NaOH溶液与稀硫酸按一定体积比 3∶1混合,若所得混合液pH=12,则原溶液的浓度为
| A.0.40mol·L-1 | B.0.20mol·L-1 |
| C.0.04mol·L-1 | D.0.50mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,一种c(H+)=10-3mol/L的酸溶液和一种c(OH-)=10-3mol/L的碱溶液等体积混合,下列说法错误的是
| A.混合前pH酸+pH碱=14 |
| B.混合后溶液一定显中性 |
| C.相比于混合前,混合后水的电离程度增大 |
| D.酸溶液中溶质的物质的量浓度可能小于10-3mol/L |
您最近一年使用:0次

 溶液和20.00mL浓度为c2的
溶液和20.00mL浓度为c2的 溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点(这两点的横坐标分别为10.60mL和17.20mL)。下列说法不正确的是
溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点(这两点的横坐标分别为10.60mL和17.20mL)。下列说法不正确的是
 溶液中,
溶液中,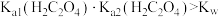
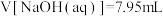 ,则a点有
,则a点有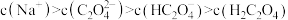
 ,则b点消耗了8.60mLNaOH溶液
,则b点消耗了8.60mLNaOH溶液 Mg(OH)2
Mg(OH)2 MgCl2(aq)→MgCl2(s)
MgCl2(aq)→MgCl2(s) Mg
Mg Ca2+(aq)+Mg(OH)2(s)的K=
Ca2+(aq)+Mg(OH)2(s)的K=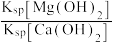
 H++A-
H++A-

