在200 ℃,将1 mol H2(g)和2 mol I2(g)充入到体积为V L的密闭容器中,发生反应:I2(g)+H2(g)  2HI(g) ΔH=-c kJ/mol
2HI(g) ΔH=-c kJ/mol
(1)反应刚开始时,由于c(H2)=______ mol/L,c(I2)=______ mol/L,而c(HI)=_____ ,所以化学反应速率 _______ 最大,而________ 最小(为零)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)_____ ,c(I2)_____ ,而c(HI)________ ,从而化学反应速率v(正)______ ,而v(逆)_____ 。(以上填“增大”“减小”或“不变”)
(3)当反应进行到v(正)与v(逆)_______ 时,此可逆反应就达到了平衡。若保持外界条件不变时,反应混合物的总物质的量为_______ mol。此时放出的热量Q_______ (填“>”“<”或“=”)c kJ。
 2HI(g) ΔH=-c kJ/mol
2HI(g) ΔH=-c kJ/mol(1)反应刚开始时,由于c(H2)=
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)
(3)当反应进行到v(正)与v(逆)
更新时间:2019-11-18 15:59:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】一定温度下,在2L的密闭容器中,M、N两种气体的物质的量随时间变化的曲线如图所示:

(1)反应的化学方程式为___________ 。
(2)反应达到化学平衡的时间是___________ min,该时间内的平均反应速率v(N)=___________ 。
(3)4min时,正、逆反应速率的大小关系为v正___________ v逆(填“>”“<”或“=”);
(4)一定温度下,将一定量的N2和H2充入固定容积催化剂的密闭容器中进行反应:N2(g)+3H2(g)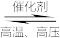 2NH3(g)。
2NH3(g)。
①下列描述能说明该可逆反应达到化学平衡状态的有___________ (填序号)。
A.容器内的压强不变
B.容器内气体的密度不变
C.相同时间内有3mol H-H键断裂,有6mol N-H键形成
D.c(N2):c(H2):c(NH3)=1︰3︰2
E.NH3的质量分数不再改变
②若起始时向容器中充入10mol·L-1的N2和15mol·L-1的H2,10min 时测得容器内NH3的浓度为1.5mol·L-1,10min内用N2表示的反应速率为___________ ;此时H2的转化率为___________ 。
(5)能加快反应速率的措施是___________ (填序号)
①升高温度 ②容器容积不变,充入惰性气体Ar ③容器压强不变,充入惰性气体Ar ④使用催化剂

(1)反应的化学方程式为
(2)反应达到化学平衡的时间是
(3)4min时,正、逆反应速率的大小关系为v正
(4)一定温度下,将一定量的N2和H2充入固定容积催化剂的密闭容器中进行反应:N2(g)+3H2(g)
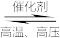 2NH3(g)。
2NH3(g)。①下列描述能说明该可逆反应达到化学平衡状态的有
A.容器内的压强不变
B.容器内气体的密度不变
C.相同时间内有3mol H-H键断裂,有6mol N-H键形成
D.c(N2):c(H2):c(NH3)=1︰3︰2
E.NH3的质量分数不再改变
②若起始时向容器中充入10mol·L-1的N2和15mol·L-1的H2,10min 时测得容器内NH3的浓度为1.5mol·L-1,10min内用N2表示的反应速率为
(5)能加快反应速率的措施是
①升高温度 ②容器容积不变,充入惰性气体Ar ③容器压强不变,充入惰性气体Ar ④使用催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某温度时,在0.5L密闭容器中,某一可逆反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析可得:

(1)该反应的化学方程式为____ 。
(2)若降低温度,则该反应的正反应速率______ ,逆反应速率______ (均填“加快”“减慢”或“不变”)。
(3)第4min时,正、逆反应速率的大小关系为:v(正)______ v(逆)(填“>”、“<”或“=”)。
(4)反应至4min时,A的转化率______ 。
(5)能判断该反应在一定温度下达到化学平衡状态的依据是_____ (填字母代号)。
A.v(A)=2v(B)
B.容器内压强不再发生变化
C.容器内气体密度不再发生变化
D.B的体积分数不再发生变化
E.容器内气体原子总数不再发生变化
F.相同时间内消耗2nmol的A的同时生成nmol的B

(1)该反应的化学方程式为
(2)若降低温度,则该反应的正反应速率
(3)第4min时,正、逆反应速率的大小关系为:v(正)
(4)反应至4min时,A的转化率
(5)能判断该反应在一定温度下达到化学平衡状态的依据是
A.v(A)=2v(B)
B.容器内压强不再发生变化
C.容器内气体密度不再发生变化
D.B的体积分数不再发生变化
E.容器内气体原子总数不再发生变化
F.相同时间内消耗2nmol的A的同时生成nmol的B
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】一定条件下,恒容密闭容器中发生某可逆反应,A、B、C三种气体的物质的量浓度随时间的变化如图所示。请回答下列问题:
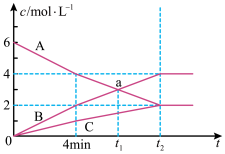
(1)此反应的化学方程式为___ 。
(2)反应从开始至4min末,用A表示的平均反应速率为____ 。
(3)t2的值___ 8(填“大于”、“等于”或“小于”),其原因是___ 。
(4)某同学经分析得出如下结论,其中正确的是___ (填选项序号)。
①该反应在t1时刻达到了反应限度
②保持条件不变,延续足够长的时间,容器中将可能不存在A物质
③该反应达到了反应限度后物质B的质量将保持不变
④改变反应条件将可能改变反应的限度

(1)此反应的化学方程式为
(2)反应从开始至4min末,用A表示的平均反应速率为
(3)t2的值
(4)某同学经分析得出如下结论,其中正确的是
①该反应在t1时刻达到了反应限度
②保持条件不变,延续足够长的时间,容器中将可能不存在A物质
③该反应达到了反应限度后物质B的质量将保持不变
④改变反应条件将可能改变反应的限度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】工业上可利用“甲烷蒸气转化法”生产氢气,反应的热化学方程式为CH4(g)+H2O(g)⇌CO2(g)+3H2(g) △H=+161.1kJ·mol-1
(1)已知温度、压强对甲烷平衡时的体积分数的影响如图1,请回答:
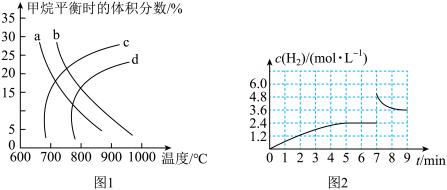
①图1中a、b、c、d四条曲线中的两条代表压强分别为1MPa、2MPa时甲烷体积分数的曲线,其中表示1MPa的是_____ 。
②该反应的平衡常数:K(600℃)___ (填“>”“<”或“=”)K(700℃)。
(2)①已知:在700℃、1MPa时,1molCH4与1molH2O在1L的密闭容器中反应,6min时达到平衡(如图2),此时CH4的转化率为__ ,该温度下反应的平衡常数为____ (结果保留小数点后一位数字)。
②从图2分析,由第一次平衡到第二次平衡,平衡移动的方向是____ (填“向正反应方向”或“向逆反应方向”)移动,采取的措施可能是____ 。
(1)已知温度、压强对甲烷平衡时的体积分数的影响如图1,请回答:

①图1中a、b、c、d四条曲线中的两条代表压强分别为1MPa、2MPa时甲烷体积分数的曲线,其中表示1MPa的是
②该反应的平衡常数:K(600℃)
(2)①已知:在700℃、1MPa时,1molCH4与1molH2O在1L的密闭容器中反应,6min时达到平衡(如图2),此时CH4的转化率为
②从图2分析,由第一次平衡到第二次平衡,平衡移动的方向是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(混合物平均摩尔质量通常可表示为: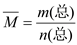 ,利用此概念可以讨论许多化学问题:
,利用此概念可以讨论许多化学问题:
(1)相同条件下,潮湿空气的密度___________ (选填“>”、“<”或“=”)干燥空气的密度,理由是___________ ___________________________________________________________________;
(2)在一定条件下的密闭容器中,以碳和水蒸气为反应物,发生反应:
C(s)+H2O(g) CO(g)+H2(g);达到平衡后保持温度不变并加压,则
CO(g)+H2(g);达到平衡后保持温度不变并加压,则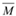 (混合气)将
(混合气)将___________ (填写“变大”、“变小”或“不变”);
(3)以物质的量之比为1:2相混合的Na2SO3和K2SO3的混合物共a g,与足量盐酸反应生成的SO2物质的量n(SO2)=___________ mol(用含a的代数式表示)。
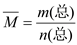 ,利用此概念可以讨论许多化学问题:
,利用此概念可以讨论许多化学问题:(1)相同条件下,潮湿空气的密度
(2)在一定条件下的密闭容器中,以碳和水蒸气为反应物,发生反应:
C(s)+H2O(g)
 CO(g)+H2(g);达到平衡后保持温度不变并加压,则
CO(g)+H2(g);达到平衡后保持温度不变并加压,则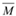 (混合气)将
(混合气)将(3)以物质的量之比为1:2相混合的Na2SO3和K2SO3的混合物共a g,与足量盐酸反应生成的SO2物质的量n(SO2)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】二烯烃与溴反应制备多卤代物,反应的区域选择性在有机合成中具有重要意义。1,3–丁二烯(g) (CH2=CH—CH=CH2)和Br2(g)反应原理如下:
①CH2=CH-CH=CH2(g)+Br2(g)→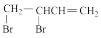 (g) △H1=akJ·mol-1
(g) △H1=akJ·mol-1
②CH2=CH-CH=CH2(g)+Br2(g)→ (g) △H2=bkJ·mol-1
(g) △H2=bkJ·mol-1
③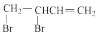 (g)⇌
(g)⇌ 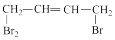 (g) △H3
(g) △H3
回答下列问题:
(1)△H3=_____________ 。
(2)1,3-丁二烯和Br2反应的能量随反应过程的变化关系如图所示:
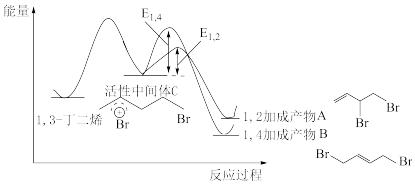
1,3-丁二烯和Br2反应会生成两种产物,一种称为动力学产物,由速率更快的反应生成;一种称为热力学产物,由产物更加稳定的反应生成。则动力学产物结构简式为_________
(3)T℃时在2L刚性密闭容器中充入1,3-丁二烯(g)(CH2=CH-CH=CH2)和Br2(g)各2mol,发生反应。1,3-丁二烯及产物的物质的量分数随时间的变化如下表:
在0 ~20min内,反应体系中1,4-加成产物的平均反应速率v(1,4加成产物)=_______ 。
(4)对于反应③,若要提高1,4-加成产物 (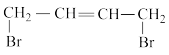 )平衡体系中的物质量分数,可以采取的措施有
)平衡体系中的物质量分数,可以采取的措施有_____
A.适当升高温度 B.使用合适的催化剂
C.增大体系的压强 D.将1,4加成产物及时从体系分离
(5)反应 1,3-丁二烯二聚体的解聚为可逆反应:
 (g)
(g) 2
2 (g) △H>0
(g) △H>0
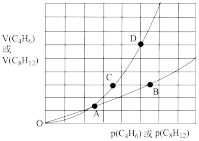
在一定条件下,C4H6和C8H12的消耗速率与各自分压有如下关系:v(C8H12)=k1·p(C8H12),v(C4H6)=k2·p2(C4H6)。相应的速率与其分压关系如图所示,一定温度下k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=_____ ;在图中标出点(A、B、C、D)中,能表示反应达到平衡状态的点是______ ,理由是________ 。
①CH2=CH-CH=CH2(g)+Br2(g)→
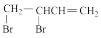 (g) △H1=akJ·mol-1
(g) △H1=akJ·mol-1②CH2=CH-CH=CH2(g)+Br2(g)→
 (g) △H2=bkJ·mol-1
(g) △H2=bkJ·mol-1③
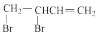 (g)⇌
(g)⇌ 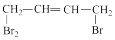 (g) △H3
(g) △H3回答下列问题:
(1)△H3=
(2)1,3-丁二烯和Br2反应的能量随反应过程的变化关系如图所示:

1,3-丁二烯和Br2反应会生成两种产物,一种称为动力学产物,由速率更快的反应生成;一种称为热力学产物,由产物更加稳定的反应生成。则动力学产物结构简式为
(3)T℃时在2L刚性密闭容器中充入1,3-丁二烯(g)(CH2=CH-CH=CH2)和Br2(g)各2mol,发生反应。1,3-丁二烯及产物的物质的量分数随时间的变化如下表:
| 时间(min) | 0 | 10 | 20 | 30 | 40 |
| 1,3-丁二烯 | 100% | 72% | 0% | 0% | 0% |
| 1,2加成产物 | 0% | 26% | 10% | 4% | 4% |
| 1,4加成产物 | 0% | 2% | 90% | 96% | 96% |
在0 ~20min内,反应体系中1,4-加成产物的平均反应速率v(1,4加成产物)=
(4)对于反应③,若要提高1,4-加成产物 (
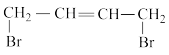 )平衡体系中的物质量分数,可以采取的措施有
)平衡体系中的物质量分数,可以采取的措施有A.适当升高温度 B.使用合适的催化剂
C.增大体系的压强 D.将1,4加成产物及时从体系分离
(5)反应 1,3-丁二烯二聚体的解聚为可逆反应:
 (g)
(g) 2
2 (g) △H>0
(g) △H>0在一定条件下,C4H6和C8H12的消耗速率与各自分压有如下关系:v(C8H12)=k1·p(C8H12),v(C4H6)=k2·p2(C4H6)。相应的速率与其分压关系如图所示,一定温度下k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】科研人员在 的综合利用研究中发现
的综合利用研究中发现 与
与 、
、 等反应可转化为有机物(如甲醇、乙醛、淀粉等)。一定条件下,将1mol
等反应可转化为有机物(如甲醇、乙醛、淀粉等)。一定条件下,将1mol 和3mol
和3mol 充入容积为2L的恒温恒容密闭容器中,发生反应
充入容积为2L的恒温恒容密闭容器中,发生反应 ,测得
,测得 和
和 的物质的量随时间的变化情况如表。
的物质的量随时间的变化情况如表。
请回答下列问题:
(1)试推断a=_______ ,理由为_______ 。
(2)4min时,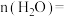
_______ mol。
(3)0~2min内,
_______ 
(4)下列描述中能说明反应达到平衡状态的是_______ (填标号)。
①当容器中气体密度不再变化时
②混合气体的压强不随时间的变化而变化
③单位时间内生成3mol ,同时生成1mol
,同时生成1mol 
④当容器中 、
、 、
、 、
、 的物质的量之比为3:9:2:2时
的物质的量之比为3:9:2:2时
(5)反应起始至4min时,反应容器内气体的平均相对分子质量随着反应的进行而_______ (填“增大”或“减小”);设反应起始时的总压强为p(始),平衡时的总压强为p(平衡),则p(始):p(平衡)=_______ 。
 的综合利用研究中发现
的综合利用研究中发现 与
与 、
、 等反应可转化为有机物(如甲醇、乙醛、淀粉等)。一定条件下,将1mol
等反应可转化为有机物(如甲醇、乙醛、淀粉等)。一定条件下,将1mol 和3mol
和3mol 充入容积为2L的恒温恒容密闭容器中,发生反应
充入容积为2L的恒温恒容密闭容器中,发生反应 ,测得
,测得 和
和 的物质的量随时间的变化情况如表。
的物质的量随时间的变化情况如表。| 时间 | 0min | 2min | 4min | 6min | 8min |
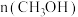 /mol /mol | 0 | 0.40 | 0.70 | 0.80 | 0.80 |
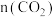 /mol /mol | 1.00 | 0.60 | 0.30 | a | 0.20 |
请回答下列问题:
(1)试推断a=
(2)4min时,
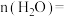
(3)0~2min内,


(4)下列描述中能说明反应达到平衡状态的是
①当容器中气体密度不再变化时
②混合气体的压强不随时间的变化而变化
③单位时间内生成3mol
 ,同时生成1mol
,同时生成1mol 
④当容器中
 、
、 、
、 、
、 的物质的量之比为3:9:2:2时
的物质的量之比为3:9:2:2时(5)反应起始至4min时,反应容器内气体的平均相对分子质量随着反应的进行而
您最近一年使用:0次
【推荐2】光气(COCl2)的分解反应为:COCl2(g) Cl2(g)+CO(g)ΔH=+108kJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如图所示(第10min到14min的COCl2浓度变化曲线未示出):
Cl2(g)+CO(g)ΔH=+108kJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如图所示(第10min到14min的COCl2浓度变化曲线未示出):

(1)计算反应在第8min时的平衡常数K=__ ;
(2)比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2)__ T(8)(填“<”、“>”或“=”);
(3)若12min时反应于温度T(8)下重新达到平衡,则此时c(COCl2)=__ mol·L-1;
(4)比较产物CO在2~3min、5~6min和12~13min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)、v(12~13)表示]的大小__ ;
(5)比较反应物COCl2在5~6min和15~16min时平均反应速率的大小:v(5~6)__ v(15~16)(填“<”、“>”或“=”),原因是__ 。
 Cl2(g)+CO(g)ΔH=+108kJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如图所示(第10min到14min的COCl2浓度变化曲线未示出):
Cl2(g)+CO(g)ΔH=+108kJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如图所示(第10min到14min的COCl2浓度变化曲线未示出):
(1)计算反应在第8min时的平衡常数K=
(2)比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2)
(3)若12min时反应于温度T(8)下重新达到平衡,则此时c(COCl2)=
(4)比较产物CO在2~3min、5~6min和12~13min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)、v(12~13)表示]的大小
(5)比较反应物COCl2在5~6min和15~16min时平均反应速率的大小:v(5~6)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】一定温度下,在三个体积均为2.0L的恒容密闭容器中分别加入一定量的X,发生反应: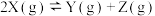 ,相关数据如下表所示:
,相关数据如下表所示:
回答下列问题:
(1)表中a=_______ ,c=_______ 。
(2)容器Ⅱ中平衡常数K=_______ ;容器Ⅰ和容器Ⅱ中X的转化率α(Ⅰ)_______ (填“大于”、“小于”或“等于”)α(Ⅱ)。
(3)已知 ,则该正反应为
,则该正反应为_______ (填“放热”或“吸热”)反应,判断理由是_______ 。
(4)387℃时,向容器Ⅰ中充入0.1 mol X、0.15 mol Y和0.10 mol Z,则反应将向_______ (填“正”或“逆”)反应方向进行,判断理由是_______ 。
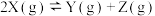 ,相关数据如下表所示:
,相关数据如下表所示:| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| X(g) | Y(g) | Z(g) | ||
| Ⅰ | 387 | 0.20 | 0.080 | a |
| Ⅱ |  | 0.40 | b | 0.160 |
| Ⅲ |  | 0.20 | c | 0.090 |
(1)表中a=
(2)容器Ⅱ中平衡常数K=
(3)已知
 ,则该正反应为
,则该正反应为(4)387℃时,向容器Ⅰ中充入0.1 mol X、0.15 mol Y和0.10 mol Z,则反应将向
您最近一年使用:0次



