(1)实验室可以用KMnO4制备氯气,反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
①该反应的氧化剂是____ ,氧化产物是_____ ,还原产物是____ 。
②当有15.8gKMnO4参加反应时,被氧化的HCl有___ mol,标况下生成Cl2的体积为____ L,有____ mol电子转移。
(2)A的核电荷数为n,A2+和B3-的电子层结构相同,则B原子的质子数是__ 。
(3)在1H216O、2H217O、2H218O、1H35Cl、1H37Cl中,共存在__ 种原子,_ 种元素。
(4)将K(Al2Si3O9)(OH)改写为氧化物形式:____ 。
①该反应的氧化剂是
②当有15.8gKMnO4参加反应时,被氧化的HCl有
(2)A的核电荷数为n,A2+和B3-的电子层结构相同,则B原子的质子数是
(3)在1H216O、2H217O、2H218O、1H35Cl、1H37Cl中,共存在
(4)将K(Al2Si3O9)(OH)改写为氧化物形式:
18-19高一·浙江·期末 查看更多[1]
(已下线)【新东方】高中化学5004
更新时间:2019-11-08 13:00:45
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)取300mL0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量为_______ mol。
(2)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是_______ ,又变为棕黄色的原因用离子方程式解释_______ 。
(3)在1LFeBr2溶液中通入标准状况下2.24LCl2,溶液中有 的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为_______ 。
(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式为_______ 。向反应后的溶液中通入过量CO2,反应的离子方程式为_______ 。
(5)三氟化氮(NF3)是一种无色、无臭的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,写出该反应的化学方程式_______ ,反应中生成0.2molHNO3,转移的电子数目为_______
(6)草酸晶体的组成可表示为:H2C2O4·xH2O,为测定x值,进行下列实验。
①称取mg草酸晶体,配成100.0mL无色溶液。
②取25.0mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,缓缓滴入浓度为cmol·L-1KMnO4溶液与之反应,所发生反应方程式为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
实验结束的标准是_______ 。若整个过程滴入高锰酸钾溶液amL,则实验所配得的草酸溶液的物质的量浓度为_______ ,因此计算出草酸晶体x值为_______ 。
(2)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
(3)在1LFeBr2溶液中通入标准状况下2.24LCl2,溶液中有
 的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式为
(5)三氟化氮(NF3)是一种无色、无臭的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,写出该反应的化学方程式
(6)草酸晶体的组成可表示为:H2C2O4·xH2O,为测定x值,进行下列实验。
①称取mg草酸晶体,配成100.0mL无色溶液。
②取25.0mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,缓缓滴入浓度为cmol·L-1KMnO4溶液与之反应,所发生反应方程式为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
实验结束的标准是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题
(1)计算标准状况下,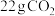 气体的体积是
气体的体积是_______ L,与_______ 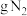 含有相同的分子数。
含有相同的分子数。
(2) 溶液中含b个
溶液中含b个 ,求阿伏加德罗常数
,求阿伏加德罗常数_______ (用a、b表示)。
(3)已知反应: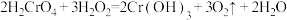 ,该反应中
,该反应中 只发生如下变化过程:
只发生如下变化过程: ,该反应中的还原剂是
,该反应中的还原剂是_______ ,若产生的气体在标准状况下体积为3.36 L,则反应中转移了_______ mol电子。
(1)计算标准状况下,
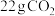 气体的体积是
气体的体积是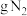 含有相同的分子数。
含有相同的分子数。(2)
 溶液中含b个
溶液中含b个 ,求阿伏加德罗常数
,求阿伏加德罗常数(3)已知反应:
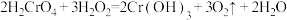 ,该反应中
,该反应中 只发生如下变化过程:
只发生如下变化过程: ,该反应中的还原剂是
,该反应中的还原剂是
您最近一年使用:0次
【推荐3】现有下列反应:
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)氧化剂的氧化性强弱顺序为____ ,还原剂的还原性强弱顺序为____ 。
(2)反应①中氧化剂是_____ 氧化产物是________ 。氧化产物和还原产物质量之比为____ 。
(3)反应②中氯化氢表现出的性质是____ 。
A.还原性 B.酸性
C.氧化性
(4)用单线桥法表示反应①的电子转移情况___
(5)用双线桥法表示反应②的电子转移情况___
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)氧化剂的氧化性强弱顺序为
(2)反应①中氧化剂是
(3)反应②中氯化氢表现出的性质是
A.还原性 B.酸性
C.氧化性
(4)用单线桥法表示反应①的电子转移情况
(5)用双线桥法表示反应②的电子转移情况
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
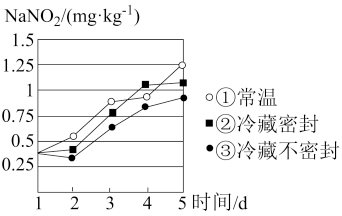
【推荐1】亚硝酸钠( ,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸(
,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸( )是一种弱酸,不稳定,易分解生成NO(无色)气体和
)是一种弱酸,不稳定,易分解生成NO(无色)气体和 (红棕色)气体;
(红棕色)气体; 是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:
是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:
(1)人体正常的血红蛋白含有 ,若误食亚硝酸钠会把
,若误食亚硝酸钠会把 转换为
转换为 而中毒,应立即注射美蓝溶液进行治疗。上述过程中
而中毒,应立即注射美蓝溶液进行治疗。上述过程中 表现出
表现出_______ 性(填“氧化”或“还原”下同),亚硝酸钠作_______ 剂,美蓝溶液被_______ 。
(2)下列有关检验工业食盐中是否混有亚硝酸钠的说法错误的是_______ 。
A.取样品,加碘化钾淀粉溶液,酸化后溶液变蓝,说明样品中含有亚硝酸钠
B.取样品,加稀硫酸,若观察到产生红棕色气体,证明样品中含有亚硝酸钠
C.取样品,加水溶解后,向其中加入 溶液,若观察到出现白色沉淀,则证明有亚硝酸钠
溶液,若观察到出现白色沉淀,则证明有亚硝酸钠
(3)可用适量二氧化氯( )处理鱼塘中过量的亚硝酸钠,
)处理鱼塘中过量的亚硝酸钠, 被还原为
被还原为 ,该反应氧化剂与还原剂的物质的量之比为
,该反应氧化剂与还原剂的物质的量之比为_______ ;若有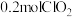 参与反应,则转移电子的数目是
参与反应,则转移电子的数目是_______ 。
(4)某腌制品中亚硝酸钠含量随时间变化如图所示,若要保证在亚硝酸钠含量低于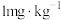 时食用,则三种条件下保存时间最长的是
时食用,则三种条件下保存时间最长的是_______ (填序号)。
 ,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸(
,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸( )是一种弱酸,不稳定,易分解生成NO(无色)气体和
)是一种弱酸,不稳定,易分解生成NO(无色)气体和 (红棕色)气体;
(红棕色)气体; 是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:
是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:(1)人体正常的血红蛋白含有
 ,若误食亚硝酸钠会把
,若误食亚硝酸钠会把 转换为
转换为 而中毒,应立即注射美蓝溶液进行治疗。上述过程中
而中毒,应立即注射美蓝溶液进行治疗。上述过程中 表现出
表现出(2)下列有关检验工业食盐中是否混有亚硝酸钠的说法错误的是
A.取样品,加碘化钾淀粉溶液,酸化后溶液变蓝,说明样品中含有亚硝酸钠
B.取样品,加稀硫酸,若观察到产生红棕色气体,证明样品中含有亚硝酸钠
C.取样品,加水溶解后,向其中加入
 溶液,若观察到出现白色沉淀,则证明有亚硝酸钠
溶液,若观察到出现白色沉淀,则证明有亚硝酸钠(3)可用适量二氧化氯(
 )处理鱼塘中过量的亚硝酸钠,
)处理鱼塘中过量的亚硝酸钠, 被还原为
被还原为 ,该反应氧化剂与还原剂的物质的量之比为
,该反应氧化剂与还原剂的物质的量之比为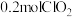 参与反应,则转移电子的数目是
参与反应,则转移电子的数目是(4)某腌制品中亚硝酸钠含量随时间变化如图所示,若要保证在亚硝酸钠含量低于
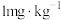 时食用,则三种条件下保存时间最长的是
时食用,则三种条件下保存时间最长的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空
(1)1mol Na2O2固体与水完全反应时转移的电子数_____________ ,反应的离子方程式为________________ 。
(2)工业上由辉铜矿生产铜的主要反应为:Cu2S+O2 2Cu+SO2,该反应中被还原的元素是
2Cu+SO2,该反应中被还原的元素是__________ (填元素符号)。
(3)反应(2)中产生的SO2尾气可用NaOH溶液吸收,若用1L 1mol/L的NaOH溶液吸收标准状况下22.4L SO2,反应的离子方程式为____________ 。
(1)1mol Na2O2固体与水完全反应时转移的电子数
(2)工业上由辉铜矿生产铜的主要反应为:Cu2S+O2
 2Cu+SO2,该反应中被还原的元素是
2Cu+SO2,该反应中被还原的元素是(3)反应(2)中产生的SO2尾气可用NaOH溶液吸收,若用1L 1mol/L的NaOH溶液吸收标准状况下22.4L SO2,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请根据题意填空:
Ⅰ.化学与人类生活、生产密切相关。
(1)钠有多种化合物,其中俗称“纯碱”的是_______ (填“ ”或“
”或“ ”)。
”)。
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是_______ (填“ ”或“
”或“ ”)。
”)。
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式:
_______ 。
Ⅱ.以下是氮循环的一部分:

(4)反应②的化学方程式是_______ 。
(5)NO2易溶于水并和水发生化学反应,该反应中氧化剂和还原剂物质的量之比为_______ 。
(6)实验室收集NO的方法为_______ 。
(7)化合物A的化学式是_______ 。A的稀溶液与铜单质反应的离子方程式为_______ 。
Ⅰ.化学与人类生活、生产密切相关。
(1)钠有多种化合物,其中俗称“纯碱”的是
 ”或“
”或“ ”)。
”)。(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
 ”或“
”或“ ”)。
”)。(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式:

Ⅱ.以下是氮循环的一部分:

(4)反应②的化学方程式是
(5)NO2易溶于水并和水发生化学反应,该反应中氧化剂和还原剂物质的量之比为
(6)实验室收集NO的方法为
(7)化合物A的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有一种矿石,经测定含有镁、硅、氧三种元素且它们的质量比为12∶7∶16。
(1)用盐的组成表示其化学式:___________ 。
(2)用氧化物的组成表示其化学式:_______ 。
(3)该矿石的成分属于________ (填物质的分类)。
(4)写出该矿石(氧化物形式)与盐酸反应的化学方程式:______ 。
(1)用盐的组成表示其化学式:
(2)用氧化物的组成表示其化学式:
(3)该矿石的成分属于
(4)写出该矿石(氧化物形式)与盐酸反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)在SO2、SiO2、Na2O、Na2O2、Fe2O3、Al2O3中,属于碱性氧化物的是______ ;
(2)石英耐高温,可制成石英坩埚,下列试剂可用石英坩埚加热的是________ ;
A.NaOH B.CaCO3 C.Na2CO3 D.KHSO4
(3)奥运金牌“金镶玉”环形碧玉由昆仑玉制成,昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2,则其用氧化物的形式可表示为________________________ ;
(4)治疗胃酸(主要成分为HCl)过多的常用药物有小苏打、胃舒平等。
①请写出小苏打和胃酸反应的离子反应方程式_________________________ ;
②胃舒平主要成分为Al(OH)3,若中和等量的酸,消耗小苏打和Al(OH)3的物质的量之比为___________ 。
(2)石英耐高温,可制成石英坩埚,下列试剂可用石英坩埚加热的是
A.NaOH B.CaCO3 C.Na2CO3 D.KHSO4
(3)奥运金牌“金镶玉”环形碧玉由昆仑玉制成,昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2,则其用氧化物的形式可表示为
(4)治疗胃酸(主要成分为HCl)过多的常用药物有小苏打、胃舒平等。
①请写出小苏打和胃酸反应的离子反应方程式
②胃舒平主要成分为Al(OH)3,若中和等量的酸,消耗小苏打和Al(OH)3的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】碳、硅、锗等碳族元素的单质及化合物广泛应用于我们生活的各个领域。回答下列问题。
(1)锗(Ge)曾被作为半导体材料,其的原子序数为32,则周期表的位置为__________ 。
(2)和田玉成分是Ca2Mg5H2Si8O24,将其用氧化物的形式表示__________ 。
(3)光导纤维在强碱性条件下容易发生“断路”,用离子方程式解释其原因________ 。
(4)水玻璃的主要成分是____ (化学式),是制备硅胶和木材防火剂的原料。
(5)铅为碳族元素中的一种元素,低价铅相对高价铅更稳定,铅的氧化物Pb3O4的氧化性比MnO2更强,请写出Pb3O4与浓盐酸反应的化学方程式____________ 。
(6)在12C、13C、14C、16O、17O、18O微粒中,共有_____ 种原子,属于________ 种元素;组成CO2分子种类有_______ 种。
(1)锗(Ge)曾被作为半导体材料,其的原子序数为32,则周期表的位置为
(2)和田玉成分是Ca2Mg5H2Si8O24,将其用氧化物的形式表示
(3)光导纤维在强碱性条件下容易发生“断路”,用离子方程式解释其原因
(4)水玻璃的主要成分是
(5)铅为碳族元素中的一种元素,低价铅相对高价铅更稳定,铅的氧化物Pb3O4的氧化性比MnO2更强,请写出Pb3O4与浓盐酸反应的化学方程式
(6)在12C、13C、14C、16O、17O、18O微粒中,共有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在 、
、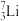 、
、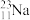 、
、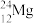 、
、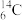 、
、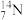 中:
中:
(1)__________ 和__________ 互为同位素;
(2)__________ 和__________ 的质量数相等,但不能互称同位素;
(3)__________ 和__________ 的中子数相等,但质子数不等,所以不是同一种元素
 、
、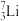 、
、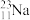 、
、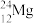 、
、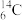 、
、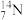 中:
中:(1)
(2)
(3)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】2021年5月15日,“天问一号”探测器成功实现环绕器和着陆巡视器的“两器分离”并成功着陆。“天问一号”采用了我国自主研制的高性能碳化硅增强铝基复合材料。工业上制取碳化硅的化学反应方程式为: ,回答下列问题。
,回答下列问题。
(1)请写出X的化学式___________ 。决定元素种类的微粒是___________ 。
(2)若生成4g碳化硅,生成X气体的体积在标准状况下为___________ L。
(3)从结构层面解释碳化硅材料硬度高的原因___________ 。以下不含共价键的离子晶体是___________ 。
A. 氯化钠 B. 硝酸钾 C. 碳化硅 D. 晶体硅
(4)写出 的电子式
的电子式___________ 。写出 的结构式
的结构式___________ 。
(5)上述材料所涉及元素中,某元素原子核外的M层上有3个电子数,则其离子结构示意图为___________ ;某元素的最外层电子数是其核外电子层数3倍,则其简单离子的电子式为___________ ,请写出与它具有相同电子数的四核微粒的化学式___________
(6)硅元素存在多种同位素。已知三种天然稳定同位素的数据如下:
请列出硅元素的相对原子质量为的计算式___________ 。放射性同位素在实际生活中有许多方面的用途,请列举一条___________ 。
 ,回答下列问题。
,回答下列问题。(1)请写出X的化学式
(2)若生成4g碳化硅,生成X气体的体积在标准状况下为
(3)从结构层面解释碳化硅材料硬度高的原因
A. 氯化钠 B. 硝酸钾 C. 碳化硅 D. 晶体硅
(4)写出
 的电子式
的电子式 的结构式
的结构式(5)上述材料所涉及元素中,某元素原子核外的M层上有3个电子数,则其离子结构示意图为
(6)硅元素存在多种同位素。已知三种天然稳定同位素的数据如下:
| 硅的同位素 | 同位素的相对原子质量 | 自然界中各同位素原子的丰度 |
 | 27.977 | 92.23% |
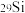 | 28.976 | 4.67% |
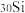 | 29.974 | 3.10% |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在进行有关阿伏加德罗常数(NA)专题分析时常出现以下问题:① 是否考虑同位素原子;② 物质种类是否考虑齐全; ③ 物质能否完全反应;④ 计算所需物理量是否齐全;⑤…以下是同学们在应用中常见的典型错例,请你分析不符合以上哪些原则(填序号)。
(1)足量MnO2与100 mL 12 mol/L浓盐酸反应,产生标况下氯气6.72 L。错误原因___________ 。
(2)1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2 NA。错误原因___________ 。
(3)25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA。错误原因___________ 。
(4)常温常压下,20.0 g重水(D2O)所含的中子数约为8NA。错误原因___________ 。
(1)足量MnO2与100 mL 12 mol/L浓盐酸反应,产生标况下氯气6.72 L。错误原因
(2)1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2 NA。错误原因
(3)25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA。错误原因
(4)常温常压下,20.0 g重水(D2O)所含的中子数约为8NA。错误原因
您最近一年使用:0次



