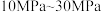在一密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生可逆反应:Ni(s)+4CO(g)  Ni(CO)4(g),已知该反应在25℃、80℃时的平衡常数分别为5×104和2,下列说法正确的是( )
Ni(CO)4(g),已知该反应在25℃、80℃时的平衡常数分别为5×104和2,下列说法正确的是( )
 Ni(CO)4(g),已知该反应在25℃、80℃时的平衡常数分别为5×104和2,下列说法正确的是( )
Ni(CO)4(g),已知该反应在25℃、80℃时的平衡常数分别为5×104和2,下列说法正确的是( )| A.上述生成Ni(CO)4(g)的反应为吸热反应 |
| B.80℃时,测得某时刻Ni(CO)4(g)、CO(g)浓度均为0.5 mol·L-1,则此时v(正)<v(逆) |
| C.恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动 |
| D.恒温恒容下,向容器中再充入少量的Ni(CO)4(g),达到新平衡时CO的百分含量将增大 |
更新时间:2019-12-05 08:52:27
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】温度 时,向容积为2L的密闭容器中加入活性炭(足量)和A,发生反应
时,向容积为2L的密闭容器中加入活性炭(足量)和A,发生反应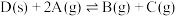 ,第15min时,温度调整到
,第15min时,温度调整到 ,测得下列各时刻A的物质的量如下表所示。反应中没有使用催化剂,下列说法不正确的是
,测得下列各时刻A的物质的量如下表所示。反应中没有使用催化剂,下列说法不正确的是
 时,向容积为2L的密闭容器中加入活性炭(足量)和A,发生反应
时,向容积为2L的密闭容器中加入活性炭(足量)和A,发生反应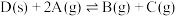 ,第15min时,温度调整到
,第15min时,温度调整到 ,测得下列各时刻A的物质的量如下表所示。反应中没有使用催化剂,下列说法不正确的是
,测得下列各时刻A的物质的量如下表所示。反应中没有使用催化剂,下列说法不正确的是 /℃ /℃ |  /℃ /℃ | ||||||
 | 0 | 5min | 10min | 15min | 20min | 25min | 30min |
 | 2.00 | 1.50 | 1.20 | 1.20 | 0.60 | 0.40 | 0.40 |
A.0~5min,生成B的平均速率为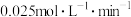 |
B.由表中数据可知 ,且该反应的 ,且该反应的 |
C.其他条件不变,30min时加入B、C各 ,达到新平衡后,A的体积分数不变 ,达到新平衡后,A的体积分数不变 |
D. 、 、 温度下,该反应对应的平衡常数为 温度下,该反应对应的平衡常数为 、 、 ,其大小顺序为 ,其大小顺序为 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在容积为2 L的密闭容器中发生反应xA(g)+yB(g) zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化关系,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化关系,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
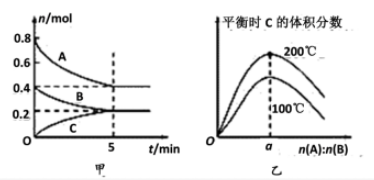
 zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化关系,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化关系,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是 
| A.200℃时,反应从开始到平衡的平均速率v(A)=v(B) |
| B.200℃时,该反应的平衡常数为25 |
| C.当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大 |
D.由图乙可知,反应xA(g)+yB(g) zC(g)的ΔH<0,且a=2 zC(g)的ΔH<0,且a=2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】在体积为2L的密闭容器中,进行如下化学反应: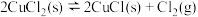 ,其化学平衡常数K和温度的关系如表:
,其化学平衡常数K和温度的关系如表:
根据信息作出的下列判断中正确的是
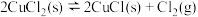 ,其化学平衡常数K和温度的关系如表:
,其化学平衡常数K和温度的关系如表:| T/℃ | 800 | 900 | 1000 | 1100 | 1200 |
| K | 1.1 | 1.5 | 1.75 | 1.90 | 2.08 |
| A.此反应为放热反应 |
B.此反应在1050℃达平衡时, |
| C.1000℃条件下容器体积由2L变为1L,平衡逆向移动,达平衡时Cl2的浓度保持不变 |
| D.降温和加入CuCl固体都能使平衡发生移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】氮化镓(GaN)是一种直接能隙的半导体,是一种用途广泛的新材料。工业上利用Ga与 高温条件下合成。反应方程式为
高温条件下合成。反应方程式为
 。如图,恒温恒容密闭体系内进行上述反应,下列说法正确的是
。如图,恒温恒容密闭体系内进行上述反应,下列说法正确的是
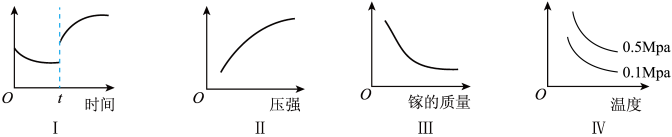
 高温条件下合成。反应方程式为
高温条件下合成。反应方程式为
 。如图,恒温恒容密闭体系内进行上述反应,下列说法正确的是
。如图,恒温恒容密闭体系内进行上述反应,下列说法正确的是
| A.图Ⅰ可以表示催化剂对平衡的影响 |
B.图Ⅱ可以表示压强对平衡时 体积分数的影响 体积分数的影响 |
| C.图Ⅲ可以表示镓的质量对平衡常数的影响 |
| D.图Ⅳ中纵坐标可以为体系内混合气体的密度 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
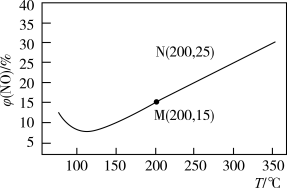
【推荐3】某科研小组研究臭氧氧化-碱吸收法脱除NO工艺,相关反应如下:
①NO(g)+O3(g)=NO2(g)+O2(g)ΔH=-200.9 kJ·mol-1
②2O3(g)=3O2(g) ΔH=-288.8kJ·mol-1
③2NO(g)+O2(g)=2NO2(g) ΔH=akJ·mol-1
已知反应① 正=k正c(NO)·c(O3),
正=k正c(NO)·c(O3), 逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。其它条件不变,每次向反应器中充入0.5molNO和1.0molO3,在不同温度下反应。测得相同时间内,体系中NO的体积分数[φ(NO)]随温度的变化如图所示。下列说法正确的是
逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。其它条件不变,每次向反应器中充入0.5molNO和1.0molO3,在不同温度下反应。测得相同时间内,体系中NO的体积分数[φ(NO)]随温度的变化如图所示。下列说法正确的是
①NO(g)+O3(g)=NO2(g)+O2(g)ΔH=-200.9 kJ·mol-1
②2O3(g)=3O2(g) ΔH=-288.8kJ·mol-1
③2NO(g)+O2(g)=2NO2(g) ΔH=akJ·mol-1
已知反应①
 正=k正c(NO)·c(O3),
正=k正c(NO)·c(O3), 逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。其它条件不变,每次向反应器中充入0.5molNO和1.0molO3,在不同温度下反应。测得相同时间内,体系中NO的体积分数[φ(NO)]随温度的变化如图所示。下列说法正确的是
逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。其它条件不变,每次向反应器中充入0.5molNO和1.0molO3,在不同温度下反应。测得相同时间内,体系中NO的体积分数[φ(NO)]随温度的变化如图所示。下列说法正确的是
| A.a=113 |
B.升高温度,k正、k逆增大, 减小 减小 |
| C.延长反应时间,可使φ(NO)由M点移到N点 |
| D.用碱液吸收、增大反应器的容积均可提高NO的转化率 |
您最近半年使用:0次

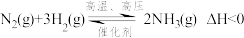 ,在合成氨工业中常采取的下列措施不能用勒夏特列原理来解释的是
,在合成氨工业中常采取的下列措施不能用勒夏特列原理来解释的是