一定温度下,在三个体积均为2.0 L的恒容密闭容器中发生反应:PCl5(g)⇌PCl3(g)+Cl2(g)。
下列说法正确的是
| 编号 | 温度 /℃ | 起始物质 的量/mol | 平衡物质 的量/mol | 达到平衡 所需时间/s | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t |
| Ⅱ | 320 | 0.80 | t1 | ||
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t2 |
| A.平衡常数K:容器Ⅱ>容器Ⅲ |
| B.反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ |
C.反应到达平衡时,容器Ⅰ中的平均速率为v(PCl5)=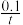 mol·L-1·s-1 mol·L-1·s-1 |
| D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl3 0.45 mol和Cl2 0.10 mol,则反应将向逆反应方向进行 |
14-15高三·江苏南通·阶段练习 查看更多[20]
河南省新蔡县第一高级中学2021-2022学年高二上学期9月月考化学试题黑龙江省哈尔滨市师大附中2020-2021学年高二上学期期末考试化学试题(已下线)考点10 化学平衡常数及其图象分析-2020年高考化学命题预测与模拟试题分类精编2019年秋高三化学复习强化练习—— 等效平衡河北省承德第一中学2020届高三上学期第三次月考化学试题黑龙江省安达市第七中学2020届高三上学期第二次模拟考试化学试题黑龙江省顶级名校2020届高三上学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2020届高三上学期期中考试化学试题安徽省师范大学附中2019-2020学年高二上学期期中考试化学试题湖南省师范大学附属中学2016-2017学年高二(理科)上学期期末考试化学试题安徽省江淮名校2017-2018学年高二期中考试化学试题安徽师范大学附属中学2017-2018学年高二上学期10月月考化学试题2018届高三一轮复习化学:微考点57-全面破解平衡常数2017届陕西省黄陵中学高三上学期第三次质检化学试卷2017届江苏省苏州市高三上学期期初调研化学试卷2016届福建省龙岩市上杭一中高三上学期12月月考化学试卷2016届福建省上杭县第一中学高三上12月月考化学试卷2016届江苏省清江中学高三第四次(12月)月考化学试卷2016届江苏省无锡市青山高级中学高三上学期10月月考化学试卷2015届江苏省南通市高三第一次模拟化学试卷
更新时间:2019-12-05 19:39:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述不正确的是
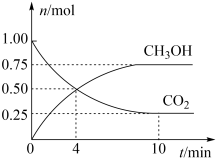

| A.达到平衡时,H2的转化率为75% |
| B.3 min 时,CH3OH和CO2的浓度相等,达到了化学平衡状态 |
| C.反应进行到10 min时,CO2的正逆反应速率相等,反应达到化学平衡 |
| D.反应开始到10 min,用CO2表示的反应速率为0.0375 mol·L-1·min-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
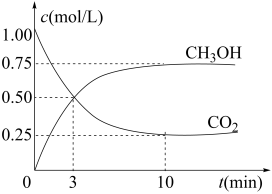
【推荐2】把1 molCO2和3 molH2通入1 L的密闭容器中,在某温度下发生反应:CO2(g) +3H2(g)  CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1 。测得 CO2和CH3OH 的浓度随时间的变化如图所示,下列说法正确的是
CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1 。测得 CO2和CH3OH 的浓度随时间的变化如图所示,下列说法正确的是
 CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1 。测得 CO2和CH3OH 的浓度随时间的变化如图所示,下列说法正确的是
CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1 。测得 CO2和CH3OH 的浓度随时间的变化如图所示,下列说法正确的是
| A.3 min 时,V正=V 逆 |
| B.0~10 min内,H2的平均反应速率为2. 25 mol • L-l • min-1 |
| C.该温度下,反应的平衡常数K=5.3 |
| D.若升高温度,则CO2的转化率大于75% |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】将1 mol X和3 mol Y在2 L的恒容密闭容器中混合,一定条件下发生反应X(s)+3Y(g) 2Z(g),10 min时测得Y的物质的量为2.4 mol。下列说法正确的是
2Z(g),10 min时测得Y的物质的量为2.4 mol。下列说法正确的是
 2Z(g),10 min时测得Y的物质的量为2.4 mol。下列说法正确的是
2Z(g),10 min时测得Y的物质的量为2.4 mol。下列说法正确的是| A.10 min内,X的平均反应速率为0.01 mol·L-1·min-1 |
| B.第10 min时,Y的反应速率为0.03 mol·L-1·min-1 |
| C.10 min时, X的转化率为20% |
| D.反应时,向容器中通入He,容器内压强增大,反应速率加快 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
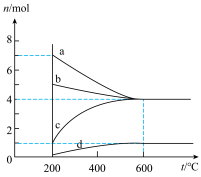
【推荐1】在2L恒容密闭容器中,加入8mol 和5mol
和5mol ,发生反应
,发生反应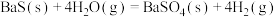 ,在不同温度下达平衡时,各组分的物质的量(n)如图所示。下列说法正确的是
,在不同温度下达平衡时,各组分的物质的量(n)如图所示。下列说法正确的是
 和5mol
和5mol ,发生反应
,发生反应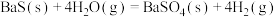 ,在不同温度下达平衡时,各组分的物质的量(n)如图所示。下列说法正确的是
,在不同温度下达平衡时,各组分的物质的量(n)如图所示。下列说法正确的是
A.该反应的 |
| B.c为BaS的物质的量随温度的变化曲线 |
C.向平衡体系中加入 ,平衡逆向移动 ,平衡逆向移动 |
| D.600℃时,该反应的平衡常数为1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】丙酮是重要的有机合成原料,可以由过氧化氢异丙苯合成。其反应为: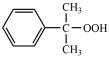
 CH3COCH3+
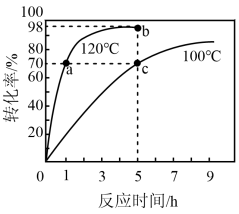
CH3COCH3+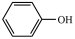 ,为了提高过氧化氢异丙苯的转化率,反应进行时需及时从溶液体系中移出部分苯酚。过氧化氢异丙苯的转化率随反应时间的变化如图所示。设过氧化氢异丙苯的初始浓度为 x mol·L-1,反应过程中的液体体积变化忽略不计。下列说法正确的是
,为了提高过氧化氢异丙苯的转化率,反应进行时需及时从溶液体系中移出部分苯酚。过氧化氢异丙苯的转化率随反应时间的变化如图所示。设过氧化氢异丙苯的初始浓度为 x mol·L-1,反应过程中的液体体积变化忽略不计。下列说法正确的是

 CH3COCH3+
CH3COCH3+ ,为了提高过氧化氢异丙苯的转化率,反应进行时需及时从溶液体系中移出部分苯酚。过氧化氢异丙苯的转化率随反应时间的变化如图所示。设过氧化氢异丙苯的初始浓度为 x mol·L-1,反应过程中的液体体积变化忽略不计。下列说法正确的是
,为了提高过氧化氢异丙苯的转化率,反应进行时需及时从溶液体系中移出部分苯酚。过氧化氢异丙苯的转化率随反应时间的变化如图所示。设过氧化氢异丙苯的初始浓度为 x mol·L-1,反应过程中的液体体积变化忽略不计。下列说法正确的是
| A.a、c两点丙酮的物质的量浓度:c(a)>c(c) |
| B.b、c两点的逆反应速率:v(b)<v(c) |
| C.100℃时,0~5h之间丙酮的平均反应速率为0.14 x mol·L-1·h-1 |
D.若b点处于化学平衡,则120℃时反应的平衡常数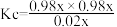 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如表所示:
下列说法错误的是
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
A.反应可表示为X(g)+3Y(g) 2Z(g),反应前后压强之比为2:3 2Z(g),反应前后压强之比为2:3 |
| B.反应达到平衡时,X的转化率为50% |
| C.平衡常数为1600,改变温度可以改变此反应的平衡常数 |
| D.X、Y、Z三种气体的初始浓度(单位mol·L-1)分别为0.2、0.4、0.2时υ(正)>υ(逆) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
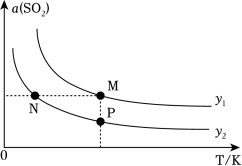
【推荐1】一定压强下,对于反应2CO(g)+SO2(g)⇌S(l)+2CO2(g)ΔH,SO2的平衡转化率[α(SO2)]与投料比的比值[ ]、温度(T)的关系如图所示。下列说法正确的是
]、温度(T)的关系如图所示。下列说法正确的是
 ]、温度(T)的关系如图所示。下列说法正确的是
]、温度(T)的关系如图所示。下列说法正确的是
| A.ΔH>0 | B.温度相同时,y1>y2 |
| C.CO的平衡转化率:N<M | D.逆反应速率:N>P |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】一定温度下,把 2.5molA 和 2.5molB 混合盛入容积为 2L 的密闭容器里,发生如下反应:3A(g)+B(s)⇌xC(g)+2D(g),经 5s 反应达平衡,在此 5s 内 C 的平均反应速率为 0.2mol·L-1·s-1,同时生成 1molD,下列叙述中不正确的是
| A.反应达到平衡状态时A的转化率为 60% |
| B.x=3 |
| C.若混合气体的密度不再变化,则该可逆反应达到化学平衡状态 |
| D.反应达到平衡状态时,相同条件下容器内气体的压强与起始时压强比为8∶5 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】在恒容条件下发生反应A(g)+3B(g)⇌2 C(g)(△H<0),改变其他反应条件,在Ⅰ、Ⅱ阶段体系中各物质浓度随时间变化的曲线如下图所示,下列说法中正确的是


| A.第Ⅰ阶段用C表示的平衡前的反应速率υ (C)=0.1 mol/(L·s) |
| B.第Ⅱ阶段中B的平衡转化率αⅡ(B)为0.019 |
| C.第Ⅰ阶段的平衡常数KⅠ与第Ⅱ阶段平衡常数KⅡ的大小关系是:KⅠ﹤KⅡ |
| D.由第一次平衡到第二次平衡,可能采取的措施是从反应体系中移出产物C |
您最近半年使用:0次
单选题
|
适中
(0.65)
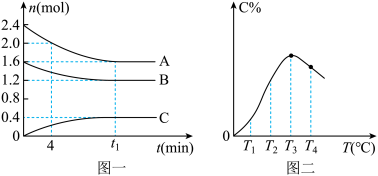
【推荐2】在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系。一定条件下,A、B、C三种物质物质的量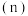 与时间
与时间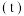 的关系如图一所示,C的百分含量
的关系如图一所示,C的百分含量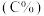 与温度
与温度 的关系如图二所示。下列分析错误的是
的关系如图二所示。下列分析错误的是
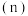 与时间
与时间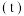 的关系如图一所示,C的百分含量
的关系如图一所示,C的百分含量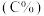 与温度
与温度 的关系如图二所示。下列分析错误的是
的关系如图二所示。下列分析错误的是
A. 时,A的平均反应速率为 时,A的平均反应速率为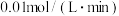 |
B.图二中 、 、 对应曲线上的点都处于化学平衡状态 对应曲线上的点都处于化学平衡状态 |
C.由 向 向 变化时, 变化时, |
| D.该反应的正反应为吸热反应 |
您最近半年使用:0次

 催化加氢制甲醇,在减少
催化加氢制甲醇,在减少 ,保持起始反应物
,保持起始反应物 ,
, 时
时 随压强变化的曲线和
随压强变化的曲线和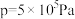 时
时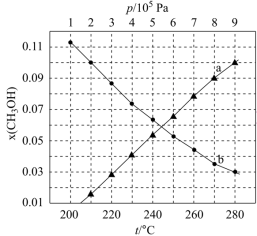
 时,达平衡后
时,达平衡后
 时,
时,


