化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
I.摩擦剂中氢氧化铝的定性检验取适量牙膏样品,加水充分搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是________ 。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是_______ 。
II.牙膏样品中碳酸钙的定量测定
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
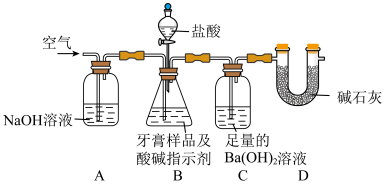
依据实验过程回答下列问题:
(3)D装置的作用是__________ 。
(4)下列各项措施中,不能提高测定准确度的是__________ (填标号)。
①在加入盐酸之前,应排净装置内的CO2气体
②滴加盐酸不宜过快
③在A-B之间增添盛有浓H2SO4的洗气装置
④在B-C之间增添盛有饱和NaHCO3溶液的洗气装置
(5)实验中准确称取10.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为__________ 。
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
I.摩擦剂中氢氧化铝的定性检验取适量牙膏样品,加水充分搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是
II.牙膏样品中碳酸钙的定量测定
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(3)D装置的作用是
(4)下列各项措施中,不能提高测定准确度的是
①在加入盐酸之前,应排净装置内的CO2气体
②滴加盐酸不宜过快
③在A-B之间增添盛有浓H2SO4的洗气装置
④在B-C之间增添盛有饱和NaHCO3溶液的洗气装置
(5)实验中准确称取10.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为
更新时间:2019-12-10 16:42:22
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】联合国大会将2019年定为“化学元素周期表国际年”,表明了元素周期律的重要性。以下短周期主族元素中,含元素a的化合物被广泛用于制作手机电池,古迪纳夫因在该领域做出了杰出贡献荣获2019年诺贝尔化学奖。
(1)a原子结构示意图为___________ 。
(2)元素g的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为___________ 。
(3)由单质a制成的电池需要注意防水,其原因用化学反应方程式表示为___________ 。
(4)科学家在研究元素周期表时,预言了在元素h的下一周期存在一种“类h”元素,该元素多年后被德国化学家文克勒发现,命名为锗(Ge),锗在周期表的位置为___________ 。
(5)已知c与氢元素能组成生活中最常见的化合物X。一定条件下,铁能与气态X发生反应,该反应的化学方程式为___________ 。
(6)2016年IUPAC确认了四种新元素,其中一种为Mc,中文为“镆”、Mc可由反应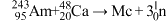 得到。Mc用核素符号表示为
得到。Mc用核素符号表示为___________ 。
| a | b | c | d | ||||
| e | g | h | j |
(2)元素g的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为
(3)由单质a制成的电池需要注意防水,其原因用化学反应方程式表示为
(4)科学家在研究元素周期表时,预言了在元素h的下一周期存在一种“类h”元素,该元素多年后被德国化学家文克勒发现,命名为锗(Ge),锗在周期表的位置为
(5)已知c与氢元素能组成生活中最常见的化合物X。一定条件下,铁能与气态X发生反应,该反应的化学方程式为
(6)2016年IUPAC确认了四种新元素,其中一种为Mc,中文为“镆”、Mc可由反应
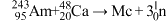 得到。Mc用核素符号表示为
得到。Mc用核素符号表示为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】某无色稀溶液X中,可能含有下表所列离子中的一种或几种。
现取适量该溶液于锥形瓶中,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。

回答下列问题:
(1)仅通过观察颜色,可以判断溶液X中一定不存在的离子是_______ (用化学用语表示)。
(2)若Y是盐酸,则Oa段生成的沉淀为_______ (填化学式);ab段发生反应的离子为_______ (用化学用语表示),bc段发生反应的离子方程式为_______ ;取少量d点对应的上层清液于试管中,加入几滴硝酸银溶液,有白色沉淀生成,不能证明溶液X中含有 ,原因是
,原因是_______ 。
(3)若Y是NaOH溶液,则X中一定含有的离子是_______ ;ab段反应的离子方程式为_______ 。
| 阴离子 |  、 、 、 、 、 、 |
| 阳离子 |  、 、 、 、 、 、 、 、 |

回答下列问题:
(1)仅通过观察颜色,可以判断溶液X中一定不存在的离子是
(2)若Y是盐酸,则Oa段生成的沉淀为
 ,原因是
,原因是(3)若Y是NaOH溶液,则X中一定含有的离子是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
(1)在⑤~⑧元素中,原子半径最大的是______ (填元素符号,下同),非金属性最强的元素是______
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有______ 。
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:______ 。
(4)③、⑤、⑧所形成的离子,其半径由小到大的顺序是______ (填离子符号)。
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是______ (填物质化学式);呈两性的氢氧化物是______ (填物质化学式),该化合物与NaOH溶液反应的离子方程式为______ 。
(6)表中元素⑦和氢元素可形成一种相对分子质量为32的化合物Y,⑧与氢元素按原子个数比1:1形成的化合物X,X与Y发生氧化还原反应,生成⑦单质和⑧的另一种氢化物,写出该反应的化学方程式______ 。
(7)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
①由镓的性质推知,镓与铝同主族,且位于铝的下一周期。试从原子结构的角度解释镓与铝性质相似的原因______ 。冶炼金属镓通常采用的方法是______ 。
②为判断Ga(OH)3是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、______ 和______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:
(4)③、⑤、⑧所形成的离子,其半径由小到大的顺序是
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(6)表中元素⑦和氢元素可形成一种相对分子质量为32的化合物Y,⑧与氢元素按原子个数比1:1形成的化合物X,X与Y发生氧化还原反应,生成⑦单质和⑧的另一种氢化物,写出该反应的化学方程式
(7)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
①由镓的性质推知,镓与铝同主族,且位于铝的下一周期。试从原子结构的角度解释镓与铝性质相似的原因
②为判断Ga(OH)3是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】雾霾严重影响人们的生活与健康,某地区的雾霾中可能含有如下离子中的一种或多种:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。某同学收集了该地区的雾霾,经预处理得试样溶液,设计并完成了如下的实验:
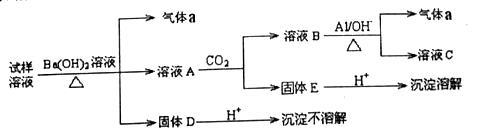
(已知;气体a能使湿润的红色石蕊试纸变蓝色,所用试剂均过量)
回答下列问题:
(1)固体E的化学式是_______________ 。
(2)该试样中肯定存在的离子有_____________ 可能存在的离子有_____________ .若要进一步验证其中的阳离子是否存在应选用的实验操作为_____________
(3)上述实验过程多次用到过滤操作,该操作需要的玻璃仪器有_____________
(4)写出上述实验过程中生成气体a 的离子方程式:
①_________________ ②_____________

(已知;气体a能使湿润的红色石蕊试纸变蓝色,所用试剂均过量)
回答下列问题:
(1)固体E的化学式是
(2)该试样中肯定存在的离子有
(3)上述实验过程多次用到过滤操作,该操作需要的玻璃仪器有
(4)写出上述实验过程中生成气体a 的离子方程式:
①
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】物质A—J间的转化关系如下图所示,A、C为金属氧化物,其中A为红棕色粉末,B、D是生活中常见金属单质,F、J是难溶于水的白色化合物,G、J受热后容易分解
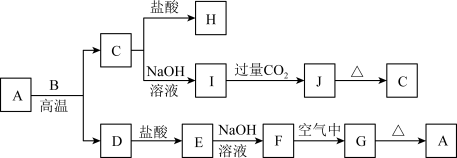
(1)A的化学式是_________ ,A与B反应的反应类型是________ (填四大基本反应类型)。
(2)I→J反应的离子方程式是___________________________________________ 。
(3)F转化为G的过程中观察到的现象是__________ ,反应的化学方程式是____________ 。

(1)A的化学式是
(2)I→J反应的离子方程式是
(3)F转化为G的过程中观察到的现象是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】利用硫铁矿烧渣(主要成分为 、
、 、
、 等)和粉煤灰(主要成分为
等)和粉煤灰(主要成分为 、
、 、
、 等),制备高效水处理剂聚合硫酸铁铝的流程如下:
等),制备高效水处理剂聚合硫酸铁铝的流程如下:
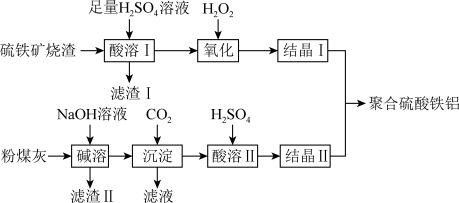
已知: 既不溶于
既不溶于 溶液,也不和
溶液,也不和 溶液反应。
溶液反应。
(1)“酸溶Ⅰ”得到的溶液中,阳离子主要有___________ 。
(2)“氧化”时,若用氯水代替 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ ;与使用氯水相比,“氧化”时使用 的优点是
的优点是___________ 。
(3)“碱溶”的目的是___________ ;通入 后生成沉淀的化学式为
后生成沉淀的化学式为___________ 。
(4)在流程中可以循环利用的是___________ (填“滤渣Ⅰ”、“滤渣Ⅱ”或“滤渣Ⅰ和滤渣Ⅱ”)。
(5)向 、
、 的固体混合物中,加入足量
的固体混合物中,加入足量 溶液,充分反应后,向溶液中再加入足量铜粉,充分搅拌反应,得到的溶液中
溶液,充分反应后,向溶液中再加入足量铜粉,充分搅拌反应,得到的溶液中 ,则固体混合物中
,则固体混合物中 为
为___________ 。
 、
、 、
、 等)和粉煤灰(主要成分为
等)和粉煤灰(主要成分为 、
、 、
、 等),制备高效水处理剂聚合硫酸铁铝的流程如下:
等),制备高效水处理剂聚合硫酸铁铝的流程如下:
已知:
 既不溶于
既不溶于 溶液,也不和
溶液,也不和 溶液反应。
溶液反应。(1)“酸溶Ⅰ”得到的溶液中,阳离子主要有
(2)“氧化”时,若用氯水代替
 ,发生反应的离子方程式为
,发生反应的离子方程式为 的优点是
的优点是(3)“碱溶”的目的是
 后生成沉淀的化学式为
后生成沉淀的化学式为(4)在流程中可以循环利用的是
(5)向
 、
、 的固体混合物中,加入足量
的固体混合物中,加入足量 溶液,充分反应后,向溶液中再加入足量铜粉,充分搅拌反应,得到的溶液中
溶液,充分反应后,向溶液中再加入足量铜粉,充分搅拌反应,得到的溶液中 ,则固体混合物中
,则固体混合物中 为
为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】苯甲酸为白色片状晶体,熔点122.4℃,苯甲酸是常用的食品防腐剂。苯甲酸在水中的溶解度为:
实验室有混有杂质(杂质为:泥沙和少量可溶性杂质)的粗苯甲酸,用下列实验方法可以分离得到纯净的苯甲酸晶体,实验步骤为:
A.将粗苯甲酸1 g加到100 mL的烧杯中,再加入50 mL蒸馏水,
B._______,全溶后再加入少量蒸馏水。
C.使用短颈漏斗(下端玻璃管短的漏斗)趁热将溶液过滤到另一100 mL烧杯中
D.将滤液静置,使其缓慢冷却结晶,滤出晶体
回答下列问题:
(1)上述步骤中有两次过滤操作,过滤用到的玻璃仪器有_______ 。
(2)步骤D中,需要洗涤晶体,洗涤步骤为:向过滤器中注入_______ (填“冷水”或“热水”)至浸没沉淀,使洗涤液自然流下,重复操作2~3次。
(3)步骤B横线上的实验操作为_______ 。
(4)步骤B中“全溶后再加入少量蒸馏水”和步骤C中“短颈漏斗”的作用是一样的,其目的是_______ 。
(5)温度越低,苯甲酸的溶解度越小,但结晶时的温度并不是越低越好,请分析原因_______ 。
| 25℃ | 50℃ | 100℃ |
| 0.344 g | 0.849 g | 6.8 g |
A.将粗苯甲酸1 g加到100 mL的烧杯中,再加入50 mL蒸馏水,
B._______,全溶后再加入少量蒸馏水。
C.使用短颈漏斗(下端玻璃管短的漏斗)趁热将溶液过滤到另一100 mL烧杯中
D.将滤液静置,使其缓慢冷却结晶,滤出晶体
回答下列问题:
(1)上述步骤中有两次过滤操作,过滤用到的玻璃仪器有
(2)步骤D中,需要洗涤晶体,洗涤步骤为:向过滤器中注入
(3)步骤B横线上的实验操作为
(4)步骤B中“全溶后再加入少量蒸馏水”和步骤C中“短颈漏斗”的作用是一样的,其目的是
(5)温度越低,苯甲酸的溶解度越小,但结晶时的温度并不是越低越好,请分析原因
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】三氯化硼(BCl3)是一种重要的化工原料。实验室制备BCl3的原理B2O3+3C+3Cl2 2BCl3+3CO,某实验小组利用干燥的氯气和下列装置(装置可重复使用)制备BCl3并验证反应中有CO生成。(已知:BCl3的熔点为-107.3℃,沸点为12.5℃;硝基苯的密度比水大)。请回答下列问题:
2BCl3+3CO,某实验小组利用干燥的氯气和下列装置(装置可重复使用)制备BCl3并验证反应中有CO生成。(已知:BCl3的熔点为-107.3℃,沸点为12.5℃;硝基苯的密度比水大)。请回答下列问题:
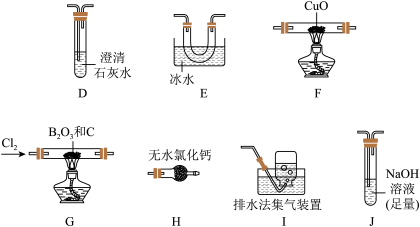
实验Ⅰ:制备BCl3并验证产物CO
(1)该实验装置中合理的连接顺序为G→______ →______ →______ →______ →F→D→I;其中装置E的作用是______ 。
(2)BCl3接触潮湿空气时会形成白雾,请写出该反应的化学方程式______ 。
(3)能证明反应中有CO生成的现象是______ 。
实验Ⅱ:产品中氯含量的测定
①准确称取少许m g产品,置于蒸馏水中完全水解,并配成100 mL溶液。
②取10.00 mL溶液于锥形瓶中
③加入V1 mL浓度为c1mol/L AgNO3溶液使氯离子完全沉淀;向其中加入少许硝基苯用力摇动。
④以硝酸铁为指示剂,用c2 mol/LKSCN标准溶液滴定过量的AgNO3溶液。重复步骤②~④二次,达到滴定终点时用去KSCN溶液的平均体积为V2 mL。
已知:Ksp(AgCl)>Ksp(AgSCN)。
(4)步骤②移取溶液时所需仪器名称为______ ,步骤④中达到滴定终点的现象为______ 。
(5)产品中氯元素的质量分数为______ 。
(6)下列操作,可能引起测得产品中氯含量偏高是______ 。
A.步骤③中未加硝基苯
B.步骤①中配制100 mL溶液时,定容时俯视刻度线
C.用KSCN溶液滴定剩余AgNO3溶液时,滴定前有气泡,滴定后无气泡
D.滴定剩余AgNO3溶液时,KSCN溶液滴到锥形瓶外面一滴
 2BCl3+3CO,某实验小组利用干燥的氯气和下列装置(装置可重复使用)制备BCl3并验证反应中有CO生成。(已知:BCl3的熔点为-107.3℃,沸点为12.5℃;硝基苯的密度比水大)。请回答下列问题:
2BCl3+3CO,某实验小组利用干燥的氯气和下列装置(装置可重复使用)制备BCl3并验证反应中有CO生成。(已知:BCl3的熔点为-107.3℃,沸点为12.5℃;硝基苯的密度比水大)。请回答下列问题:
实验Ⅰ:制备BCl3并验证产物CO
(1)该实验装置中合理的连接顺序为G→
(2)BCl3接触潮湿空气时会形成白雾,请写出该反应的化学方程式
(3)能证明反应中有CO生成的现象是
实验Ⅱ:产品中氯含量的测定
①准确称取少许m g产品,置于蒸馏水中完全水解,并配成100 mL溶液。
②取10.00 mL溶液于锥形瓶中
③加入V1 mL浓度为c1mol/L AgNO3溶液使氯离子完全沉淀;向其中加入少许硝基苯用力摇动。
④以硝酸铁为指示剂,用c2 mol/LKSCN标准溶液滴定过量的AgNO3溶液。重复步骤②~④二次,达到滴定终点时用去KSCN溶液的平均体积为V2 mL。
已知:Ksp(AgCl)>Ksp(AgSCN)。
(4)步骤②移取溶液时所需仪器名称为
(5)产品中氯元素的质量分数为
(6)下列操作,可能引起测得产品中氯含量偏高是
A.步骤③中未加硝基苯
B.步骤①中配制100 mL溶液时,定容时俯视刻度线
C.用KSCN溶液滴定剩余AgNO3溶液时,滴定前有气泡,滴定后无气泡
D.滴定剩余AgNO3溶液时,KSCN溶液滴到锥形瓶外面一滴
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室利用SO2合成硫酰氯(SO2Cl2),并对H2SO3和HClO的酸性强弱进行探究。
I.磺酰氯(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2在活性炭作用下反应,制取少量的SO2Cl2,SO2(g)+Cl2(g)=SO2Cl2(l),该反应放热,装置如图所示(部分夹持装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈反应,并产生白雾。
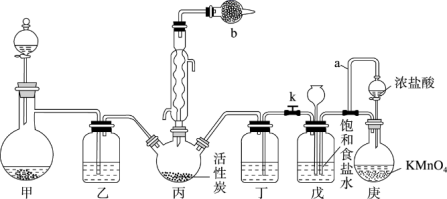
回答下列问题。
(1)甲装置可以用于实验室制SO2,则下列试剂组合中合适的是___________ 。
A.18.4 mol·L-1的硫酸和Cu
B.10 mol·L-1的硝酸和Na2SO3固体
C.70%的硫酸和Na2SO3固体
(2)导管a的作用是___________ 。仪器b盛放的试剂为___________ ,其作用是___________ ,装置乙和丁中可以使用同一种试剂,该试剂为___________ 。
(3)实验结束时,关闭分液漏斗活塞和止水夹k,此时装置戊的作用是___________ 。
(4)若反应中消耗的氯气体积为896 mL(已转化为标准状况,SO2足量),最后得到纯净的磺酰氯4.05 g,则磺酰氯的产率为___________ (保留两位有效数字)。(产率: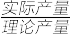 ×100%)
×100%)
II.(5)选用下面的装置探究酸性:H2SO3>HClO,其连接顺序为A→___________ 。能证明H2SO3的酸性强于HClO的实验现象为___________ 。
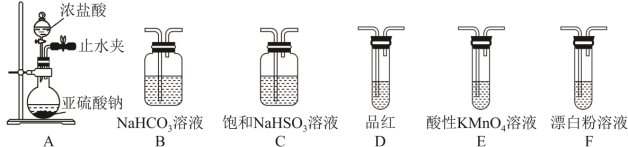
I.磺酰氯(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2在活性炭作用下反应,制取少量的SO2Cl2,SO2(g)+Cl2(g)=SO2Cl2(l),该反应放热,装置如图所示(部分夹持装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈反应,并产生白雾。

回答下列问题。
(1)甲装置可以用于实验室制SO2,则下列试剂组合中合适的是
A.18.4 mol·L-1的硫酸和Cu
B.10 mol·L-1的硝酸和Na2SO3固体
C.70%的硫酸和Na2SO3固体
(2)导管a的作用是
(3)实验结束时,关闭分液漏斗活塞和止水夹k,此时装置戊的作用是
(4)若反应中消耗的氯气体积为896 mL(已转化为标准状况,SO2足量),最后得到纯净的磺酰氯4.05 g,则磺酰氯的产率为
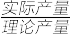 ×100%)
×100%)II.(5)选用下面的装置探究酸性:H2SO3>HClO,其连接顺序为A→

您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】NOCl(亚硝酰氯)是有机物合成中的重要试剂,对眼睛、皮肤和黏膜有强烈刺激性,沸点为-5.5℃,常温下是一种黄色气体,其液体呈红褐色,遇水和潮气快速反应:2NOCl+H2O=2HCl+NO↑+NO2↑,某化学兴趣小组利用以下仪器制备NOCl(Cl2+2NO=2NOCl,该反应为放热反应)。

回答下列相关问题:
(1)装置F中,合成NOCl仪器的名称为_______ ,装置A、E中,X的作用是_______ 。
(2)按气流的方向,上述仪器的连接顺序为a→_______ →j,l←_______ ←h,k→_______ (仪器可重复使用);实验开始后,先打开装置A中分液漏斗的活塞,当F中_______ (填现象),再打开装置E分液漏斗的活塞,这样做的目的是_______ ,装置F处在冰盐水水浴中的目的是_______ 。
(3)装置G中吸收尾气时,NOCl发生反应的化学方程式为_______ 。
(4)查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为_______ 。
(5)测定产品中NOCl纯度,其步骤如下所示:
步骤1:取装置F中mg产品,溶于水,配制成250mL溶液,准确量取25.00mL溶液于250mL锥形瓶中;
步骤2:用cmol·L-1AgNO3溶液与步骤1锥形瓶中液体恰好完全反应,消耗AgNO3溶液的体积为VmL;
则产品中NOCl纯度的计算式为_______ 。

回答下列相关问题:
(1)装置F中,合成NOCl仪器的名称为
(2)按气流的方向,上述仪器的连接顺序为a→
(3)装置G中吸收尾气时,NOCl发生反应的化学方程式为
(4)查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为
(5)测定产品中NOCl纯度,其步骤如下所示:
步骤1:取装置F中mg产品,溶于水,配制成250mL溶液,准确量取25.00mL溶液于250mL锥形瓶中;
步骤2:用cmol·L-1AgNO3溶液与步骤1锥形瓶中液体恰好完全反应,消耗AgNO3溶液的体积为VmL;
则产品中NOCl纯度的计算式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】某研究小组根据文献模拟利用氨浸法从某钢铁厂烟灰(主要成分为ZnO,并含有少量的CuO、Fe2O3等)中制备碱式碳酸锌,并测定其组成的流程如下:
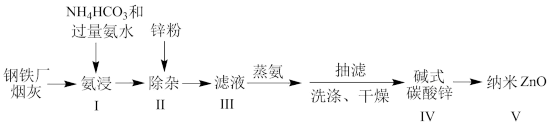
已知:a、碱式碳酸锌白色粉末,难溶于水和乙醇,微溶于氨;
纳米氧化锌具有极强的吸附性,空气中久置容易变质。
b、ZnO+2NH3+2 →Zn(NH3)
→Zn(NH3) +H2O
+H2O
Zn(NH3) →Zn2++4NH3
→Zn2++4NH3
Zn2++2OH-→Zn(OH)2↓
Zn2++ →ZnCO3↓
→ZnCO3↓
(1)“氨浸”时加入过量氨水的目的:
①使HCO 转化为
转化为 :
:
②_______ 。
(2)下列说法不正确的是_______。
(3)I、该研究小组利用步骤V对碱式碳酸锌[Zn3(OH)m(CO3)n(其中m。n为整数)]组成进行测定,从下列选项中选出合理的操作并排序:坩埚预处理后将样品放入坩埚中称量,再置于高温炉中加热→_______→_______→_______→_______→_______。_______
①放在石棉网上
②放在干燥器中
③冷却至室温
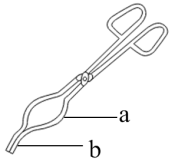
④用如图坩埚钳a处夹取坩埚
⑤用如图坩埚钳b处夹取坩埚⑥放入电子天平中称量
⑦重复以上操作,确认最后两次称量值差≦0.001g
II、电子天平记录的部分数据如下表所示
①根据数据计算该碱式碳酸锌的化学式_______ 。
②写出蒸氨步骤制得该碱式碳酸锌的离子方程式_______ 。

已知:a、碱式碳酸锌白色粉末,难溶于水和乙醇,微溶于氨;
纳米氧化锌具有极强的吸附性,空气中久置容易变质。
b、ZnO+2NH3+2
 →Zn(NH3)
→Zn(NH3) +H2O
+H2OZn(NH3)
 →Zn2++4NH3
→Zn2++4NH3Zn2++2OH-→Zn(OH)2↓
Zn2++
 →ZnCO3↓
→ZnCO3↓(1)“氨浸”时加入过量氨水的目的:
①使HCO
 转化为
转化为 :
:②
(2)下列说法不正确的是_______。
| A.步骤I可以采用加热方式来加快浸出速率,提高浸出量 |
| B.步骤II过滤得到的滤渣中含有Cu、Fe、Zn |
| C.步骤III蒸氨过程产生气体除了氨气还有CO2,冷凝后得到的碳化氨水循环用于氨浸 |
| D.步骤IV洗涤时可先用浓氨水洗涤,减少固体溶解,再用无水乙醇洗涤 |

①放在石棉网上
②放在干燥器中
③冷却至室温
④用如图坩埚钳a处夹取坩埚
⑤用如图坩埚钳b处夹取坩埚⑥放入电子天平中称量
⑦重复以上操作,确认最后两次称量值差≦0.001g
II、电子天平记录的部分数据如下表所示
| 电子天平视数/g | |
| 空坩埚 | 19.2500 |
| 空坩埚+样品 | 25.7100 |
| 第一次灼烧后称量 | 24.3251 |
| 第二次灼烧后称量 | 24.1414 |
| 第三次灼烧后称量 | 24.1101 |
| 第四次灼烧后称量 | 24.1100 |
| 第五次灼烧后称量 | 24.1099 |
②写出蒸氨步骤制得该碱式碳酸锌的离子方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,实验班的某同学设计如图实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组分的质量分数。(提示固体干燥剂主要有:碱石灰、无水CaCl2、P2O5等)
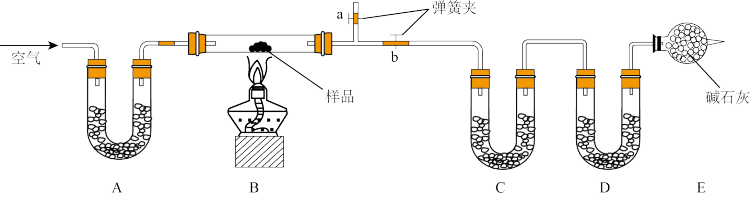
(1)装置A、C中盛放的试剂分别为A__ ,C___ 。
(2)E装置的作用是__ ,若无该装置,则测定结果中NaHCO3的含量将___ (填“偏高”、“偏低”或“无影响”,下同);若B中反应管右侧有水蒸气冷凝,则测定结果中NaHCO3的含量将___ 。
(3)若样品质量为wg,反应后C、D增加的质量分别为m1g、m2g,由此可知混合物中NaHCO3质量分数为___ (用含w、m1g、m2g的代数式表示)

(1)装置A、C中盛放的试剂分别为A
(2)E装置的作用是
(3)若样品质量为wg,反应后C、D增加的质量分别为m1g、m2g,由此可知混合物中NaHCO3质量分数为
您最近半年使用:0次



