锌是人体必需的微量元素,明朝《天工开物》中有世界上最早的关于炼锌技术的记载。回答下列问题:
(1)基态Zn原子的价电子排布式为____________ ,在周期表中位置为________________ 。
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①组成[Zn(NH3)4]SO4的元素中,除H外其余元素的第一电离能由大到小排序为________________________ 。
②在[Zn(NH3)4]SO4溶液中滴加NaOH溶液,未出现浑浊,其原因是___________________________ 。
③已知[Zn(NH3)4]2+的空间构型与SO42-相同,则在[Zn(NH3)4]2+中Zn2+的杂化类型为________ 。
④以下作用力在[Zn(NH3)4]SO4晶体中存在的有________ 。
A.离子键 B.极性共价键 C.非极性共价键
D.配位键 E.范德华力 F.金属键
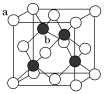
(3)ZnS晶胞结构如图(已知a为硫离子,b为锌离子)所示,ZnS晶体的熔点约为1 700 ℃。
①已知晶体密度为ρ g·cm-3,NA为阿伏加 德罗常数的值。则1个ZnS晶胞的体积为________ cm3。
②ZnO与ZnS结构相似,熔点为1 975 ℃,其熔点较高的原因是_____________________________ 。
(1)基态Zn原子的价电子排布式为
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①组成[Zn(NH3)4]SO4的元素中,除H外其余元素的第一电离能由大到小排序为
②在[Zn(NH3)4]SO4溶液中滴加NaOH溶液,未出现浑浊,其原因是
③已知[Zn(NH3)4]2+的空间构型与SO42-相同,则在[Zn(NH3)4]2+中Zn2+的杂化类型为
④以下作用力在[Zn(NH3)4]SO4晶体中存在的有
A.离子键 B.极性共价键 C.非极性共价键
D.配位键 E.范德华力 F.金属键
(3)ZnS晶胞结构如图(已知a为硫离子,b为锌离子)所示,ZnS晶体的熔点约为1 700 ℃。
①已知晶体密度为ρ g·cm-3,NA为阿伏加 德罗常数的值。则1个ZnS晶胞的体积为
②ZnO与ZnS结构相似,熔点为1 975 ℃,其熔点较高的原因是

更新时间:2019-12-20 09:06:59
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,A、B、D、E、F、G、W、Q各代表一种化学元素。请用元素符号及其物质回答下列问题.
(1)W位于周期表_______ 区;基态Q原子核外简化电子排布式为_______ ;
(2)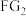 中心原子杂化轨道类型:
中心原子杂化轨道类型:_______ ;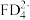 的
的 模型名称:
模型名称:_______ ;
(3)E、F、G三元素第一电离能从大到小的顺序是_______ ;
(4)化合物AD与 溶液反应的离子方程式为
溶液反应的离子方程式为_______ ;
(5)有机物甲由B、氢、D三种元素的原子按个数比为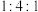 组成,可通过电解法由
组成,可通过电解法由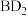 制取,用稀硫酸作电解质溶液,写出生成有机物甲的电极反应式:
制取,用稀硫酸作电解质溶液,写出生成有机物甲的电极反应式:_______ ,有机物甲也可作为燃料电池的原料,写出该燃料电池在碱性条件下的负极反应式:_______ 。
| A | B | D | |||||||||||||||
| E | F | G | |||||||||||||||
| W | Q |
(2)
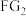 中心原子杂化轨道类型:
中心原子杂化轨道类型: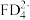 的
的 模型名称:
模型名称:(3)E、F、G三元素第一电离能从大到小的顺序是
(4)化合物AD与
 溶液反应的离子方程式为
溶液反应的离子方程式为(5)有机物甲由B、氢、D三种元素的原子按个数比为
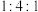 组成,可通过电解法由
组成,可通过电解法由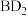 制取,用稀硫酸作电解质溶液,写出生成有机物甲的电极反应式:
制取,用稀硫酸作电解质溶液,写出生成有机物甲的电极反应式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】W、X、Y、Z、N是短周期元素且其中只有一种金属元素,它们的核电荷数依次增大。
(1)W单质的化学式为___________ ,Z元素原子核外有___________ 个原子轨道填充了电子。
(2)Y、Z和N三种元素第一电离能由大到小的顺序为___________ (填元素符号)。
(3)X与Z两元素的电负性较大的是___________ (填元素符号)。
(4)Z元素原子共有___________ 种不同运动状态的电子。
| 元素 | 元素性质或原子结构 |
| W | 原子核内无中子 |
| X | 原子核外s能级上的电子总数与p能级上的电子总数相等 |
| Y | 元素的离子半径在该周期中最小 |
| Z | 原子核外p能级上的电子总数比s能级上的电子总数多2 |
| N | 最外层电子数比次外层电子数少1 |
(2)Y、Z和N三种元素第一电离能由大到小的顺序为
(3)X与Z两元素的电负性较大的是
(4)Z元素原子共有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】C、N化合物对人类生存环境有重要影响。
Ⅰ.汽车尾气中的NO和CO在催化剂作用下可生成无毒无害的气体,工业废气中的NO可被NH3在高温催化作用下还原为N2和H2O。
(1)原子序数为N元素两倍的元素的基态原子的外围电子排布图为_________ 。
(2)C、N、O三种元素的第一电离能由小到大的顺序为_________ 。
(3)键角:NH3__________ (填“>“<”或“=”)H2O;NH3的VSEPR模型为_________ 。
Ⅱ.NO与血红蛋白中的[Fe(H2O)6]2+结合生成[Fe(NO)(H2O)5]2+可导致人体的血红蛋白丧失携氧能力。
(4)Fe2+的配位数为_________ 。
(5)在[Fe(NO)(H2O)5]2+中,配体NO提供配位的原子为_________ (填元素符号),原因是_________ 。
Ⅲ.C元素与N元素形成的一种超硬晶体的晶胞结构如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),设晶胞参数为anm,NA为阿伏加德罗常数的值,1号原子的坐标为(0,0,0)、3号原子的坐标为(1,1,1)。_________ 。
②2号原子的坐标为_________ 。
③该晶体的密度为__________ g/cm3。
Ⅰ.汽车尾气中的NO和CO在催化剂作用下可生成无毒无害的气体,工业废气中的NO可被NH3在高温催化作用下还原为N2和H2O。
(1)原子序数为N元素两倍的元素的基态原子的外围电子排布图为
(2)C、N、O三种元素的第一电离能由小到大的顺序为
(3)键角:NH3
Ⅱ.NO与血红蛋白中的[Fe(H2O)6]2+结合生成[Fe(NO)(H2O)5]2+可导致人体的血红蛋白丧失携氧能力。
(4)Fe2+的配位数为
(5)在[Fe(NO)(H2O)5]2+中,配体NO提供配位的原子为
Ⅲ.C元素与N元素形成的一种超硬晶体的晶胞结构如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),设晶胞参数为anm,NA为阿伏加德罗常数的值,1号原子的坐标为(0,0,0)、3号原子的坐标为(1,1,1)。
②2号原子的坐标为
③该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,基态镍原子M层上的未成对电子数为___________ ;
(2)大阪大学近日宣布,有机太阳能固体电池效率突破5.3%,而高纯度C60是其“秘密武器”。C60的结构如图1,分子中碳原子轨道的杂化类型为___________ ;1mol C60分子中π键的数目为___________ ;
(3)金属酞菁配合物在硅太阳能电池中有重要作用,一种金属镁酞菁配合物的结构如图2,该结构中,碳氮之间的共价键类型有___________ (按原子轨道重叠方式填写共价键的类型),请在图2中用箭头表示出配位键_________________ 。
。

(4)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜锢硒薄膜电池等。
①第一电离能:As__________ Se(填“>”、“<”或“=”);
②硫化锌的晶胞中(结构如图3所示),硫离子的配位数是___________ ;
③二氧化硒分子的空间构型为___________ ;
(5) 在硼酸盐中,阴离子有链状、环状等多种结构形式。图(a)是一种链状结构的多硼酸根,则多硼酸根离子符号为___________ ;图(b)是硼砂晶体中阴离子的环状结构,其中硼原子采取的杂化类型为___________ 。

(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,基态镍原子M层上的未成对电子数为
(2)大阪大学近日宣布,有机太阳能固体电池效率突破5.3%,而高纯度C60是其“秘密武器”。C60的结构如图1,分子中碳原子轨道的杂化类型为
(3)金属酞菁配合物在硅太阳能电池中有重要作用,一种金属镁酞菁配合物的结构如图2,该结构中,碳氮之间的共价键类型有
。

(4)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜锢硒薄膜电池等。
①第一电离能:As
②硫化锌的晶胞中(结构如图3所示),硫离子的配位数是
③二氧化硒分子的空间构型为
(5) 在硼酸盐中,阴离子有链状、环状等多种结构形式。图(a)是一种链状结构的多硼酸根,则多硼酸根离子符号为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】铁与镁组成的合金是目前已发现的储氢密度最高的储氢材料之一,回答下列问题:
(1)下列铁的外围电子排布图中,再失去一个电子需要能量最大的是_______ (填字母)。
A. B.
B.
C.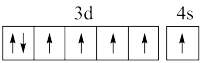 D.
D.
在第四周期过渡元素中,基态原子未成对电子数比铁多的元素为_______ (填元素符号)。
(2)甘氨酸亚铁络合物[(H2NCH2COO)2Fe]是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。
①(H2NCH2COO)2Fe中含有的非金属元素的第一电离能由大到小的顺序为_______ (用元素符号表示),碳原子的杂化类型为_______ 。
②甘氨酸H2NCH2COOH的沸点比相同相对分子质量的烷烃的沸点大很多,原因是_______ 。
③原子中的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的氧原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氧原子,其价电子自旋磁量子数的代数和为_______ 。
④硫酸亚铁(FeSO4)可用于制造甘氨酸亚铁, 的空间构型为
的空间构型为_______ 、形成的σ键的类型为_______ 。
(1)下列铁的外围电子排布图中,再失去一个电子需要能量最大的是
A.
 B.
B.
C.
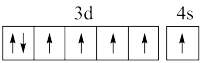 D.
D.
在第四周期过渡元素中,基态原子未成对电子数比铁多的元素为
(2)甘氨酸亚铁络合物[(H2NCH2COO)2Fe]是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。
①(H2NCH2COO)2Fe中含有的非金属元素的第一电离能由大到小的顺序为
②甘氨酸H2NCH2COOH的沸点比相同相对分子质量的烷烃的沸点大很多,原因是
③原子中的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的氧原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氧原子,其价电子自旋磁量子数的代数和为④硫酸亚铁(FeSO4)可用于制造甘氨酸亚铁,
 的空间构型为
的空间构型为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】前四周期的以下五种元素:
(1)X元素名称_____________ ,RZ3中R的杂化方式为_____________ 。
(2)W原子结构示意图为_____________ ,,Y、Z、Q电负性由小到大顺序_____________ 。(用元素符号表示)
(3)将Q氢化物浓溶液中加入Cu粉,并通入Z2,充分反应后溶液呈深蓝色,该反应的离子方程式为_______________________________________ 。
| X | 单质与水反应生成的气体可使带火星的木条复燃 |
| Y | 核外有三个能级,每个能级的电子数相等 |
| Z | 最外层电子数是次外层的3倍 |
| W | 在元素周期表中处于第8列 |
| R | 核外电子占据9个轨道,有2个未成对电子 |
| Q | 第二周期中单电子数最多 |
(1)X元素名称
(2)W原子结构示意图为
(3)将Q氢化物浓溶液中加入Cu粉,并通入Z2,充分反应后溶液呈深蓝色,该反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】氟及其化合物用途非常广泛。回答下列问题:
(1)基态氟原子的价层电子排布图(轨道表示式)为_______ 。
(2)制备NSF3的反应为FCONSF2+2AgF2⇌NSF3+2AgF+COF2。
①F、O、N、S的第一电离能从小到大的顺序是_______ 。
②化工生产中NSF3可用作SF6的替代品,SF6分子的空间构型为_______ 。
③COF2分子中σ键和π键的个数比为_______ 。
(3)NHF2的一种制备方法是CO(NH2)2+2F2+H2O=NHF2+CO2+NH4HF2。
①CO(NH2)2中C的杂化方式是_______ 。
②CO(NH2)2的熔沸点比CH3CONH2的高,其原因是_______ 。
③下列说法正确的是_______ (填标号)。
A.NHF2、CO2均是极性分子
B.H2O与NHF2中心原子的价层电子对数相同
C.NH4HF2中存在离子键、配位键和氢键
(4)由Cs、Ag及F三种元素组成的一种超导材料的晶体结构如下图所示(Ag不是+1价):

已知AC=BE,则C、D(Cs与F)间的距离为_______ pm(用含a、c、s的代数式表示,列出计算式,下同);设NA为阿伏加德罗常数的值,则晶体的密度为_______ g·cm-3。
(1)基态氟原子的价层电子排布图(轨道表示式)为
(2)制备NSF3的反应为FCONSF2+2AgF2⇌NSF3+2AgF+COF2。
①F、O、N、S的第一电离能从小到大的顺序是
②化工生产中NSF3可用作SF6的替代品,SF6分子的空间构型为
③COF2分子中σ键和π键的个数比为
(3)NHF2的一种制备方法是CO(NH2)2+2F2+H2O=NHF2+CO2+NH4HF2。
①CO(NH2)2中C的杂化方式是
②CO(NH2)2的熔沸点比CH3CONH2的高,其原因是
③下列说法正确的是
A.NHF2、CO2均是极性分子
B.H2O与NHF2中心原子的价层电子对数相同
C.NH4HF2中存在离子键、配位键和氢键
(4)由Cs、Ag及F三种元素组成的一种超导材料的晶体结构如下图所示(Ag不是+1价):

已知AC=BE,则C、D(Cs与F)间的距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】钛、铬、铁、镍、铜、硼等元素及其化合物在工业上有重要用途。
(1)钛铁合金是铁系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为___________ 。
②Fe的基态原子共有___________ 种不同能级的电子。
③ 也是一种储氢材料,可由
也是一种储氢材料,可由 和
和 反应制得。
反应制得。 由
由 和
和 构成,
构成, 的立体结构是
的立体结构是___________ 。
(2)制备 的反应为
的反应为 。
。
①上述化学方程式中非金属元素电负性由大到小的顺序是___________ (用元素符号表示)。
②分子中所有原子均满足8电子构型, 的电子式为
的电子式为___________ ,分子中 键和
键和 键的个数比为
键的个数比为___________ ,中心原子的杂化方式为___________ 。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中 和
和 的离子半径分别为
的离子半径分别为 和
和 。则熔点:NiO
。则熔点:NiO___________ FeO(填“>”、“<”或“=”)。
(4)某铜镍合金的立方晶胞结构如图所示。
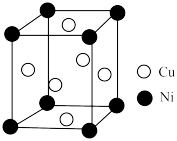
①该晶体的化学式为___________ 。
②已知该晶胞的摩尔质量为 ,密度为
,密度为 。设
。设 为阿伏加德罗常数的值,则该晶胞的棱长是
为阿伏加德罗常数的值,则该晶胞的棱长是___________ cm。(用含M、d、 的代数式表示)
的代数式表示)
(1)钛铁合金是铁系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为
②Fe的基态原子共有
③
 也是一种储氢材料,可由
也是一种储氢材料,可由 和
和 反应制得。
反应制得。 由
由 和
和 构成,
构成, 的立体结构是
的立体结构是(2)制备
 的反应为
的反应为 。
。①上述化学方程式中非金属元素电负性由大到小的顺序是
②分子中所有原子均满足8电子构型,
 的电子式为
的电子式为 键和
键和 键的个数比为
键的个数比为(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中
 和
和 的离子半径分别为
的离子半径分别为 和
和 。则熔点:NiO
。则熔点:NiO(4)某铜镍合金的立方晶胞结构如图所示。

①该晶体的化学式为
②已知该晶胞的摩尔质量为
 ,密度为
,密度为 。设
。设 为阿伏加德罗常数的值,则该晶胞的棱长是
为阿伏加德罗常数的值,则该晶胞的棱长是 的代数式表示)
的代数式表示)
您最近一年使用:0次
【推荐3】在建国 70周年阅兵仪式上,“歼20”“东风-41核导弹”等国之重器亮相,它们采用了大量合金材料。回答下列问题:
(1)早期战斗机主要采用铝合金,其中超硬铝属A1-Cu-Mg-Zn系。Cu在元素周期表中的位置是___________ ,比较第一电离能Al___________ Mg (填“>”“<”“=”)。
(2)查阅资料显示第二电离能Cu大于Zn,理由是___________ 。
(3)中期战斗机主要采用钛合金,Ti的价电子排布图为___________ 。钛晶体在882 °C以 上为体心立方的β钛,其中钛原子的配位数为___________ 。
(4)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成Ti (SO4)2、 NiSO4,其中阴离子中心S的___________ 杂化轨道与O的2p轨道形成___________ 键(填“π”或“σ”)。
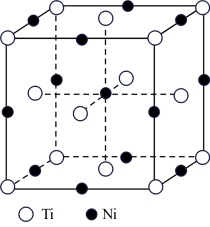
(5)一种钛镍合金的立方晶胞结构如图所示,若晶胞的边长为a pm,则晶胞的密度为___________ g/cm3(用含a、NA的计算式表示)。
(1)早期战斗机主要采用铝合金,其中超硬铝属A1-Cu-Mg-Zn系。Cu在元素周期表中的位置是
(2)查阅资料显示第二电离能Cu大于Zn,理由是
(3)中期战斗机主要采用钛合金,Ti的价电子排布图为
(4)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成Ti (SO4)2、 NiSO4,其中阴离子中心S的
(5)一种钛镍合金的立方晶胞结构如图所示,若晶胞的边长为a pm,则晶胞的密度为

您最近一年使用:0次



