已知:某些强酸盐的水溶液呈中性,如NaCl溶液,某些弱酸盐的水溶液呈碱性,如Na2CO3溶液。请根据如下图所示转化关系回答有关问题。A和B均为焰色反应呈黄色的水溶液,A呈中性,B呈碱性并具有强氧化性。

(1)写出C的化学式:________ 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:___________________ ,_____________________ 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:____________ 。
(4)检验K溶液中阳离子的简易方法是__________ 。

(1)写出C的化学式:
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:
(4)检验K溶液中阳离子的简易方法是
更新时间:2019-12-18 15:43:58
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】二氧化氯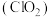 是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)在处理废水时, 可将废水中的
可将废水中的 氧化成
氧化成 和
和 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
(2)某小组按照文献中制备 的方法设计了如图所示的实验装置用于制备
的方法设计了如图所示的实验装置用于制备 。
。

①装置A用于生成 气体,该反应的化学方程式是
气体,该反应的化学方程式是_______ 。
②通入氮气的作用有两个,一个是起到搅拌作用,二是_______ 装置B的作用是_______ 。
(3)测定装置C中 溶液的浓度:取
溶液的浓度:取 中溶液于锥形瓶中,加入足量的
中溶液于锥形瓶中,加入足量的 溶液和
溶液和 酸化,然后加入
酸化,然后加入_______ 作指示剂,用 的
的 标准液滴定锥形瓶中的溶液(
标准液滴定锥形瓶中的溶液( ),消耗标准溶液的体积为
),消耗标准溶液的体积为 ,滴定终点的现象是
,滴定终点的现象是_______ 。
(4)计算C中 溶液的物质的量浓度,写出计算过程
溶液的物质的量浓度,写出计算过程_______ 。
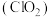 是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:(1)在处理废水时,
 可将废水中的
可将废水中的 氧化成
氧化成 和
和 ,该反应的离子方程式是
,该反应的离子方程式是(2)某小组按照文献中制备
 的方法设计了如图所示的实验装置用于制备
的方法设计了如图所示的实验装置用于制备 。
。
①装置A用于生成
 气体,该反应的化学方程式是
气体,该反应的化学方程式是②通入氮气的作用有两个,一个是起到搅拌作用,二是
(3)测定装置C中
 溶液的浓度:取
溶液的浓度:取 中溶液于锥形瓶中,加入足量的
中溶液于锥形瓶中,加入足量的 溶液和
溶液和 酸化,然后加入
酸化,然后加入 的
的 标准液滴定锥形瓶中的溶液(
标准液滴定锥形瓶中的溶液( ),消耗标准溶液的体积为
),消耗标准溶液的体积为 ,滴定终点的现象是
,滴定终点的现象是(4)计算C中
 溶液的物质的量浓度,写出计算过程
溶液的物质的量浓度,写出计算过程
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
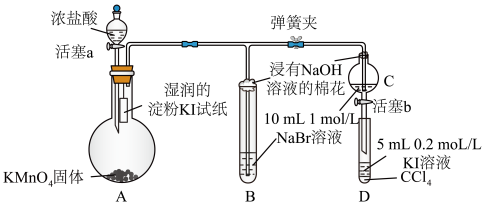
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是_____ 。
(2)验证氯气的氧化性强于碘的实验现象是____ 。
(3)B中溶液发生反应的离子方程式是______ 。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是_____ 。
(5)过程Ⅲ实验的目的是______ 。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是
(2)验证氯气的氧化性强于碘的实验现象是
(3)B中溶液发生反应的离子方程式是
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是
(5)过程Ⅲ实验的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加_________ ,该过程的现象为:_____________ 。
(2)步骤②加入过量H2O2的目的:____________ 。
(3)步骤③中反应的离子方程式:____________ 。
(4)步骤④中一系列处理的操作步骤:过滤、_________ 、灼烧、_________ 、称量。
(5)若实验无损耗,则每片补血剂含铁元素的质量_________ g。
(6)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+=5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需___________ 。
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是_________ 。
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
③滴定到终点时的溶液颜色为_________ 色。

请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加
(2)步骤②加入过量H2O2的目的:
(3)步骤③中反应的离子方程式:
(4)步骤④中一系列处理的操作步骤:过滤、
(5)若实验无损耗,则每片补血剂含铁元素的质量
(6)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+=5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
③滴定到终点时的溶液颜色为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】用下图所示实验装置进行铁与水蒸气反应的实验,并对反应后硬质试管中固体物质的组成进行了探究。
Ⅰ.已知:铁氰化钾可用于检验二价铁离子,离子方程式为: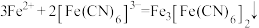 ,现象:将待测液滴入黄色的铁氰化钾溶液中,产生特征的蓝色沉淀
,现象:将待测液滴入黄色的铁氰化钾溶液中,产生特征的蓝色沉淀
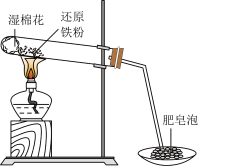
请回答下列问题:
(1)该反应的化学方程式是________ ,
(2)该同学对反应后硬质试管中固体物质的组成提出了如下假设。
假设1:只有Fe;
假设2:只有________ (填化学式)
假设3:既有Fe 也有 。
。
(3)为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究:反应前固体物质的质量为5.6g,反应后固体物质的质量为6.6g。从数据分析,反应后硬质试管中固体物质的组成成分为________ 。
Ⅱ.长期放置的FeSO4溶液易被氧化而变质,某兴趣小组进行了如下实验:
(4)设计实验检验FeSO4溶液的变质程度
①将上述方案补充完整;
②步骤2涉及的离子反应方程式是________ 。
③若要使变质的FeSO4复原,方法是_____ 。(写离子反应方程式)
Ⅰ.已知:铁氰化钾可用于检验二价铁离子,离子方程式为:
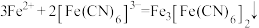 ,现象:将待测液滴入黄色的铁氰化钾溶液中,产生特征的蓝色沉淀
,现象:将待测液滴入黄色的铁氰化钾溶液中,产生特征的蓝色沉淀
请回答下列问题:
(1)该反应的化学方程式是
(2)该同学对反应后硬质试管中固体物质的组成提出了如下假设。
假设1:只有Fe;
假设2:只有
假设3:既有Fe 也有
 。
。(3)为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究:反应前固体物质的质量为5.6g,反应后固体物质的质量为6.6g。从数据分析,反应后硬质试管中固体物质的组成成分为
Ⅱ.长期放置的FeSO4溶液易被氧化而变质,某兴趣小组进行了如下实验:
(4)设计实验检验FeSO4溶液的变质程度
实验方案 | 实验现象 | 实验结论 | |
步骤1 | 取待检测液于试管中,向其中滴加KSCN溶液 | FeSO4溶液部分变质 | |
步骤2 | 取待检测液于试管中,向其中滴加 溶液 溶液 | ||
②步骤2涉及的离子反应方程式是
③若要使变质的FeSO4复原,方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铁及其化合物与生产、生活关系密切
(1)生铁是通过高炉冶炼而得,用化学方程式表示其原理为______________________ 。冶炼过程中,即被氧化又被还原的元素是(填元素符号)____________ ;
(2)铁在一定条件下可与多种非金属单质反应,铁与氯气反应的化学方程式为___________________ ,铁与硫反应的化学方程式为__________________________ 。
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:
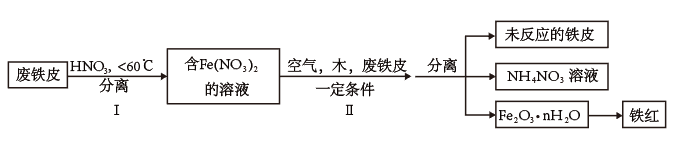
①步骤I若要检验是否有Fe3+生成,方法是____________ ,离子方程式为_________ 。
②步骤II中发生反应:4Fe(NO3)2+O2+(2n+4)H2O→2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为________________ 。
③上述生产流程中,能体现“绿色化学”思想的是_____________________ (任写一项)。
(1)生铁是通过高炉冶炼而得,用化学方程式表示其原理为
(2)铁在一定条件下可与多种非金属单质反应,铁与氯气反应的化学方程式为
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤I若要检验是否有Fe3+生成,方法是
②步骤II中发生反应:4Fe(NO3)2+O2+(2n+4)H2O→2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为
③上述生产流程中,能体现“绿色化学”思想的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】铁及其化合物有丰富多彩的化学性质。回答下列问题:
(1)铁元素在周期表中的位置为第______ 周期第_____ 族。
(2)FeCl3溶液可用于吸收尾气中的SO2,写出该反应的离子方程式:_____________________________________________________ 。
(3)某化学兴趣小组同学用如图装置,充分加热硫酸亚铁晶体(FeSO4·xH2O)至完全分解。

①装置A中需持续通入N2,其目的是__________________________________________________________________ 。
②充分反应一段时间后,小组同学观察到实验现象为:装置A中残留有红棕色固体,装置B中固体变蓝,C中溶液褪色,请写出FeSO4分解的化学方程式:____________________________________ 。
③装置D中干燥管的作用为____________________________ 。
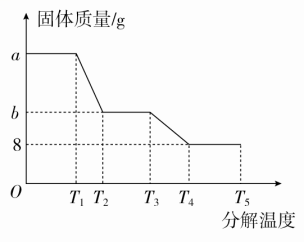
④小组同学利用数字化实验仪器测定了不同温度时FeSO4·xH2O分解的质量变化情况,得到如图关系:
实验结束后,装置B质量增加12.6 g,结合上图数据,确定FeSO4·xH2O中的x=________ 。
(1)铁元素在周期表中的位置为第
(2)FeCl3溶液可用于吸收尾气中的SO2,写出该反应的离子方程式:
(3)某化学兴趣小组同学用如图装置,充分加热硫酸亚铁晶体(FeSO4·xH2O)至完全分解。

①装置A中需持续通入N2,其目的是
②充分反应一段时间后,小组同学观察到实验现象为:装置A中残留有红棕色固体,装置B中固体变蓝,C中溶液褪色,请写出FeSO4分解的化学方程式:
③装置D中干燥管的作用为

④小组同学利用数字化实验仪器测定了不同温度时FeSO4·xH2O分解的质量变化情况,得到如图关系:
实验结束后,装置B质量增加12.6 g,结合上图数据,确定FeSO4·xH2O中的x=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某校高一某化学小组欲探如下实验,想请你帮助他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性;实验所用试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、碘化钾、淀粉溶液;实验记录:
实验结论:Fe只有还原性;Fe3+只有氧化性;Fe2+既有氧化性,又有还原性。
实验目的:探究铁及其化合物的氧化性和还原性;实验所用试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、碘化钾、淀粉溶液;实验记录:
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为黄色 | Fe2+具有还原性 | |
| ② | 在FeCl3溶液中加入足量铁粉 | Fe +2Fe3+=3Fe2+ | ||
| ③ | 在FeCl3溶液中滴入适量KI溶液和淀粉溶液 | 溶液最终变为蓝色 | Fe3+具有氧化性 |
您最近一年使用:0次
【推荐3】硫化镍矿的主要成分是 ,还含有
,还含有 、
、 、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
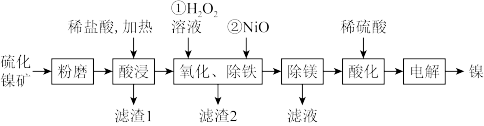
(1)硫化镍矿粉磨的目的是_______ ,“酸浸”时,硫化镍与稀盐酸反应的化学方程式为_______ 。
(2)“氧化、除铁”过程中加入 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为_______ ;加入氧化镍的目的是除去铁元素,用化学平衡移动原理解释除去铁元素的原因_______ 。
(3)已知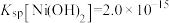 ,
,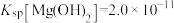 ,若“除镁”后的滤液中
,若“除镁”后的滤液中 的浓度不大于
的浓度不大于 ,则滤液中
,则滤液中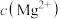 ≤
≤_______ 。
(4)电解硫酸镍溶液时,在_______ 极得到镍单质,电解产物_______ (填化学式)可以循环使用。
 ,还含有
,还含有 、
、 、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
(1)硫化镍矿粉磨的目的是
(2)“氧化、除铁”过程中加入
 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为(3)已知
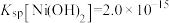 ,
,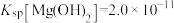 ,若“除镁”后的滤液中
,若“除镁”后的滤液中 的浓度不大于
的浓度不大于 ,则滤液中
,则滤液中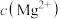 ≤
≤(4)电解硫酸镍溶液时,在
您最近一年使用:0次

 溶于
溶于


