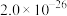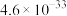硫化镍矿的主要成分是 ,还含有
,还含有 、
、 、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
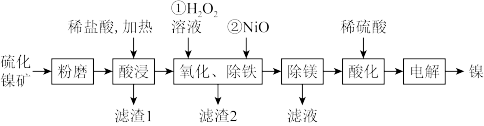
(1)硫化镍矿粉磨的目的是_______ ,“酸浸”时,硫化镍与稀盐酸反应的化学方程式为_______ 。
(2)“氧化、除铁”过程中加入 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为_______ ;加入氧化镍的目的是除去铁元素,用化学平衡移动原理解释除去铁元素的原因_______ 。
(3)已知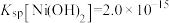 ,
,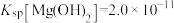 ,若“除镁”后的滤液中
,若“除镁”后的滤液中 的浓度不大于
的浓度不大于 ,则滤液中
,则滤液中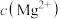 ≤
≤_______ 。
(4)电解硫酸镍溶液时,在_______ 极得到镍单质,电解产物_______ (填化学式)可以循环使用。
 ,还含有
,还含有 、
、 、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
(1)硫化镍矿粉磨的目的是
(2)“氧化、除铁”过程中加入
 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为(3)已知
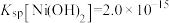 ,
,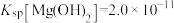 ,若“除镁”后的滤液中
,若“除镁”后的滤液中 的浓度不大于
的浓度不大于 ,则滤液中
,则滤液中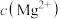 ≤
≤(4)电解硫酸镍溶液时,在
2021·河北·模拟预测 查看更多[3]
2021年河北省高中名校名师原创预测卷化学(第三模拟)(已下线)微专题18 金属及其化合物制备流程(Ni)-备战2022年高考化学考点微专题(已下线)第三章 金属及其化合物 第16练 金属及其化合物知识落实与拓展
更新时间:2021-01-10 19:44:28
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费。可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。测得某废腐蚀液中含CuCl2 1.5 mol/L,FeCl2 3.0 mol/L,FeCl3 1.0 mol/L,HCl 3.0 mol/L。取废腐蚀液200 mL按如下流程在实验室进行实验:

回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂所需试剂是________ (填化学式)。
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物。反应的化学方程式为__________________________________ 。
(3)如图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置。

实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收。控制生成氯气速度的操作是__________________________________ 。
(4)按上述流程操作,需称取Fe粉的质量应不少于________ g(精确到0.1 g),需通入Cl2的体积不少于________ L(标况)。

回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂所需试剂是
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物。反应的化学方程式为
(3)如图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置。

实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收。控制生成氯气速度的操作是
(4)按上述流程操作,需称取Fe粉的质量应不少于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】 在现代工业生产中应用广泛,查阅资料得:无水
在现代工业生产中应用广泛,查阅资料得:无水 在空气中易潮解,加热易升华。
在空气中易潮解,加热易升华。
(1)用丁达尔效应鉴别 胶体和
胶体和 溶液的操作是
溶液的操作是____________ (写出具体实验操作、结论)。
(2)电子工业中用 溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出
溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:__________________ 。该反应的还原剂是______ 。
(3)硫化氢( )是一种有毒的气体,可用
)是一种有毒的气体,可用 溶液吸收,生成单质硫(S)沉淀。
溶液吸收,生成单质硫(S)沉淀。 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为____________ 。该反应中氧化产物与还原产物的物质的量之比为______ 。
(4)某小组同学设计了制备无水) 的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
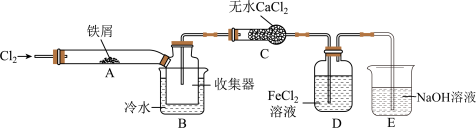
步骤Ⅰ.检验装置的气密性;
步骤Ⅱ.通入干燥的 ,赶尽装置中的空气;
,赶尽装置中的空气;
步骤Ⅲ.用酒精灯在铁屑下方加热至反应完成;
步骤Ⅳ.体系冷却后,停止通入 ,并用干燥的
,并用干燥的 赶尽
赶尽 ,将收集器密封。
,将收集器密封。
①装置A中发生反应的化学方程式为__________________ 。
②装置B中冷水浴的作用为____________ 。
 在现代工业生产中应用广泛,查阅资料得:无水
在现代工业生产中应用广泛,查阅资料得:无水 在空气中易潮解,加热易升华。
在空气中易潮解,加热易升华。(1)用丁达尔效应鉴别
 胶体和
胶体和 溶液的操作是
溶液的操作是(2)电子工业中用
 溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出
溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:(3)硫化氢(
 )是一种有毒的气体,可用
)是一种有毒的气体,可用 溶液吸收,生成单质硫(S)沉淀。
溶液吸收,生成单质硫(S)沉淀。 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为(4)某小组同学设计了制备无水)
 的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
步骤Ⅰ.检验装置的气密性;
步骤Ⅱ.通入干燥的
 ,赶尽装置中的空气;
,赶尽装置中的空气;步骤Ⅲ.用酒精灯在铁屑下方加热至反应完成;
步骤Ⅳ.体系冷却后,停止通入
 ,并用干燥的
,并用干燥的 赶尽
赶尽 ,将收集器密封。
,将收集器密封。①装置A中发生反应的化学方程式为
②装置B中冷水浴的作用为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硫的化合物在生产、生活中应用广泛。
I.某兴趣小组探究 气体还原
气体还原 、
、 。
。
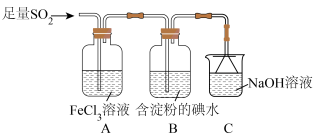
(1)通入足量 后,装置B中的现象是
后,装置B中的现象是___________ ;装置C的作用是___________ 。
(2)该小组同学认为 与
与 溶液发生的是氧化还原反应。写出
溶液发生的是氧化还原反应。写出 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
II.实验室可用如图装皿(略去部分夹持仪器)制取 并验证其性质。
并验证其性质。
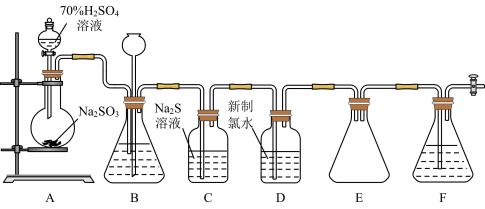
(3)盛装 的仪器名称为
的仪器名称为___________ 。
(4)装置B的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择___________ (填字母)。
a.蒸馏水 b.饱和 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和NaOH溶液
溶液 d.饱和NaOH溶液
(5)为验证二氧化硫的还原性,充分反应后,取装置D中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案II:向第二份溶液中加入品红溶液,红色褪去;
方案III:向第三份溶液中加入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
上述方案合理的是方案___________ (填“I”“II”或“III”);装置D中发生反应的离子方程式为___________ 。
I.某兴趣小组探究
 气体还原
气体还原 、
、 。
。
(1)通入足量
 后,装置B中的现象是
后,装置B中的现象是(2)该小组同学认为
 与
与 溶液发生的是氧化还原反应。写出
溶液发生的是氧化还原反应。写出 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:II.实验室可用如图装皿(略去部分夹持仪器)制取
 并验证其性质。
并验证其性质。
(3)盛装
 的仪器名称为
的仪器名称为(4)装置B的作用之一是通过观察产生气泡的多少判断
 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择a.蒸馏水 b.饱和
 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和NaOH溶液
溶液 d.饱和NaOH溶液(5)为验证二氧化硫的还原性,充分反应后,取装置D中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案II:向第二份溶液中加入品红溶液,红色褪去;
方案III:向第三份溶液中加入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。上述方案合理的是方案
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】一种利用某镍矿资源(主要成分为 、
、 ,含有少量
,含有少量 、
、 、
、 、
、 、
、 )提取含Ni、Cu、Fe、Mg、Al的物质的流程如下:
)提取含Ni、Cu、Fe、Mg、Al的物质的流程如下:
i.25℃时,一些物质的 如下:
如下:
ii.溶液中离子浓度 时认为该离子沉淀完全。
时认为该离子沉淀完全。
(1)流程中能加快反应速率的措施有_________ 。
(2)固体A中还有少量酸浸后剩余的NiS,II中反应的离子方程式为_________ 。
(3)III中,生成 转移
转移 ,III中反应的化学方程式为
,III中反应的化学方程式为_________ ;III过滤后得到的固体残渣中含有的物质是_________ 。
(4)IV可以除去溶液D中的 ,由此推测氧化性
,由此推测氧化性
_________  (填“>”或“<”)。
(填“>”或“<”)。
(5)结合离子方程式解释V中加入 的作用:
的作用:_________ 。
(6)为了使 沉淀完全,VI中溶液pH的最小值所属范围为
沉淀完全,VI中溶液pH的最小值所属范围为_________ (填字母)。
a.2~3 b.3~4 c.9~10 d.10~11
(7)VI中, 不宜多加,原因是
不宜多加,原因是_________ 。
 、
、 ,含有少量
,含有少量 、
、 、
、 、
、 、
、 )提取含Ni、Cu、Fe、Mg、Al的物质的流程如下:
)提取含Ni、Cu、Fe、Mg、Al的物质的流程如下: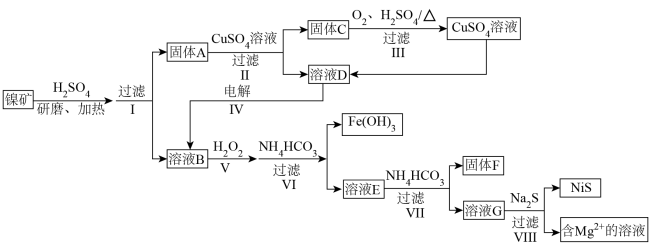
i.25℃时,一些物质的
 如下:
如下:物质 |
|
|
|
|
|
|
|
|
|
|
|
|
|
 时认为该离子沉淀完全。
时认为该离子沉淀完全。(1)流程中能加快反应速率的措施有
(2)固体A中还有少量酸浸后剩余的NiS,II中反应的离子方程式为
(3)III中,生成
 转移
转移 ,III中反应的化学方程式为
,III中反应的化学方程式为(4)IV可以除去溶液D中的
 ,由此推测氧化性
,由此推测氧化性
 (填“>”或“<”)。
(填“>”或“<”)。(5)结合离子方程式解释V中加入
 的作用:
的作用:(6)为了使
 沉淀完全,VI中溶液pH的最小值所属范围为
沉淀完全,VI中溶液pH的最小值所属范围为a.2~3 b.3~4 c.9~10 d.10~11
(7)VI中,
 不宜多加,原因是
不宜多加,原因是
您最近一年使用:0次
【推荐2】盐湖卤水(主要含 、
、 '、
'、 、
、 、
、 和硼酸根等)是锂盐的重要来源,一种以高镁卤水为原料经两段除镁制备Li2CO3的工艺流程如图:
和硼酸根等)是锂盐的重要来源,一种以高镁卤水为原料经两段除镁制备Li2CO3的工艺流程如图:
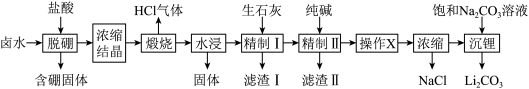
已知:硼原子有3个价电子,但有4个价轨道,这种价电子数少于价轨道数的原子称作缺电子原子。
常温下 、
、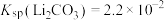 。
。
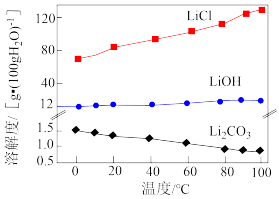
相关化合物的溶解度与温度的关系如图所示。
回答下列问题:
(1)含硼固体中的 晶体为层型片状结构,在层与层之间容易裂解,其原因是层与层之间通过
晶体为层型片状结构,在层与层之间容易裂解,其原因是层与层之间通过_______ 结合, 在水中的电离方程式为
在水中的电离方程式为_______ 。
(2) 与
与 溶液反应可制备硼砂
溶液反应可制备硼砂 ,硼砂分子中硼原子的化合价为
,硼砂分子中硼原子的化合价为_______ ;常温下 硼砂溶液中,
硼砂溶液中, 水解生成相同浓度的
水解生成相同浓度的 和
和 ,则溶液
,则溶液
_______ 。
(3)“水浸”后的固体主要成分为_______ (填化学式,下同);精制 后溶液中
后溶液中 的浓度为
的浓度为 ,则常温下精制II过程中
,则常温下精制II过程中 浓度应控制在
浓度应控制在_______  以下。
以下。
(4)精制II的目的是除去滤液中的_______ ,进行操作 的目的是除去溶液中的
的目的是除去溶液中的_______ 。
 、
、 '、
'、 、
、 、
、 和硼酸根等)是锂盐的重要来源,一种以高镁卤水为原料经两段除镁制备Li2CO3的工艺流程如图:
和硼酸根等)是锂盐的重要来源,一种以高镁卤水为原料经两段除镁制备Li2CO3的工艺流程如图:
已知:硼原子有3个价电子,但有4个价轨道,这种价电子数少于价轨道数的原子称作缺电子原子。
常温下
 、
、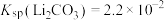 。
。相关化合物的溶解度与温度的关系如图所示。

回答下列问题:
(1)含硼固体中的
 晶体为层型片状结构,在层与层之间容易裂解,其原因是层与层之间通过
晶体为层型片状结构,在层与层之间容易裂解,其原因是层与层之间通过 在水中的电离方程式为
在水中的电离方程式为(2)
 与
与 溶液反应可制备硼砂
溶液反应可制备硼砂 ,硼砂分子中硼原子的化合价为
,硼砂分子中硼原子的化合价为 硼砂溶液中,
硼砂溶液中, 水解生成相同浓度的
水解生成相同浓度的 和
和 ,则溶液
,则溶液
(3)“水浸”后的固体主要成分为
 后溶液中
后溶液中 的浓度为
的浓度为 ,则常温下精制II过程中
,则常温下精制II过程中 浓度应控制在
浓度应控制在 以下。
以下。(4)精制II的目的是除去滤液中的
 的目的是除去溶液中的
的目的是除去溶液中的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】组成芯片的核心物质是高纯度硅。如图是以石英砂为原料同时制备硅和金属锂的工艺流程。(石英砂主要含SiO2、锂的碳酸盐和少量的Fe2O3、Al2O3)
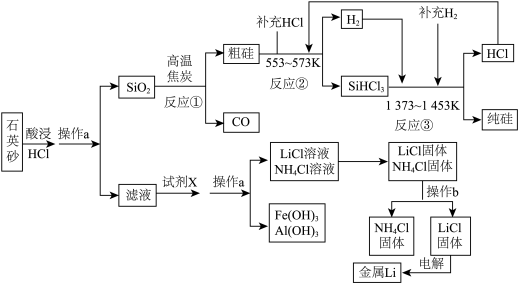
已知:LiCl的熔点是605℃、沸点是1350℃;NH4Cl在100℃开始显著挥发,337.8℃分解完全。常温下,Ksp[Fe(OH)3]=2.64×10-39,Ksp[Al(OH)3]=1×10-33。
(1)粗硅中常含有副产物SiC,请写出反应①中生成SiC的反应方程式:_____ 。
(2)整个制硅过程必须严格控制无水无氧。SiHCl3遇水能发生剧烈反应,写出该反应的化学方程式:______ 。
(3)试剂X是_____ ;请写出操作名称:a.______ ;b.______ 。
(4)本生产工艺要求常温下要控制LiCl和NH4Cl溶液中的杂质离子浓度不大于1.0×10-6mol•L-1,应控制溶液的pH最小为_____ ,此时溶液中Fe3+的浓度为______ 。

已知:LiCl的熔点是605℃、沸点是1350℃;NH4Cl在100℃开始显著挥发,337.8℃分解完全。常温下,Ksp[Fe(OH)3]=2.64×10-39,Ksp[Al(OH)3]=1×10-33。
(1)粗硅中常含有副产物SiC,请写出反应①中生成SiC的反应方程式:
(2)整个制硅过程必须严格控制无水无氧。SiHCl3遇水能发生剧烈反应,写出该反应的化学方程式:
(3)试剂X是
(4)本生产工艺要求常温下要控制LiCl和NH4Cl溶液中的杂质离子浓度不大于1.0×10-6mol•L-1,应控制溶液的pH最小为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】碳酸镍可用于电镀、陶瓷器着色等。从镍矿渣出发制备碳酸镍的流程如下:
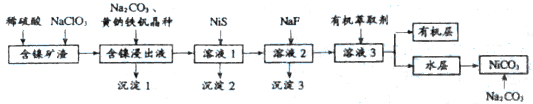
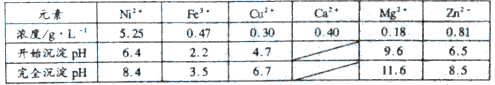
已知:(Ⅰ)含镍浸出液的成分及离子沉淀的pH:
(Ⅱ)溶度积常数:

(1)镍矿渣中镍元素的主要存在形式是Ni(OH)2、NiS,写出浸取时NiS反应的离子方程式_____________ 。
(2)黄钠铁钒[NaFe3(SO4)2(OH)6]具有沉淀颗粒大、沉淀速度快,容易过滤等特点,常用于除铁。写出流程中第一次加入 Na2CO3溶液时反应的离子方程式:_____________ ;
(3)NiS的作用是除去溶液中的Cu2+,原理是NiS+Cu2+=CuS+Ni2+,该反应的平衡常数是_____________ ;
(4)滤液2中加入NaF的作用是除去溶液中的Ca2+、Mg2+,则加入NaF先沉淀的离子是_____________ 。
(5)NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由NiCO3为原料获得,结合上述流程,制备NiSO4•6H2O的操作步骤如下:
①向被有机萃取剂萃取后所得的水层中加入足量Na2CO3溶液(流程中第二次加Na2CO3溶液),搅拌,得NiCO3沉淀:
②___________________________ ;
③___________________________ ;
④蒸发、冷却结晶并从溶液中分离出晶体;
⑤用少量乙醇洗涤并晾干。
确定步骤①中Na2CO3溶液足量,碳酸镍已完成沉淀的简单方法是:_____________ ;
补充完整上述步骤②和③【可提供的试剂有6mol/L的H2SO4溶液,蒸馏水、pH试纸】。

已知:(Ⅰ)含镍浸出液的成分及离子沉淀的pH:

(Ⅱ)溶度积常数:

(1)镍矿渣中镍元素的主要存在形式是Ni(OH)2、NiS,写出浸取时NiS反应的离子方程式
(2)黄钠铁钒[NaFe3(SO4)2(OH)6]具有沉淀颗粒大、沉淀速度快,容易过滤等特点,常用于除铁。写出流程中第一次加入 Na2CO3溶液时反应的离子方程式:
(3)NiS的作用是除去溶液中的Cu2+,原理是NiS+Cu2+=CuS+Ni2+,该反应的平衡常数是
(4)滤液2中加入NaF的作用是除去溶液中的Ca2+、Mg2+,则加入NaF先沉淀的离子是
(5)NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由NiCO3为原料获得,结合上述流程,制备NiSO4•6H2O的操作步骤如下:
①向被有机萃取剂萃取后所得的水层中加入足量Na2CO3溶液(流程中第二次加Na2CO3溶液),搅拌,得NiCO3沉淀:
②
③
④蒸发、冷却结晶并从溶液中分离出晶体;
⑤用少量乙醇洗涤并晾干。
确定步骤①中Na2CO3溶液足量,碳酸镍已完成沉淀的简单方法是:
补充完整上述步骤②和③【可提供的试剂有6mol/L的H2SO4溶液,蒸馏水、pH试纸】。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】一种利用钛铁矿(主要成分为FeTiO3,还含有少量Fe2O3)联合生产铁红和钛白粉的工艺流程如图所示,回答下列问题:
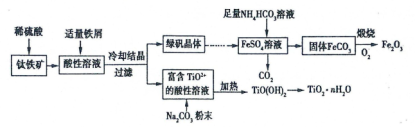
(1)为加快钛铁矿在稀硫酸中的溶解,可采取的措施有______ 任写两种)。
(2)FeSO4溶液与 NH4HCO3溶液反应的离子方程式是________ 。
(3)TiO2+水解为TiO(OH)2沉淀的离子方程式为__________ ,需要加入Na2CO3粉末的目的是__________________________________________ 。
(4)常温下,在生成的FeCO3达到沉淀溶解平衡的溶液中,测得溶液中c(CO32-) = 3.0×10-6 mol/L,需要控制溶液pH____________ 时,才能使所得的FeCO3中不含Fe(OH)2。(已知:Ksp[FeCO3] = 3.0×10-11,Ksp[Fe(OH)2] = 1.0×10-16)

(1)为加快钛铁矿在稀硫酸中的溶解,可采取的措施有
(2)FeSO4溶液与 NH4HCO3溶液反应的离子方程式是
(3)TiO2+水解为TiO(OH)2沉淀的离子方程式为
(4)常温下,在生成的FeCO3达到沉淀溶解平衡的溶液中,测得溶液中c(CO32-) = 3.0×10-6 mol/L,需要控制溶液pH
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上以软锰矿(主要成分为MnO2,还含有少量Fe2O3)和辉钼矿(主要成分为MoS2,还含有少量Si、Ni的氧化物)为原料,制备四钼酸铵晶体[(NH4)2Mo4O13 2H2O]和硫酸锰晶体的工艺流程如下:
2H2O]和硫酸锰晶体的工艺流程如下: 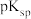 分别为19.4和12.6;
分别为19.4和12.6; 。
。
回答下列问题:
(1)为了提高焙烧效率,可以采取的措施有___________ (写一条即可);“高温焙烧”时MnO2、MoS2转化为MnMoO4、MnSO4,写出该反应的化学方程式___________ 。
(2)“除铁”过程中加入碳酸钠调节溶液的pH至2,生成难溶于水的黄钠铁矾[NaFe3(SO4)2(OH)6],写出该反应的离子方程式___________ 。
(3)“除铁”后的溶液中c(Mn2+)=0.5 mol L-1,当溶液中可溶组分浓度c≤10-5mol
L-1,当溶液中可溶组分浓度c≤10-5mol L-1时,可认为已除尽,则“除镍”应控制溶液pH的范围是
L-1时,可认为已除尽,则“除镍”应控制溶液pH的范围是___________ [已知pc(S2-)=-lgc(S2-),该溶液中pc(S2-)和pH的关系为pc(S2-)=15.1-pH;忽略溶液体积变化]。
(4)硫酸锰在不同温度下的溶解度和该温度范围内析出晶体的组成如下图所示。从过滤所得的滤液中获得较高纯度MnSO4 H2O的操作是:控制温度在80~90 ℃之间蒸发结晶,
H2O的操作是:控制温度在80~90 ℃之间蒸发结晶,___________ ,使固体MnSO4 H2O与溶液分离,
H2O与溶液分离,___________ ,真空干燥。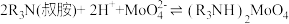 ,则“反萃取”中的试剂X最适宜选用
,则“反萃取”中的试剂X最适宜选用___________ (填标号)。
a.稀硫酸 b.(NH4)2SO4溶液 c.NaOH溶液 d.氨水
从“母液”中回收的副产品主要是___________ (填名称)。
 2H2O]和硫酸锰晶体的工艺流程如下:
2H2O]和硫酸锰晶体的工艺流程如下: 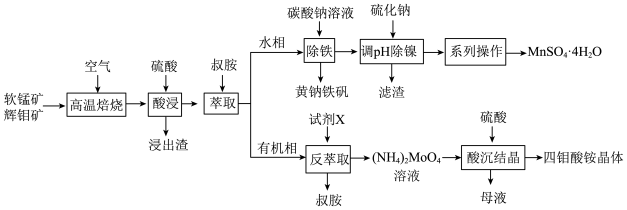
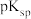 分别为19.4和12.6;
分别为19.4和12.6; 。
。回答下列问题:
(1)为了提高焙烧效率,可以采取的措施有
(2)“除铁”过程中加入碳酸钠调节溶液的pH至2,生成难溶于水的黄钠铁矾[NaFe3(SO4)2(OH)6],写出该反应的离子方程式
(3)“除铁”后的溶液中c(Mn2+)=0.5 mol
 L-1,当溶液中可溶组分浓度c≤10-5mol
L-1,当溶液中可溶组分浓度c≤10-5mol L-1时,可认为已除尽,则“除镍”应控制溶液pH的范围是
L-1时,可认为已除尽,则“除镍”应控制溶液pH的范围是(4)硫酸锰在不同温度下的溶解度和该温度范围内析出晶体的组成如下图所示。从过滤所得的滤液中获得较高纯度MnSO4
 H2O的操作是:控制温度在80~90 ℃之间蒸发结晶,
H2O的操作是:控制温度在80~90 ℃之间蒸发结晶, H2O与溶液分离,
H2O与溶液分离,
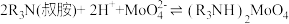 ,则“反萃取”中的试剂X最适宜选用
,则“反萃取”中的试剂X最适宜选用a.稀硫酸 b.(NH4)2SO4溶液 c.NaOH溶液 d.氨水
从“母液”中回收的副产品主要是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】用工业废渣(主要含有Fe2O3、FeO、Al2O3及少量Fe)制备FeSO4·7H2O的流程如下:

(1)“浸泡”过程中反应的离子方程式为___________ 。
(2) “还原”时,FeS2(难溶于水,铁为+2价)与溶液中的Fe2(SO4)3反应,产物为FeSO4和H2SO4,该反应的离子方程式为___________ 。
(3)检验“还原”反应已经完全的方法是___________ 。
(4)由“还原”所得溶液制取FeSO4·7H2O晶体的操作过程为___________ 。
(5)将FeSO4·7H2O在空气中加热分解所得气体冷却后可得绿矾油,绿矾油就是硫酸。验证绿矾油是硫酸的实验方法是___________ 。

(1)“浸泡”过程中反应的离子方程式为
(2) “还原”时,FeS2(难溶于水,铁为+2价)与溶液中的Fe2(SO4)3反应,产物为FeSO4和H2SO4,该反应的离子方程式为
(3)检验“还原”反应已经完全的方法是
(4)由“还原”所得溶液制取FeSO4·7H2O晶体的操作过程为
(5)将FeSO4·7H2O在空气中加热分解所得气体冷却后可得绿矾油,绿矾油就是硫酸。验证绿矾油是硫酸的实验方法是
您最近一年使用:0次
【推荐2】以软锰矿(主要成分为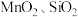 等)为原料制备高纯
等)为原料制备高纯 的流程如下:
的流程如下:
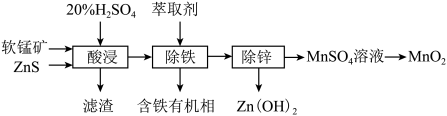
(1)为了提高酸浸速率,可以采取的措施有___________ 。
(2)酸浸时,通常加入 作催化剂加快反应速率。滤渣中含大量硫单质,酸浸时主要反应的化学方程式:
作催化剂加快反应速率。滤渣中含大量硫单质,酸浸时主要反应的化学方程式:___________ 。
(3)“除铁”操作名称为___________ ,所需玻璃仪器为___________ 。
(4)酸性条件下,用合适的氧化剂可以将 转化为高纯
转化为高纯 。
。
①用 作氧化剂时会同时产生
作氧化剂时会同时产生 ,该反应的离子方程式:
,该反应的离子方程式:___________ 。
②反应中 的用量不宜过多的原因是
的用量不宜过多的原因是___________ 。
③用适量的 作氧化剂,反应后溶液中无锰元素剩余。理论上消耗
作氧化剂,反应后溶液中无锰元素剩余。理论上消耗 与生成
与生成 的
的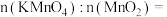
___________ 。
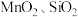 等)为原料制备高纯
等)为原料制备高纯 的流程如下:
的流程如下:
(1)为了提高酸浸速率,可以采取的措施有
(2)酸浸时,通常加入
 作催化剂加快反应速率。滤渣中含大量硫单质,酸浸时主要反应的化学方程式:
作催化剂加快反应速率。滤渣中含大量硫单质,酸浸时主要反应的化学方程式:(3)“除铁”操作名称为
(4)酸性条件下,用合适的氧化剂可以将
 转化为高纯
转化为高纯 。
。①用
 作氧化剂时会同时产生
作氧化剂时会同时产生 ,该反应的离子方程式:
,该反应的离子方程式:②反应中
 的用量不宜过多的原因是
的用量不宜过多的原因是③用适量的
 作氧化剂,反应后溶液中无锰元素剩余。理论上消耗
作氧化剂,反应后溶液中无锰元素剩余。理论上消耗 与生成
与生成 的
的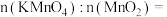
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某铝土矿中主要含有Al2O3、Al(OH)3、AlO(OH),还含有Fe2O3等杂质。利用拜耳法生产氧化铝的流程如图所示:
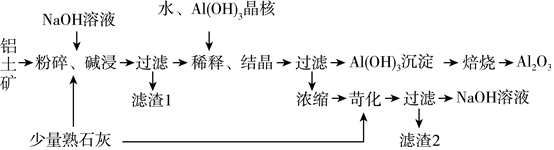
请回答下列问题:
(1)粉碎后的铝土矿碱浸时应在高温下进行,其目的是_______ 。
(2)AlO(OH)与NaOH溶液反应的化学方程式为___________ 。
(3)在稀释、结晶过程中,稀释的目的是_____________ ;加Al(OH)3晶核的目的是促进Al(OH)3的析出。上述“稀释、结晶”工艺,也可用通入足量的________ 气体的方法来代替。
(4)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化反应除去,写出苛化反应的化学方程式:__________ 。
(5)该生产流程能实现________ (填化学式)的循环利用。

请回答下列问题:
(1)粉碎后的铝土矿碱浸时应在高温下进行,其目的是
(2)AlO(OH)与NaOH溶液反应的化学方程式为
(3)在稀释、结晶过程中,稀释的目的是
(4)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化反应除去,写出苛化反应的化学方程式:
(5)该生产流程能实现
您最近一年使用:0次