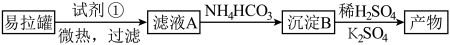有A、B、C、D、E、F、G七种物质,它们的相互转化关系如下图(反应条件略,有些反应的产物和反应的条件没有全部标出)。已知A、B、E是单质,其中A着火只能用干燥的沙土灭火,A在O2中燃烧的产物为G,B在常温下为气体,C俗名称为烧碱,D为无色无味液体。

(1)写出A、F的化学式 A_________ F _________ 。
(2)写出A和D反应生成B和C的化学方程式______________________________ 。
(3)写出E与C、D反应生成的B和F的离子方程式____________________________ 。
(4)写出G与CO2反应的化学方程式____________________________ ,若有1mol的G参加反应,则转移的电子数目为_________ 。

(1)写出A、F的化学式 A
(2)写出A和D反应生成B和C的化学方程式
(3)写出E与C、D反应生成的B和F的离子方程式
(4)写出G与CO2反应的化学方程式
19-20高一上·云南大理·阶段练习 查看更多[8]
云南省大理市下关第一中学2019-2020学年高一上学期第二次段考化学试题辽宁省铁岭市调兵山市第二高级中学2019—2020学年高一下学期线上教学测试化学试题(已下线)第三章 铁 金属材料(基础过关)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)(已下线)第三章 金属及其化合物(基础过关)-2020-2021学年高一化学单元测试定心卷(人教版必修1)(已下线)3.2.1 日常使用的金属材料(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)练习6 日常使用的金属材料2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)(已下线)练习12 从铝土矿到铝合金-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)(已下线)练习5 金属的化学性质-2020-2021学年【补习教材·寒假作业】高一化学(人教版)
更新时间:2019-12-25 18:50:50
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】已知C的相对分子质量比B大16,D为强酸。
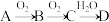
I.若A为淡黄色固体,则:
(1)D的化学式为___________ 。
(2)写出B→C的化学方程式___________ 。
(3)将B通入盛有 溶液的试管中,再滴加少量过氧化氢溶液,现象是
溶液的试管中,再滴加少量过氧化氢溶液,现象是___________ ,说明B具有___________ 性。
II.若A和D可以反应生成盐,则:
(4)A的化学式为___________ ,可用___________ 试纸检验A的存在。
(5)写出C→D的反应中,氧化剂与还原剂的物质的量之比为___________ 。
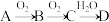
I.若A为淡黄色固体,则:
(1)D的化学式为
(2)写出B→C的化学方程式
(3)将B通入盛有
 溶液的试管中,再滴加少量过氧化氢溶液,现象是
溶液的试管中,再滴加少量过氧化氢溶液,现象是II.若A和D可以反应生成盐,则:
(4)A的化学式为
(5)写出C→D的反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】已知A、B为常见酸的浓溶液;X、Y、Z、W均为氧化物,其中X是红棕色气体,Y的固体可用于人工降雨,W既能使澄清石灰水变浑浊,又能使品红溶液褪色。根据如图所示转化关系(反应条件略),回答下列问题:

(1)Y是___________ (填化学式);实验室收集X气体的方法是___________ 。
(2)将B露置在空气中一段时间,溶液质量增加但溶液浓度减小,表明B具有___________ 性;利用这种性质可以___________ (填序号)。
a.干燥二氧化硫 b.检验 c.干燥氨气 d.钝化铝片
c.干燥氨气 d.钝化铝片
(3)工业尾气中的W可用氨水吸收,反应的化学方程式为___________ 。
(4)反应①中,氧化产物和还原产物的物质的量之比为___________ 。
(5)将A和B混合后稀释,取出10mL混合液,向其中加入足量的 溶液,将生成的沉淀过滤,洗涤,干燥,称得沉淀质量为4.66g;另取10mL混合液与
溶液,将生成的沉淀过滤,洗涤,干燥,称得沉淀质量为4.66g;另取10mL混合液与 的NaOH溶液恰好完全反应。
的NaOH溶液恰好完全反应。
①稀释后的混合液中两种溶质的物质的量浓度分别为___________ 。
②再取10mL稀释后的混合液与0.96g铜粉混合,充分反应(假设只生成一种气体),产生气体的体积为___________ L(标准状况下)。

(1)Y是
(2)将B露置在空气中一段时间,溶液质量增加但溶液浓度减小,表明B具有
a.干燥二氧化硫 b.检验
 c.干燥氨气 d.钝化铝片
c.干燥氨气 d.钝化铝片(3)工业尾气中的W可用氨水吸收,反应的化学方程式为
(4)反应①中,氧化产物和还原产物的物质的量之比为
(5)将A和B混合后稀释,取出10mL混合液,向其中加入足量的
 溶液,将生成的沉淀过滤,洗涤,干燥,称得沉淀质量为4.66g;另取10mL混合液与
溶液,将生成的沉淀过滤,洗涤,干燥,称得沉淀质量为4.66g;另取10mL混合液与 的NaOH溶液恰好完全反应。
的NaOH溶液恰好完全反应。①稀释后的混合液中两种溶质的物质的量浓度分别为
②再取10mL稀释后的混合液与0.96g铜粉混合,充分反应(假设只生成一种气体),产生气体的体积为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】已知A、B、C、D、E、F六种常见物质存在如图所示转化关系(部分生成物和反应条件略去)。

(1)若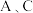 均为氧化物:
均为氧化物:
①若 为单质,向
为单质,向 溶液中滴加
溶液中滴加 溶液,溶液显红色,
溶液,溶液显红色, 为
为___________ (填化学式);写出 的离子方程式:
的离子方程式:___________ 。
②若 是含钠正盐,其水溶液呈碱性,
是含钠正盐,其水溶液呈碱性, 是一种温室气体,写出
是一种温室气体,写出 的一条用途:
的一条用途:___________ ; 的水溶液呈碱性的原因为
的水溶液呈碱性的原因为___________ (用离子方程式表示)。
(2)若 为固体氧化物,
为固体氧化物, 为气体单质,
为气体单质, 进行焰色试验时,火焰呈黄色,写出化合物
进行焰色试验时,火焰呈黄色,写出化合物 的电子式:
的电子式:___________ ;每生成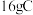 ,转移的电子的物质的量为
,转移的电子的物质的量为___________  。
。
(3)若 为
为 ,写出
,写出 与
与 反应的化学方程式:
反应的化学方程式:___________ 。

(1)若
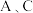 均为氧化物:
均为氧化物:①若
 为单质,向
为单质,向 溶液中滴加
溶液中滴加 溶液,溶液显红色,
溶液,溶液显红色, 为
为 的离子方程式:
的离子方程式:②若
 是含钠正盐,其水溶液呈碱性,
是含钠正盐,其水溶液呈碱性, 是一种温室气体,写出
是一种温室气体,写出 的一条用途:
的一条用途: 的水溶液呈碱性的原因为
的水溶液呈碱性的原因为(2)若
 为固体氧化物,
为固体氧化物, 为气体单质,
为气体单质, 进行焰色试验时,火焰呈黄色,写出化合物
进行焰色试验时,火焰呈黄色,写出化合物 的电子式:
的电子式: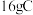 ,转移的电子的物质的量为
,转移的电子的物质的量为 。
。(3)若
 为
为 ,写出
,写出 与
与 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】1.A、B、C、D四种物质之间有如图所示的转化关系。已知:A是空气中的主要成分之一,B、C、D均为化合物,且C为一种红棕色气体。
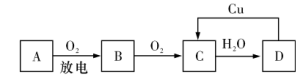
请回答下列问题:
(1)写出B的化学式:___ 。
(2)在D→C的过程中,D表现出强___ (填“氧化性”或“还原性”)。
(3)写出C→D的化学方程式:___ 。
2.汽车尾气中含有NO,在汽车尾气排放管中安装一个“催化转换器”(用铂、钯合金作催化剂),可将尾气中另一种有害气体CO跟NO反应转化为无毒气体。写出CO与NO反应的化学方程式:___ 。
3.控制或者减少城市汽车尾气污染的方法还可以有___ 。
a.开发氢能源 b.使用电动车 c.使用含铅汽油 d.严禁车辆行驶

请回答下列问题:
(1)写出B的化学式:
(2)在D→C的过程中,D表现出强
(3)写出C→D的化学方程式:
2.汽车尾气中含有NO,在汽车尾气排放管中安装一个“催化转换器”(用铂、钯合金作催化剂),可将尾气中另一种有害气体CO跟NO反应转化为无毒气体。写出CO与NO反应的化学方程式:
3.控制或者减少城市汽车尾气污染的方法还可以有
a.开发氢能源 b.使用电动车 c.使用含铅汽油 d.严禁车辆行驶
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】如图所示,A、B、C、D、E各代表水、锌、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质(已知C是氢氧化钡溶液,B是硫酸铜溶液).常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且A的相对分子(或原子)质量大于D,请填空:
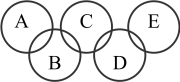
(1)写出下列物质的化学式:A______ 、D______ 、E______ .
(2)写出B与C反应的化学方程式:___________ .
(3)以B为原料,制备CuO,写出具体的化学方程式__________ .
(4)相连环物质间发生的反应中,属于置换反应的是(写出具体化学方程式)___________ .

(1)写出下列物质的化学式:A
(2)写出B与C反应的化学方程式:
(3)以B为原料,制备CuO,写出具体的化学方程式
(4)相连环物质间发生的反应中,属于置换反应的是(写出具体化学方程式)
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】现有原子序数依次增大且小于20的四种主族元素X、Y、Z、W,该四种元素的最外层电子数之和等于18,其中X、Y原子最外层电子数分别是其自身电子层数的2倍、3倍,W的单质会与水剧烈反应,W的简单离子的电子层结构与Z的简单离子的电子层结构相同,Z单质能使湿润的红色布条褪色。
请回答下列问题:
(1)Y的一种单质具有强氧化性,常用作漂白剂和消毒剂,其名称为___________ ,化合物XZ4的电子式为___________ 。
(2)W的单质与水反应的离子方程式为___________ 。
(3)X、Y的最简单氢化物的稳定性由强到弱的顺序为___________ (用氢化物的化学式表示)。
(4)X、Y、Z、W的原子半径由大到小的顺序为___________ (用元素符号表示)。
请回答下列问题:
(1)Y的一种单质具有强氧化性,常用作漂白剂和消毒剂,其名称为
(2)W的单质与水反应的离子方程式为
(3)X、Y的最简单氢化物的稳定性由强到弱的顺序为
(4)X、Y、Z、W的原子半径由大到小的顺序为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】已知B为碱性氧化物,D为淡黄色固体粉末,F为医疗上治疗胃酸过多的一种药剂;物质的转化关系如图所示,请回答下列问题:

(1)请写出下列物质的化学式:A_____ 、F______ 。
(2)请写出下列反应的方程式:
①D→E(写化学方程式):_____ ;
②C→E(写在水溶液中进行的离子方程式):_____ 。
(3)将4.6gA投入47.8g水中,所得溶液中溶质的质量分数为______ (用百分数表示,保留一位小数)。若把A投入盛有CuSO4的溶液中,溶液中出现______ (填沉淀颜色)沉淀。

(1)请写出下列物质的化学式:A
(2)请写出下列反应的方程式:
①D→E(写化学方程式):
②C→E(写在水溶液中进行的离子方程式):
(3)将4.6gA投入47.8g水中,所得溶液中溶质的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】化合物A由两种元素组成,是一种重要的还原剂,在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3)。将4.80g化合物A隔绝空气加热至完全分解,得到金属单质X和2.24L的气体Y;所得单质X与水反应又得到2.24L气体Y和强碱溶液Z(题中气体体积均已折算为标准状况)。
回答下列问题:
(1)气体Y的分子式为_______ ;
(2)单质X与水反应的化学方程式_______ ;
(3)化合物A在钢铁制品脱锈过程发生反应的化学方程式_______ ;
(4)化合物A化学活性很高,在潮湿空气中能自燃。若着火,_______ (填“能”或“不能”)用二氧化碳灭火;若不能,写出原因_______ (用化学方程式表示)。
回答下列问题:
(1)气体Y的分子式为
(2)单质X与水反应的化学方程式
(3)化合物A在钢铁制品脱锈过程发生反应的化学方程式
(4)化合物A化学活性很高,在潮湿空气中能自燃。若着火,
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】位于遵义市播州区的南白铝厂以电解生产铝为主。由于铝具有外观漂亮,不易被腐蚀,质轻等优点,目前在国际市场上的应用越来越广泛。
(1)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层。
①Al在周期表中的位置是:_______ 。
②写出NaOH溶液溶解钢制品表面的铝镀层的离子方程式_______ 。
③钢制品上电镀铝的电镀装置中钢制品位于电镀池的_______ 极。
(2)如图是实验室模拟南白铝厂从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并制取Al的流程:

①用NaOH溶解过程中,通常将铝土矿粉碎,其目的是_______ 。
②“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应:2Na2SiO3+2NaAlO2+2H2O=Na2Al2Si2O8↓+4NaOH,“赤泥”的主要成分为_______ 写 出化学式)。
③“酸化”时,通入过量CO2与NaAlO2反应,写出该反应化学方程式_______ 。
④过滤需要的玻璃仪器有_______ 。
(3)电解是电解熔融的Al2O3,电解过程中阴极的电极反应式为_______ 。
(1)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层。
①Al在周期表中的位置是:
②写出NaOH溶液溶解钢制品表面的铝镀层的离子方程式
③钢制品上电镀铝的电镀装置中钢制品位于电镀池的
(2)如图是实验室模拟南白铝厂从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并制取Al的流程:

①用NaOH溶解过程中,通常将铝土矿粉碎,其目的是
②“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应:2Na2SiO3+2NaAlO2+2H2O=Na2Al2Si2O8↓+4NaOH,“赤泥”的主要成分为
③“酸化”时,通入过量CO2与NaAlO2反应,写出该反应化学方程式
④过滤需要的玻璃仪器有
(3)电解是电解熔融的Al2O3,电解过程中阴极的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】含镁3%~5%的铝镁合金是轮船制造、化工生产、机械制造等行业的重要原料。现有一块质量为m g的铝镁合金,欲测定其中镁的质量分数,几位同学设计了以下不同的实验方案:
方案1:铝镁合金与足量盐酸反应,测定气体的质量为m 1g。
方案2:铝镁合金与足量氢氧化钠溶液反应,过滤、洗涤、烘干,测定剩余固体质量w1 g。
方案3:铝镁合金与过量的盐酸反应,在溶液中加入过量的氢氧化钠溶液,过滤、洗涤、灼烧,测定固体的质量w2 g。(说明:Al (OH)3 既可以与酸反应,也可以与碱反应)
(1)某化学实验小组利用如图所示的装置,按照方案1进行了实验。
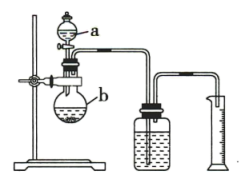
实验装置中有两处明显错误,请指出至少一种:_______ 。
(2)方案2中的化学方程式为_______ 。
(3)方案3中“过滤”操作中用到玻璃棒,玻璃棒的作用是_______ ,若按方案3进行实验,测得的镁的质量分数为_______ 。
方案1:铝镁合金与足量盐酸反应,测定气体的质量为m 1g。
方案2:铝镁合金与足量氢氧化钠溶液反应,过滤、洗涤、烘干,测定剩余固体质量w1 g。
方案3:铝镁合金与过量的盐酸反应,在溶液中加入过量的氢氧化钠溶液,过滤、洗涤、灼烧,测定固体的质量w2 g。(说明:Al (OH)3 既可以与酸反应,也可以与碱反应)
(1)某化学实验小组利用如图所示的装置,按照方案1进行了实验。

实验装置中有两处明显错误,请指出至少一种:
(2)方案2中的化学方程式为
(3)方案3中“过滤”操作中用到玻璃棒,玻璃棒的作用是
您最近一年使用:0次