已知常温下,硫化物的沉淀在溶液中达溶解平衡时,金属阳离子的浓度随S2-浓度的变化曲线如图所示。据图判断,下列说法错误的是


| A.三种物质的溶度积大小为Ksp(CuS)<Ksp(CdS)<Ksp(SnS) |
| B.向SnS悬浊液中加入少量CuSO4固体,c(Sn2+)会减少 |
| C.a点无CdS沉淀产生 |
| D.向含等物质的量浓度的Cu2+、Sn2-的混合液中,滴加Na2S溶液,先析出CuS沉淀 |
更新时间:2019/12/24 08:51:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关BaSO4沉淀的溶解平衡状态的说法中,正确的是
| A.BaSO4沉淀的生成和溶解不断进行,但速率相等 |
B.BaSO4难溶于水,溶液中没有Ba2+和SO |
| C.升高温度,BaSO4的溶解度不变 |
| D.向BaSO4沉淀的溶解平衡体系中加入NaSO4固体,BaSO4的溶解度不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.在一定温度下的饱和AgCl水溶液中,Ag+与Cl-的浓度乘积是一个常数 |
| B.已知AgCl的Ksp=1.8×10-10,则在任何含AgCl固体的溶液中,c(Ag+)=c(Cl-),且Ag+与Cl-浓度的乘积等于1.8×10-10mol2·L-2 |
| C.Ksp数值越大的难溶电解质在水中的溶解能力越强 |
| D.难溶电解质的溶解度很小,故外界条件改变,对它的溶解度没有影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列图示与对应的叙述符合的是
A.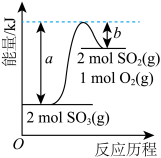 由图可知,2SO3(g) 由图可知,2SO3(g) 2SO2(g)+O2(g) ΔH=(b−a) kJ·mol−1 2SO2(g)+O2(g) ΔH=(b−a) kJ·mol−1 |
B.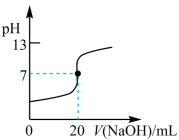 表示常温下,0.100 0 mol·L−1 NaOH溶液滴定20.00 mL 0.100 0 mol·L−1醋酸溶液的滴定曲线 表示常温下,0.100 0 mol·L−1 NaOH溶液滴定20.00 mL 0.100 0 mol·L−1醋酸溶液的滴定曲线 |
C.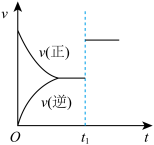 表示反应2HI(g) 表示反应2HI(g) H2(g) +I2(g)的速率随时间变化的图象,在t1时刻改变的条件一定是加入催化剂 H2(g) +I2(g)的速率随时间变化的图象,在t1时刻改变的条件一定是加入催化剂 |
D. 表示一定温度下,溴化银在水中的沉淀溶解平衡曲线,其中a点代表的是不饱和溶液,b点代表的是饱和溶液 表示一定温度下,溴化银在水中的沉淀溶解平衡曲线,其中a点代表的是不饱和溶液,b点代表的是饱和溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列装置或操作能达到相应实验目的的是


A.甲装置用于酸性 溶液滴定 溶液滴定 溶液 溶液 |
B.乙装置用于判断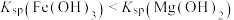 ,且 ,且 可转化成 可转化成 |
| C.丙装置可用于吸收氨气,且能防止倒吸 |
| D.丁装置可用于除去氯气中的HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】由实验操作和现象,可得出相应正确结论的是
| 实验操作 | 现象 | 结论 | |
| A. | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的Cu(OH)2悬浊液 | 无砖红色沉淀 | 蔗糖未发生水解 |
| B. | 向碳酸钠溶液中加入浓盐酸,将产生的气体通入苯酚钠溶液中 | 溶液变浑浊 | 酸性:碳酸>苯酚 |
| C. | 检验铁锈中是否含有二价铁 | 将铁锈溶于浓盐酸,滴入KMnO4溶液,紫色褪去 | 铁锈中含有二价铁 |
| D. | 向 溶液中滴入2滴 溶液中滴入2滴 溶液,再滴入2滴 溶液,再滴入2滴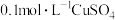 溶液 溶液 | 先产生白色沉淀,滴入 溶液后白色沉淀逐渐变为蓝色 溶液后白色沉淀逐渐变为蓝色 |  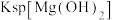 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】硫酸锶(SrSO4)常用于烟火和陶瓷工业,可在Na2SO4溶液中加入锶盐溶液沉淀而得。下图表示不同温度下,SrSO4溶液中lg[c( Sr2+)]与lg[c( SO42-)]之间的关系。下列有关说法正确的是


| A.图象中a 、c两点的溶度积Ksp ( a ) < Ksp ( c ) |
| B.363K时Ksp (SrSO4) = 1.0×10ˉ3.2 |
| C.SrSO4的溶解度随温度升高而增大 |
| D.313K时,b点对应的溶液为饱和溶液,d点对应的溶液为不饱和溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
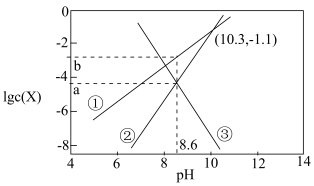
【推荐2】天然溶洞的形成与水体中含碳物种的浓度有密切关系。已知Ksp(CaCO3)=10-8.7,某溶洞水体中lgc(X)(X为 、
、 或Ca2+)与pH变化的关系如下图所示。下列说法错误的是
或Ca2+)与pH变化的关系如下图所示。下列说法错误的是
 、
、 或Ca2+)与pH变化的关系如下图所示。下列说法错误的是
或Ca2+)与pH变化的关系如下图所示。下列说法错误的是
A.曲线②代表 |
| B.Ka2(H2CO3)的数量级为10-11 |
| C.a=-4.35,b=-2.75 |
| D.pH=10.3时,c(Ca2+)=10-7.6 mol·L-1 |
您最近一年使用:0次

 是弱电解质,可以用
是弱电解质,可以用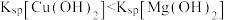 ,向含
,向含 混合溶液中滴加少量NaOH溶液,产生蓝色沉淀
混合溶液中滴加少量NaOH溶液,产生蓝色沉淀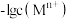 ]与溶液pH的变化关系如图(当溶液中离子浓度小于
]与溶液pH的变化关系如图(当溶液中离子浓度小于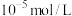 ,认为已完全除去)。
,认为已完全除去)。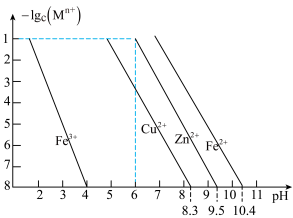

 溶液中的
溶液中的
 ,无法完全除去工业废水中的
,无法完全除去工业废水中的

