某温度下,在一密闭容器中发生如下可逆反应: ;
; 若起始时E浓度为a
若起始时E浓度为a  ,F、G浓度均为0,达平衡时E浓度为 0.5a
,F、G浓度均为0,达平衡时E浓度为 0.5a ;若E的起始浓度改为 2a
;若E的起始浓度改为 2a  ,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
 ;
; 若起始时E浓度为a
若起始时E浓度为a  ,F、G浓度均为0,达平衡时E浓度为 0.5a
,F、G浓度均为0,达平衡时E浓度为 0.5a ;若E的起始浓度改为 2a
;若E的起始浓度改为 2a  ,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是| A.升高温度时,正反应速率加快、逆反应速率减慢 |
B.若 ,容器体积保持不变,新平衡下E的体积分数为 ,容器体积保持不变,新平衡下E的体积分数为 |
C.若 ,容器体积保持不变,新平衡下F的平衡浓度小于 ,容器体积保持不变,新平衡下F的平衡浓度小于  |
D.若 ,容器压强保持不变,新平衡下E的物质的量为a mol ,容器压强保持不变,新平衡下E的物质的量为a mol |
9-10高一下·浙江·期末 查看更多[18]
(已下线)2019年9月24日 《每日一题》2020年高考一轮复习-化学平衡的移动第22届(2008年)全国高中学生化学竞赛(河南省赛区)预赛试题江西省南昌市第二中学2020-2021学年高二上学期期中考试化学试题山东省济宁市微山一中2020-2021学年高二上学期第一次月考化学试题江西省高安中学2020-2021学年高二第一次段考化学(B)试题河北省衡水市深州市中学2020届高三第一次月考化学试题2019年秋高三化学复习强化练习—— 等效平衡2019年秋高三化学复习强化练习—— 等效平衡安徽省六安市二中2018-2019学年高二第一学期10月月考化学试题福建省永春县第一中学2018-2019学年高二上学期期末考试(理)化学试题【全国百强校】福建省厦门市双十中学2018-2019学年高二下学期第一次月考化学试题(已下线)2019高考备考二轮复习精品资料-专题9 化学反应速率与化学平衡(押题专练)陕西省西安市远东第一中学2018-2019学年高二上学期期中考试化学试题(已下线)2018年9月25日《每日一题》一轮复习-化学平衡的移动(已下线)二轮复习 专题9 化学反应速率与化学平衡 押题专练(已下线)2011届江苏省宿豫中学高三第二次模拟考试化学试卷(已下线)09~10年瑞安中学高一下学期期末考试(理)化学卷2016届山东省枣庄第三中学高三上10月阶段质检化学试卷
更新时间:2019-12-27 23:15:35
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学反应2A(g) B(g)+D(g)在四种不同条件下的恒容密闭容器中进行,B、D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表所示:
B(g)+D(g)在四种不同条件下的恒容密闭容器中进行,B、D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表所示:
下列说法错误的是
 B(g)+D(g)在四种不同条件下的恒容密闭容器中进行,B、D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表所示:
B(g)+D(g)在四种不同条件下的恒容密闭容器中进行,B、D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表所示:实验 序号 | 浓度/mol·L-1 温度/°C | 时间/min | ||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | ||
| I | 800 | 1.00 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| II | 800 | 1.00 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| III | 800 | c | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| IV | 820 | 1.00 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| A.实验I中10~20min内的平均反应速率v(B)=0.013mol·L-1·min-1 |
| B.实验II与实验I条件不同,可能是使用了催化剂 |
| C.实验III中c=1.20 |
| D.比较实验I和实验IV可知,该反应为吸热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】 催化加氢制甲醇过程中的主要反应有:
催化加氢制甲醇过程中的主要反应有:
反应I:

反应II:

压强分别为 、
、 时,将
时,将 的混合气体置于恒容密闭容器中反应,不同温度下平衡时体系中
的混合气体置于恒容密闭容器中反应,不同温度下平衡时体系中 转化率和
转化率和 (或CO)选择性如图所示,
(或CO)选择性如图所示, (或CO)的选择性可表示为
(或CO)的选择性可表示为 ,下列说法正确的是
,下列说法正确的是

 催化加氢制甲醇过程中的主要反应有:
催化加氢制甲醇过程中的主要反应有:反应I:


反应II:


压强分别为
 、
、 时,将
时,将 的混合气体置于恒容密闭容器中反应,不同温度下平衡时体系中
的混合气体置于恒容密闭容器中反应,不同温度下平衡时体系中 转化率和
转化率和 (或CO)选择性如图所示,
(或CO)选择性如图所示, (或CO)的选择性可表示为
(或CO)的选择性可表示为 ,下列说法正确的是
,下列说法正确的是
| A.曲线①代表的是CO选择性 |
B.反应  |
C.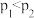 |
| D.其他条件不变,增大压强,CO选择性变小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
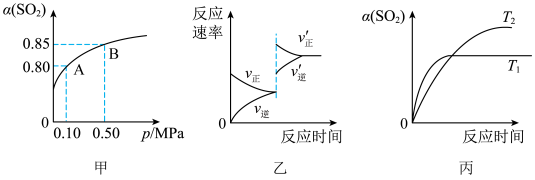
【推荐3】已知反应:2SO2(g)+O2(g) 2SO3(g) △H<0。某温度下,将2molSO2和1molO2置于10L密闭容器中,反应到达平衡后,SO2的平衡转化率(a)与体系总压强(p)的关系如图甲所示。则下列说法错误的是
2SO3(g) △H<0。某温度下,将2molSO2和1molO2置于10L密闭容器中,反应到达平衡后,SO2的平衡转化率(a)与体系总压强(p)的关系如图甲所示。则下列说法错误的是
 2SO3(g) △H<0。某温度下,将2molSO2和1molO2置于10L密闭容器中,反应到达平衡后,SO2的平衡转化率(a)与体系总压强(p)的关系如图甲所示。则下列说法错误的是
2SO3(g) △H<0。某温度下,将2molSO2和1molO2置于10L密闭容器中,反应到达平衡后,SO2的平衡转化率(a)与体系总压强(p)的关系如图甲所示。则下列说法错误的是
| A.由图甲推断,A点SO2的平衡浓度为0.04mol/L |
| B.到达平衡后,升高温度,则反应速率变化图像可以用图乙表示 |
| C.到达平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示 |
| D.压强为0.50MPa时不同温度下SO2转化率与温度关系可以用图丙表示 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】相同温度下,甲、乙两个恒容密闭容器中均进行反应: △H<0。实验过程中部分数据如表所示。
△H<0。实验过程中部分数据如表所示。
下列说法错误的是
 △H<0。实验过程中部分数据如表所示。
△H<0。实验过程中部分数据如表所示。| 容器 | 起始容积 | 物质的起始加入量 | 平衡时W的物质的量 |
| 甲 | 5 L | 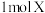 、 、 | 0.6 mol |
| 乙 | 5 L | 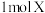 、 、 、 、 、 、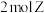 | a |
| A.a>1.8 mol |
| B.平衡时,两容器中Z的物质的量:n(乙)<3n(甲) |
| C.平衡时,两容器内的压强:p(乙)<3p(甲) |
| D.升高乙容器温度,能使甲、乙两容器中X的体积分数相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2,发生如下反应:2SO2(g)+O2(g) 2SO3(g)ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量QkJ。则下列分析正确的是
2SO3(g)ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量QkJ。则下列分析正确的是
 2SO3(g)ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量QkJ。则下列分析正确的是
2SO3(g)ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量QkJ。则下列分析正确的是| A.若反应开始时容器体积为2 L,则v(SO3)=0.35 mol·L-1·min-1 |
| B.2 min后,向容器中再通入一定量的SO3气体,重新达到平衡时,SO2的含量降低 |
| C.若把条件“恒温恒压”改为“恒压绝热”,则平衡后n(SO3)大于1.4 mol |
| D.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于QkJ |
您最近一年使用:0次



