用0.55 mol·L-1 NaOH溶液分别与0.5 mol·L-1的盐酸、醋酸溶液反应,且所取的溶液体积均相等,测出的中和热数值分别为ΔH1和ΔH2,则ΔH1和ΔH2两者的关系正确的是( )
| A.ΔH1>ΔH2 | B.ΔH1=ΔH2 | C.ΔH1<ΔH2 | D.无法比较 |
更新时间:2020-01-01 20:01:43
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】草酸(H2C2O4)是一种常见的二元弱酸,0.010mol/L的H2C2O4溶液中H2C2O4、 和
和 的物质的量分数δ(X)随pH变化如图。下列说法正确的是
的物质的量分数δ(X)随pH变化如图。下列说法正确的是
 和
和 的物质的量分数δ(X)随pH变化如图。下列说法正确的是
的物质的量分数δ(X)随pH变化如图。下列说法正确的是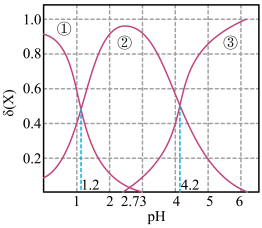
A.曲线①表示 的物质的量分数δ(X)随pH变化关系 的物质的量分数δ(X)随pH变化关系 |
| B.NaHC2O4溶液中c(OH-)>c(H+) |
C.0.01mol/LNaHC2O4溶液中,c( )+c(OH-)=c(H+)+c(H2C2O4) )+c(OH-)=c(H+)+c(H2C2O4) |
D.反应H2C2O4+  2 2 的化学平衡常数为10-5.4 的化学平衡常数为10-5.4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】25℃时,下列溶液中水的电离程度最小的是
A.pH=2的 溶液 溶液 | B.0.01  溶液 溶液 |
C.0.1 NaCl溶液 NaCl溶液 | D.pH=10氨水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
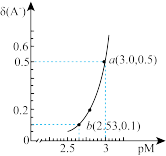
【推荐3】MA2是一种微溶盐,M(OH)2是二元强碱,HA是一元弱酸。25℃时,实验测得随着c(H+)变化,MA2饱和溶液中pM与δ(A-)的关系如图所示,其中a点对应的pH=5.0,[已知pM=-lgc(M2+),δ(A-)= 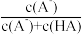 ]。则下列说法错误的是
]。则下列说法错误的是
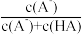 ]。则下列说法错误的是
]。则下列说法错误的是
| A.HA的电离常数Ka为1.0×10-5 |
| B.a点对应溶液中有c(M2+)=c(HA) |
| C.Ksp(MA2)的数量级为10-9 |
| D.b点对应溶液中c(OH-)=9×10-5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验能达到目的的是
| A.测定中和反应的反应热:用酸碱中和滴定法 |
| B.判断醋酸为弱电解质:测定并比较醋酸和盐酸的pH |
| C.用98%浓硫酸配制10%的稀硫酸:仪器为烧杯、玻璃棒 |
| D.测定镀锌铁皮的镀层厚度:将镀锌铁皮放入稀硫酸中,待产生氢气的速率突然减小,可以判断锌镀层已反应完全 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
| A.pH<7的溶液不一定呈酸性 |
| B.中和pH和体积均相等的氨水、NaOH溶液,所需HCl的物质的量相同 |
| C.在相同温度下,pH相等的盐酸、CH3COOH溶液中,c(OH-)相等 |
D.氨水和盐酸反应后的溶液,若溶液呈中性,则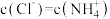 |
您最近一年使用:0次



