2019年诺贝尔化学奖由来自美、英、日的三人分获,以表彰他们在锂离子电池研究方面做出的贡献,他们最早发明用LiCoO2作离子电池的正极,用聚乙炔作负极。回答下列问题:
(1)基态Co原子价电子排布图为______________ (轨道表达式)。第四电离能I4(Co)比I4(Fe)小,是因为_____________________ 。
(2)LiCl的熔点(605℃)比LiF的熔点(848℃)低,其原因是_________________________ .
(3)乙炔(C2H2)分子中δ键与π键的数目之比为_______________ 。
(4)锂离子电池的导电盐有LiBF4等,碳酸亚乙酯(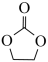 )是一种锂离子电池电解液的添加剂。
)是一种锂离子电池电解液的添加剂。
①LiBF4中阴离子的空间构型是___________ ;与该阴离子互为等电子体的分子有_____________ 。(列一种)
②碳酸亚乙酯分子中碳原子的杂化方式有_______________________ 。
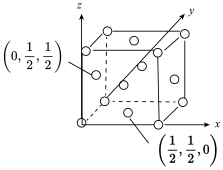
(5)Li2S是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如图所示,已知晶胞参数a=588pm。
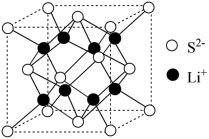
①S2-的配位数为______________ 。
②设NA为阿伏加 德罗常数的值,Li2S的晶胞密度为____________ (列出计算式) 。
。
(1)基态Co原子价电子排布图为
(2)LiCl的熔点(605℃)比LiF的熔点(848℃)低,其原因是
(3)乙炔(C2H2)分子中δ键与π键的数目之比为
(4)锂离子电池的导电盐有LiBF4等,碳酸亚乙酯(
 )是一种锂离子电池电解液的添加剂。
)是一种锂离子电池电解液的添加剂。①LiBF4中阴离子的空间构型是
②碳酸亚乙酯分子中碳原子的杂化方式有
(5)Li2S是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如图所示,已知晶胞参数a=588pm。

①S2-的配位数为
②设NA为阿伏加 德罗常数的值,Li2S的晶胞密度为
 。
。
20-21高三上·云南昆明·阶段练习 查看更多[6]
云南省昆明市第一中学2020届高三上学期12月月考理综试卷化学试题2019年湖北省十堰市高三元月调研考试理综化学试题河北省邢台市2020届高三上学期第四次月考化学试题河南省驻马店市2020届高三上学期期末统一考试化学试题海南省2020届高三下学期新高考线上诊断性测试化学试题(已下线)考点14 物质结构与性质(选考)-2020年高考化学命题预测与模拟试题分类精编
更新时间:2020-01-09 20:47:25
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】硼元素、钙元素、铜元素在化学中有很重要的地位。
(1)已知CaC2与水反应生成乙炔。请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为_______ 。
②CaC2中C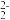 与O
与O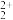 结构相似,1molO
结构相似,1molO 中含有的π键的物质的量为
中含有的π键的物质的量为_______ mol。
③乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是_______ 。
(2)硼酸溶于水生成弱电解质-水合硼酸B(OH)3•H2O,它电离生成少量[B(OH)4]-和H+,则[B(OH)4]-的空间构型为_______ ,含有的化学键类型为_______ (填字母)。
A.共价键 B.离子键 C.金属键 D.配位键
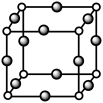
(3)Cu3N的晶胞结构如图,N3-的配位数为_______ ,Cu+半径为apm,N3-半径为bpm,Cu3N的密度为_______ g•cm-3(阿伏加德罗常数用NA表示)
(1)已知CaC2与水反应生成乙炔。请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为
②CaC2中C
 与O
与O 结构相似,1molO
结构相似,1molO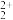 中含有的π键的物质的量为
中含有的π键的物质的量为③乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是
(2)硼酸溶于水生成弱电解质-水合硼酸B(OH)3•H2O,它电离生成少量[B(OH)4]-和H+,则[B(OH)4]-的空间构型为
A.共价键 B.离子键 C.金属键 D.配位键
(3)Cu3N的晶胞结构如图,N3-的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铂(Pt)的单质又称白金,是常用的催化剂和电极材料,含铂配合物是很好的抗癌药物。请回答下列问题:
(1)铂的价电子排布式是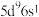 ,用酒精把铂丝润湿后点燃,这时酒精燃烧得特别剧烈,能使铂丝温度达到炽热程度,发出很亮的光,上述现象可能的原因是
,用酒精把铂丝润湿后点燃,这时酒精燃烧得特别剧烈,能使铂丝温度达到炽热程度,发出很亮的光,上述现象可能的原因是_________________ 。
(2)顺二氨环丁羧酸铂( )又名卡铂,是一种低毒性抗癌药,遇光易分解。
)又名卡铂,是一种低毒性抗癌药,遇光易分解。
①卡铂分子中非金属元素的电负性由大到小的顺序为____ ,碳原子的杂化轨道类型有_____________ 。
②卡铂溶于水,不溶于乙醚的原因是_____ ,卡铂静脉注射时需要注意的事项是_______ 。
③卡铂分子中存在的微粒间作用力有_________ (填序号)。
A.离子键 B.配位键 C.金属键 D.非极性键
(3)超硬材料(仅次于金刚石)氮化铂的一种晶胞如图所示,N的配位数是__________ ,若该晶胞的边长为a pm,晶胞的密度为 ,则阿伏加 德罗常数(
,则阿伏加 德罗常数( )为
)为_________  (用a、
(用a、 表示,并化成最简)。
表示,并化成最简)。

(1)铂的价电子排布式是
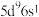 ,用酒精把铂丝润湿后点燃,这时酒精燃烧得特别剧烈,能使铂丝温度达到炽热程度,发出很亮的光,上述现象可能的原因是
,用酒精把铂丝润湿后点燃,这时酒精燃烧得特别剧烈,能使铂丝温度达到炽热程度,发出很亮的光,上述现象可能的原因是(2)顺二氨环丁羧酸铂(
 )又名卡铂,是一种低毒性抗癌药,遇光易分解。
)又名卡铂,是一种低毒性抗癌药,遇光易分解。①卡铂分子中非金属元素的电负性由大到小的顺序为
②卡铂溶于水,不溶于乙醚的原因是
③卡铂分子中存在的微粒间作用力有
A.离子键 B.配位键 C.金属键 D.非极性键
(3)超硬材料(仅次于金刚石)氮化铂的一种晶胞如图所示,N的配位数是
 ,则阿伏加 德罗常数(
,则阿伏加 德罗常数( )为
)为 (用a、
(用a、 表示,并化成最简)。
表示,并化成最简)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钴及其化合物在生产生活中有广泛应用。回答下列问题:
(1)基态钴原子价电子排布式为___________ 。
(2)Co3+在水中易被还原成Co2+,而在氨水中可稳定存在,其原因为___________ 。
(3)[Co(NO3-)4]2-中Co2+的配位数为4,配体中N的杂化方式为___________ ,该配离子中各元素I1由小到大的顺序为___________ (填元素符号),1mol该配离子中含σ键数目为___________ NA。
(4)八面体配合物CoCl3·3NH3结构有___________ 种,其中极性分子有___________ 种。
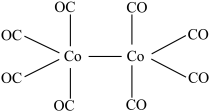
(5)配合物Co2(CO)8的结构如下图,该配合物中存在的作用力类型有___________ (填标号)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
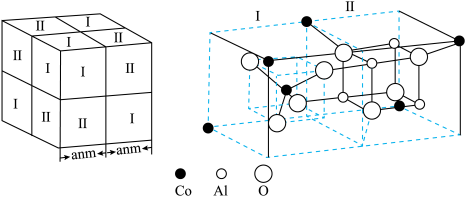
(6)钴蓝晶体结构如下图,该立方晶胞由4个I型和4个Ⅱ型小立方体构成,其化学式为___________ ,晶体中Al3+占据O2-形成的___________ (填“四面体空隙”或“八面体空隙”)。NA为阿伏伽德罗常数的值,钴蓝晶体的密度为___________ g·cm-3(列计算式)。
(1)基态钴原子价电子排布式为
(2)Co3+在水中易被还原成Co2+,而在氨水中可稳定存在,其原因为
(3)[Co(NO3-)4]2-中Co2+的配位数为4,配体中N的杂化方式为
(4)八面体配合物CoCl3·3NH3结构有
(5)配合物Co2(CO)8的结构如下图,该配合物中存在的作用力类型有
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力

(6)钴蓝晶体结构如下图,该立方晶胞由4个I型和4个Ⅱ型小立方体构成,其化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】钛及其化合物在科技、生物、材料领域均有广泛应用。回答下列问题:
(1)基态钛原子核外s能级和p能级的电子数之比为____ ;钛元素处于元素周期表的____ 区。
(2)含钛新型正极材料KTiPO4F具有高化学电位。
①PO 的立体构型为
的立体构型为____ 。与PO 互为等电子体的分子为
互为等电子体的分子为____ (任写一种,填化学式)。
②KTiPO4F中所含元素的第一电离能由大到小的顺序为____ (用元素符号表示)。
③一些氢化物的沸点如表所示:
解释表中氢化物之间沸点存在差异的原因:____ 。
(3)Ti(IV)在酸溶液中可形成多种离子。其中如图1所示结构的离子符号为____ ;[Ti(OH)2(H2O)4]2+中配位键的数目为____ 。
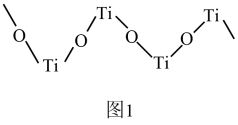
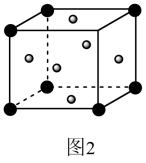
(4)CaTiO3晶体中Ca、O原子在立方晶胞中的位置如图2所示,其中Ti原子填充在O原子围成的____ (填“正八面体”或“正四面体”)空隙中;若阿伏加德罗常数的值为NA,晶体密度为ρg·cm-3,则O原子间的最近距离为____ pm(用含NA、ρ的代数式表示)。
(1)基态钛原子核外s能级和p能级的电子数之比为
(2)含钛新型正极材料KTiPO4F具有高化学电位。
①PO
 的立体构型为
的立体构型为 互为等电子体的分子为
互为等电子体的分子为②KTiPO4F中所含元素的第一电离能由大到小的顺序为
③一些氢化物的沸点如表所示:
| 氢化物 | PH3 | H2O | HF |
| 沸点/℃ | -87.5 | 100 | 19.5 |
(3)Ti(IV)在酸溶液中可形成多种离子。其中如图1所示结构的离子符号为

(4)CaTiO3晶体中Ca、O原子在立方晶胞中的位置如图2所示,其中Ti原子填充在O原子围成的

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】BaTiO3、KH2PO4和NaNO2都属于铁电体,它们具有许多特异的性能如当它受压力而改变形状时产生电流,通电时会改变形状等。
(1)基态Ti原子的价电子排布式为___________ ,属于___________ 区元素。
(2)KH2PO4晶体中存在的作用力有___________ (选填字母)。
A.离子键 B.共价键 C.氢键
(3) NaNO2中N原子的杂化类型为___ ,键角(填“>、<或=”)____ 120°,其原因是___________ 。N、O、Na三种元素的第二电离能(I2)由大到小的顺序为________ (用元素符号表示)。
(4)BaTiO3的晶胞如下图所示:
Ti原子的配位数为_____ ,晶体的密度为ρg/cm3,最近的Ba原子和O原子之间的距离为___ (填计算式)nm。( BaTiO3的摩尔质量为233g/mol,NA为阿伏伽德罗常数的值)
(1)基态Ti原子的价电子排布式为
(2)KH2PO4晶体中存在的作用力有
A.离子键 B.共价键 C.氢键
(3) NaNO2中N原子的杂化类型为
(4)BaTiO3的晶胞如下图所示:
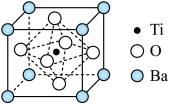
Ti原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氢氧化镍在乙醇的悬浊液中可发生如下反应生成单质镍的配合物:Ni(OH)2+5CH3NC=(CH3NC)4Ni+CH3NCO+H2O
(1)Ni2+基态核外电子排布式为________ 。
(2)CH3NC(其结构简式为CH3- N C)分子中碳原子轨道的杂化类型是
C)分子中碳原子轨道的杂化类型是_____ ;1molCH3NC中σ键的数目为_______ 。
(3)用光气(COCl2)与甲胺(CH3NH2)可以制取CH3NCO。
①与COCl2互为等电子体的一种阴离子为___ 。
②甲胺极易溶于水,除因为它们都是极性分子外,还因为___ 。
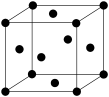
(4)Ni单质的晶胞结构如下图所示,晶体中每个Ni原子周围与之距离最近的原子个数为______ 。
(1)Ni2+基态核外电子排布式为
(2)CH3NC(其结构简式为CH3- N
 C)分子中碳原子轨道的杂化类型是
C)分子中碳原子轨道的杂化类型是(3)用光气(COCl2)与甲胺(CH3NH2)可以制取CH3NCO。
①与COCl2互为等电子体的一种阴离子为
②甲胺极易溶于水,除因为它们都是极性分子外,还因为
(4)Ni单质的晶胞结构如下图所示,晶体中每个Ni原子周围与之距离最近的原子个数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】氮及其化合物与人类生产、生活息息相关。其中尿素(H2NCONH2) 是人类最早合成的有机物,工业上生产尿素的反应为: N2+3H2 2NH3,2NH3+CO2
2NH3,2NH3+CO2 H2NCONH2+H2O。回答下列问题:
H2NCONH2+H2O。回答下列问题:
(1)纳米氧化铜、纳米氧化锌均可作合成氨的催化剂,Cu2+价层电子的轨道表达式为______ ,Zn位于元素周期表的_______ 区。
(2)C、N、O三种元素第一电离能从大到小的顺序是___________ 。
(3)上述化学方程式中的无机化合物,沸点由高到低的顺序是____________ ,原因: ___________ 。
(4)尿素分子中,原子杂化轨道类型有____________ ,σ键与π键数目之比为_______ 。
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼(如图1) 和六方氮化硼(如图2),前者类似于金刚石,后者与石墨相似。
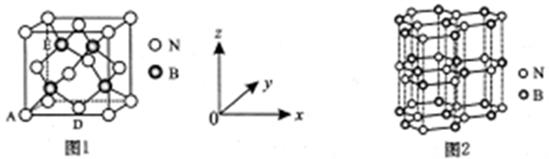
①晶胞中的原子坐标参数可表示晶胞内部各原子的相对位置。图1中原子坐标参数A为(0,0,0),D为(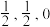 ),则E原子的坐标参数为
),则E原子的坐标参数为_____ 。X-射线衍射实验测得立方氮化硼晶胞参数为361.5pm,则立方氮化硼晶体N 与B的原子半径之和为______ pm。(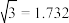 )
)
②已知六方氮化硼同层中B-N距离为acm,密度为dg/cm3,则层与层之间距离的计算表达式为_______ pm。
 2NH3,2NH3+CO2
2NH3,2NH3+CO2 H2NCONH2+H2O。回答下列问题:
H2NCONH2+H2O。回答下列问题:(1)纳米氧化铜、纳米氧化锌均可作合成氨的催化剂,Cu2+价层电子的轨道表达式为
(2)C、N、O三种元素第一电离能从大到小的顺序是
(3)上述化学方程式中的无机化合物,沸点由高到低的顺序是
(4)尿素分子中,原子杂化轨道类型有
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼(如图1) 和六方氮化硼(如图2),前者类似于金刚石,后者与石墨相似。

①晶胞中的原子坐标参数可表示晶胞内部各原子的相对位置。图1中原子坐标参数A为(0,0,0),D为(
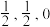 ),则E原子的坐标参数为
),则E原子的坐标参数为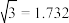 )
)②已知六方氮化硼同层中B-N距离为acm,密度为dg/cm3,则层与层之间距离的计算表达式为
您最近一年使用:0次
【推荐2】【化学——选修3:物质结构与性质】
氮是动植物生长不可缺少的元素,是组成蛋白质的重要元素。氮的化合物在人类社会发展中扮演重要角色,例如,合成氨技术、硝酸及其盐以及新型的材料和能源等。
(1)Li3N晶体中氮以N3-存在,基态N3-的核外电子排布式为____________ 。
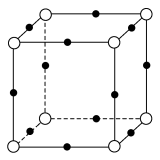
(2)N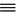 N的键能为942kJ·mol-1, N—N单键的键能为247 kJ·mol-1,计算说明N2中的
N的键能为942kJ·mol-1, N—N单键的键能为247 kJ·mol-1,计算说明N2中的____________ 键比________ 键稳定(填“σ”或“π”)。
(3)(CH3)3NH+和AlCl4- 可形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,阴、阳离子间的作用力大于有机溶剂分子间的范德华力,其挥发性一般比有机溶剂________ (填“大”或“小”),可用作________ (填代号)。
a.助燃剂 b.“绿色”溶剂 c.复合材料 d.绝热材料
(4)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是________ ,与同一个N3-最接近的X+有_________ 个。
(5)据报道:用激光可将置于铁室中的石墨靶上的碳原子“炸松”,再用一个射频电火花喷射出氮气,可使碳、氮原子结合成碳氮化合物的薄膜,氮化碳结构如图,其中β一氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料。下列有关氮化碳的说法不正确的是________ 。

A.氮化碳属于原子晶体 B.该碳氮化合物呈片层状结构
C.氮化碳的化学式为C3N4 D.该碳氮化合物中C一N键键长大于金刚石中C一C键键长
(6)氮和氧元素可以形成多种化合物,比较N和O的电负性:N________ O (填大于、小于);N 和O的第一电离能:N_________ O (填大于、小于)。
氮是动植物生长不可缺少的元素,是组成蛋白质的重要元素。氮的化合物在人类社会发展中扮演重要角色,例如,合成氨技术、硝酸及其盐以及新型的材料和能源等。
(1)Li3N晶体中氮以N3-存在,基态N3-的核外电子排布式为
(2)N
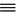 N的键能为942kJ·mol-1, N—N单键的键能为247 kJ·mol-1,计算说明N2中的
N的键能为942kJ·mol-1, N—N单键的键能为247 kJ·mol-1,计算说明N2中的(3)(CH3)3NH+和AlCl4- 可形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,阴、阳离子间的作用力大于有机溶剂分子间的范德华力,其挥发性一般比有机溶剂
a.助燃剂 b.“绿色”溶剂 c.复合材料 d.绝热材料
(4)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是

(5)据报道:用激光可将置于铁室中的石墨靶上的碳原子“炸松”,再用一个射频电火花喷射出氮气,可使碳、氮原子结合成碳氮化合物的薄膜,氮化碳结构如图,其中β一氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料。下列有关氮化碳的说法不正确的是

A.氮化碳属于原子晶体 B.该碳氮化合物呈片层状结构
C.氮化碳的化学式为C3N4 D.该碳氮化合物中C一N键键长大于金刚石中C一C键键长
(6)氮和氧元素可以形成多种化合物,比较N和O的电负性:N
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】CaF2、CaC2都是工业生产的重要物质。回答下列问题:
(1)基态钙原子的电子排布式________ ,钙原子核外有________ 种能量状态的电子。
(2)CaC2与水反应生成乙炔(C2H2),乙炔中的σ键与π键数之比为_______ 。
(3)CaF2与浓H2SO4反应生成HF,HF的沸点高于C2H2,原因是________ 。
(4)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为___________ ,其中氧原子的杂化方式为___________ 。
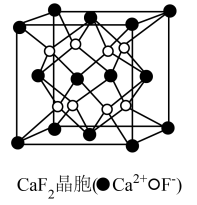
(5)CaF2晶胞结构见图,则距Ca2+最近且等距的F-有________ 个。晶胞中两个F-的最近距离为273.1pm,用NA表示阿伏加德罗常数,则晶胞的密度为________ g·cm-3(列出计算式即可)。
(6)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是________ (用离子方程式表示)。 已知AlF63-在溶液中可稳定存在。
(7)NaF溶液中c(F-)=0.02mol·L-1 ,向其中加入等体积的CaCl2溶液,使 F-沉淀完全,已知 Ksp (CaF2)=3.45×10-11,则所加 CaCl2溶液的浓度最小为_______ mol·L-1 。
(1)基态钙原子的电子排布式
(2)CaC2与水反应生成乙炔(C2H2),乙炔中的σ键与π键数之比为
(3)CaF2与浓H2SO4反应生成HF,HF的沸点高于C2H2,原因是
(4)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为
(5)CaF2晶胞结构见图,则距Ca2+最近且等距的F-有

(6)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是
(7)NaF溶液中c(F-)=0.02mol·L-1 ,向其中加入等体积的CaCl2溶液,使 F-沉淀完全,已知 Ksp (CaF2)=3.45×10-11,则所加 CaCl2溶液的浓度最小为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,据此回答下列问题。
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过___________ 方法区分晶体、准晶体和非晶体;
(2)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是__________________________ ;Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有_______ 个铜原子;
(3)经验规律告诉我们,当成键的两个原子电负性χ的差值Δχ大于1.7时,原子间一般形成的是离子键;Δχ小于1.7时,原子间一般形成的是共价键。已知χ(Fe)=1.8,χ(Cl)=3.1,据此推断化合物FeCl3中Fe-Cl键的共用电子对偏向______ 原子(填名称),FeCl3属于__________ (填“共价化合物”或“离子化合物”);
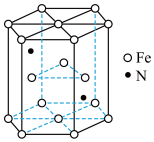
(4)某种磁性氮化铁的结构如图所示,N随机排列在Fe构成的正四面体空隙中。正六棱柱底边长为a cm,高为c cm,阿伏加 德罗常数的值为NA,则该磁性氮化铁的晶体密度为__________ g/cm3(用代数式表示)。
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是
(3)经验规律告诉我们,当成键的两个原子电负性χ的差值Δχ大于1.7时,原子间一般形成的是离子键;Δχ小于1.7时,原子间一般形成的是共价键。已知χ(Fe)=1.8,χ(Cl)=3.1,据此推断化合物FeCl3中Fe-Cl键的共用电子对偏向
(4)某种磁性氮化铁的结构如图所示,N随机排列在Fe构成的正四面体空隙中。正六棱柱底边长为a cm,高为c cm,阿伏加 德罗常数的值为NA,则该磁性氮化铁的晶体密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
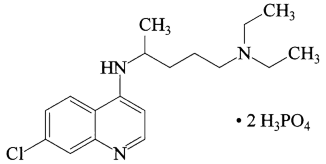
【推荐2】磷酸氯喹在细胞水平上能有效抑制新型冠状病毒(SARS-CoV-2)的感染。磷酸氯喹的结构如图所示,据此回答下列问题。
(1)基态P原子中,电子占据的最高能级符号为___ ,基态N原子核外有__ 种运动状态不同的电子。
(2)C、N、O三种元素电负性从大到小的顺序为___ ;第一电离能χ(P)__ χ(Cl)(填“>”或“<”)。
(3)磷酸氯喹中N原子的杂化方式为__ ,NH3是一种极易溶于水的气体,其沸点比AsH3的沸点高,其原因是___ 。
(4)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体碳化硅类似,熔点如表所示,
①GaN、GaP、GaAs的熔点变化原因是___ 。
②砷化镓晶体中含有的化学键类型为___ (填选项字母)。
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
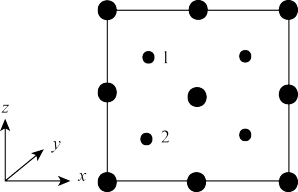
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置。称作原子分数坐标。如图为沿y轴投影的磷化镓晶胞中所有原子的分布图。若原子1的原子分数坐标为(0.25,0.25,0.75),则原子2的原子分数坐标为___ ;若磷化镓的晶体密度为ρg·cm-3,阿伏加德罗常数的值为NA,则晶胞中Ga和P原子的最近距离为___ pm(用代数式表示)。

(1)基态P原子中,电子占据的最高能级符号为
(2)C、N、O三种元素电负性从大到小的顺序为
(3)磷酸氯喹中N原子的杂化方式为
(4)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体碳化硅类似,熔点如表所示,
| GaN | GaP | GaAs | |
| 熔点/℃ | 1700 | 1480 | 1238 |
②砷化镓晶体中含有的化学键类型为
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置。称作原子分数坐标。如图为沿y轴投影的磷化镓晶胞中所有原子的分布图。若原子1的原子分数坐标为(0.25,0.25,0.75),则原子2的原子分数坐标为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】超分子化学已逐渐扩展到化学的各个分支,还扩展到生命科学和物理学等领域。由Mo将2个 分子、2个p一甲酸丁酯吡啶分子及2个CO分子利用配位键自组装的超分子结构如图1所示。
分子、2个p一甲酸丁酯吡啶分子及2个CO分子利用配位键自组装的超分子结构如图1所示。
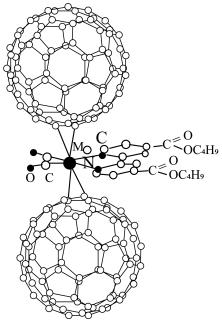
(1)Mo位于第5周期ⅥB族,基态原子核外电子排布与Cr相似,则基态Mo原子的价电子排布式为___________ 。
(2)该超分子中存在的化学键类型有___________(填字母)
(3)配体CO中提供孤电子对的原子是___________ (填元素符号);p—甲酸丁酯吡啶配体中C原子的杂化方式有___________ 。
(4)从电负性角度解释 的酸性强于
的酸性强于 的原因
的原因___________ 。
(5)已知:某晶胞中各原子的相对位置可用如图2所示的原子坐标表示,其中所有顶点原子坐标均为(0,0,0)。钼(Mo)的一种立方晶系的晶体结构中,每个晶胞有2个Mo原子,其中Mo原子坐标是(0,0,0)及( ,
, ,
, )。根据以上信息,推断该晶体的原子堆积方式是
)。根据以上信息,推断该晶体的原子堆积方式是___________ 。已知该晶体的密度是 ,Mo的摩尔质量是
,Mo的摩尔质量是 ,阿伏加德罗常数的值是NA,晶体中距离最近的Mo原子核之间的距离为
,阿伏加德罗常数的值是NA,晶体中距离最近的Mo原子核之间的距离为___________ pm。
(6) 与金刚石互为同素异形体,从结构与性质之间的关系解释
与金刚石互为同素异形体,从结构与性质之间的关系解释 的熔点远低于金刚石的原因是
的熔点远低于金刚石的原因是___________ 。金刚石晶胞含有___________ 个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=___________ a,列式表示碳原子在晶胞中的空间占有率___________ (列出表达式即可)。
 分子、2个p一甲酸丁酯吡啶分子及2个CO分子利用配位键自组装的超分子结构如图1所示。
分子、2个p一甲酸丁酯吡啶分子及2个CO分子利用配位键自组装的超分子结构如图1所示。
(1)Mo位于第5周期ⅥB族,基态原子核外电子排布与Cr相似,则基态Mo原子的价电子排布式为
(2)该超分子中存在的化学键类型有___________(填字母)
| A.σ键 | B.π键 | C.离子键 | D.氢键 |
(4)从电负性角度解释
 的酸性强于
的酸性强于 的原因
的原因(5)已知:某晶胞中各原子的相对位置可用如图2所示的原子坐标表示,其中所有顶点原子坐标均为(0,0,0)。钼(Mo)的一种立方晶系的晶体结构中,每个晶胞有2个Mo原子,其中Mo原子坐标是(0,0,0)及(
 ,
, ,
, )。根据以上信息,推断该晶体的原子堆积方式是
)。根据以上信息,推断该晶体的原子堆积方式是 ,Mo的摩尔质量是
,Mo的摩尔质量是 ,阿伏加德罗常数的值是NA,晶体中距离最近的Mo原子核之间的距离为
,阿伏加德罗常数的值是NA,晶体中距离最近的Mo原子核之间的距离为
(6)
 与金刚石互为同素异形体,从结构与性质之间的关系解释
与金刚石互为同素异形体,从结构与性质之间的关系解释 的熔点远低于金刚石的原因是
的熔点远低于金刚石的原因是
您最近一年使用:0次



