乙酸蒸气能形成二聚分子:2CH3COOH(g) (CH3COOH)2(g)ΔH<0。为了获得更多的二聚乙酸分子,应采用的反应条件是
(CH3COOH)2(g)ΔH<0。为了获得更多的二聚乙酸分子,应采用的反应条件是
 (CH3COOH)2(g)ΔH<0。为了获得更多的二聚乙酸分子,应采用的反应条件是
(CH3COOH)2(g)ΔH<0。为了获得更多的二聚乙酸分子,应采用的反应条件是| A.低温高压 | B.高温低压 | C.低温低压 | D.高温高压 |
更新时间:2020/01/18 09:55:11
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】工业合成甲醇的反应为
 。反应相同时间,实验测得甲醇的产率与压强,温度的关系分别如图1,图2所示。下列叙述正确的是
。反应相同时间,实验测得甲醇的产率与压强,温度的关系分别如图1,图2所示。下列叙述正确的是

 。反应相同时间,实验测得甲醇的产率与压强,温度的关系分别如图1,图2所示。下列叙述正确的是
。反应相同时间,实验测得甲醇的产率与压强,温度的关系分别如图1,图2所示。下列叙述正确的是
| A.合成甲醇时压强越大越好 | B.增大压强,正反应速率增大,逆反应速率减小 |
| C.合成甲醇的最佳温度为520K | D.520K之前升高温度单位时间内甲醇的产率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】德国化学家哈伯在合成氨方面的研究促进了人类的发展。合成氨的工业流程如图,下列说法错误的是
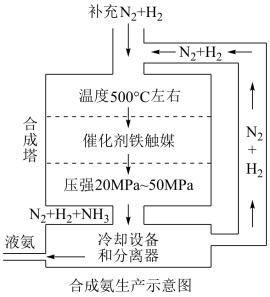

| A.增大压强既可以加快反应速率,又可以提高原料转化率 |
| B.升高温度可提高平衡转化率 |
| C.冷却过程中采用热交换有助于节约能源 |
| D.原料循环可提高其利用率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】工业制硫酸的一步重要反应是SO2在400~600℃下的催化氧化:2SO2(g)+O2(g) 2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法正确的是
2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法正确的是
 2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法正确的是
2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法正确的是| A.使用催化剂可加快反应速率,提高SO3产率 |
| B.其它条件保持不变,温度越高,速率越快,生产效益越好 |
| C.实际生产中选定400~600℃作为操作温度,其原因是在此温度下催化剂的活性最高,SO2能100%转化为SO3 |
| D.增大压强可以提高SO3产率,但高压对动力和设备要求太高,会增加生产成本 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列事实不能用化学平衡移动原理解释的是( )
A.滴加少量 溶液可以加快Zn与稀 溶液可以加快Zn与稀 反应的速率 反应的速率 |
B.高压比常压更有利于 转化为 转化为 |
C.蒸干 溶液无法得到无水 溶液无法得到无水 |
| D.新制氯水长时间放置颜色变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】如图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯(烧杯内有水)中:在(1)中加入CaO,在(2)中不加其他任何物质,在(3)中加入NH4Cl晶体,发现(1)中红棕色变深,(3)中红棕色变浅,下列叙述正确的是


A.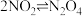 是放热反应 是放热反应 |
| B.NH4Cl溶于水时放出热量 |
| C.烧瓶(1)中平衡混合气的平均相对分子质量增大 |
| D.烧瓶(3)中气体的压强增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示,下列说法不正确 的是

| A.由图可知:乙酸的生成速率随温度升高而升高 |
| B.250—300℃时,温度升高而乙酸的生成速率降低的主要原因是催化剂的催化效率降低 |
| C.由300—400℃可知,其他条件相同时,催化剂的催化效率越低,乙酸的生成速率越大 |
| D.根据图象推测,工业上制备乙酸最适宜的温度应为250℃ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】硫酸是一种重要的化工产品,目前硫酸的主要生产方法是“接触法”,其主要反应之一为2SO2+O2 2SO3。下列有关该反应的说法不正确的是
2SO3。下列有关该反应的说法不正确的是
 2SO3。下列有关该反应的说法不正确的是
2SO3。下列有关该反应的说法不正确的是| A.SO2和O2不可能全部转化为SO3 |
| B.达到平衡后,反应就停止了,故正、逆反应速率相等且均为零 |
| C.该反应从开始到平衡的过程中,正反应速率不断减小,逆反应速率不断增大 |
| D.工业上生产SO3时,要同时考虑反应所能达到的限度和化学反应速率两个方面 |
您最近一年使用:0次

 左右比室温更有利于合成
左右比室温更有利于合成 的反应
的反应 和
和 的混合气体,受热后颜色加深
的混合气体,受热后颜色加深 生成
生成

