近年全国各地雾霾严重,为有效控制雾霾,各地积极采取措施改善大气质量。研究并有效控制空气中氮氧化物、碳氧化物等污染物是一项重要而艰巨的工作。氮氧化物的研究
 一定条件下,将2molNO与
一定条件下,将2molNO与 置于恒容密闭容器中发生反应:
置于恒容密闭容器中发生反应: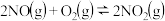 ,下列状态能说明该反应达到化学平衡的是
,下列状态能说明该反应达到化学平衡的是______  填字母编号
填字母编号 。
。
A.混合气体的密度保持不变 的转化率保持不变
的转化率保持不变
C.NO和 的物质的量之比保持不变
的物质的量之比保持不变  的消耗速率和
的消耗速率和 的消耗速率相等
的消耗速率相等
 已知反应
已知反应 ,在不同条件时
,在不同条件时 的体积分数随时间
的体积分数随时间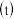 的变化如图所示。根据图象可以判断曲线
的变化如图所示。根据图象可以判断曲线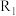 、
、 对应的下列反应条件中不同的是
对应的下列反应条件中不同的是______  填字母序号
填字母序号 。
。
A.压强 温度
温度 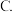 催化剂
催化剂


根据上图中的能量变化数据,计算反应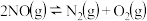 的
的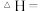
______ 。
 一定条件下,将2molNO与
一定条件下,将2molNO与 置于恒容密闭容器中发生反应:
置于恒容密闭容器中发生反应: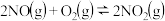 ,下列状态能说明该反应达到化学平衡的是
,下列状态能说明该反应达到化学平衡的是 填字母编号
填字母编号 。
。A.混合气体的密度保持不变
 的转化率保持不变
的转化率保持不变C.NO和
 的物质的量之比保持不变
的物质的量之比保持不变  的消耗速率和
的消耗速率和 的消耗速率相等
的消耗速率相等 已知反应
已知反应 ,在不同条件时
,在不同条件时 的体积分数随时间
的体积分数随时间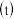 的变化如图所示。根据图象可以判断曲线
的变化如图所示。根据图象可以判断曲线 、
、 对应的下列反应条件中不同的是
对应的下列反应条件中不同的是 填字母序号
填字母序号 。
。A.压强
 温度
温度 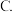 催化剂
催化剂

根据上图中的能量变化数据,计算反应
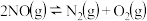 的
的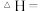
更新时间:2020-01-27 16:50:55
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】医用酒精在抗击“新型冠状病毒”战役中发挥着杀菌消毒的作用,其主要成分是乙醇。回答下列问题:
I.工业上主要采用乙烯直接水合法(CH2 =CH2+H2O→CH3CH2OH)制乙醇。
(1)在磷酸/硅藻土催化剂作用下,乙烯进行气相水合的反应机理大致如下:
i. CH2 =CH2+H3O+
 +H2O
+H2O
ii. +H2O
+H2O

iii. +H2O
+H2O CH3CH2OH+H3O+
CH3CH2OH+H3O+
随着反应进程,该过程能量变化如图1所示。
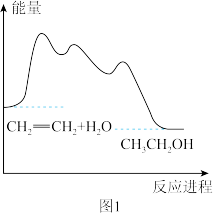
下列有关说法正确的是___________ (填字母标号,下同)。
a.该反应过程中i~ iii步均释放能量
b.第i步反应的活化能最大,决定总反应速率
c. 和
和 是反应的中间产物
是反应的中间产物
(2)已知:C2H4(g) +H2O(g) C2H5OH(g)的反应速率表达式为v正=k正c(C2H4)·c(H2O),v 逆=k逆c( C2H5OH) ,其中k正、k 逆为速率常数。若其他条件不变时,降低温度,则下列推断合理的是___________。
C2H5OH(g)的反应速率表达式为v正=k正c(C2H4)·c(H2O),v 逆=k逆c( C2H5OH) ,其中k正、k 逆为速率常数。若其他条件不变时,降低温度,则下列推断合理的是___________。
II.工业用二氧化碳加氢可合成乙醇:2CO2(g)+6H2(g) C2H5OH(g) +3H2O(g)保持压强为5MPa,向密闭容器中投入一定量CO2和H2发生上述反应, CO2的平衡转化率与温度、投料比m[
C2H5OH(g) +3H2O(g)保持压强为5MPa,向密闭容器中投入一定量CO2和H2发生上述反应, CO2的平衡转化率与温度、投料比m[ ]的关系如图2所示。
]的关系如图2所示。
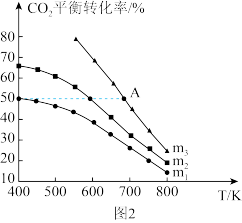
(3)投料比由大到小的顺序为_____ 。
(4)若投料比m=1,一定温度下发生反应,下列说法不能作为反应是否达平衡依据的是_____ (填标号)。
a.容器内气体密度不再变化
b.容器内气体中均相对分子质量不再变化
c. CO2的体积分数不再变化
d.容器内 不再变化
不再变化
e.断裂3NA个H-H键的同时生成l.5NA个水分子
(5)若m3=3,则A点温度下,该反应的平衡常数Kp的数值为_____ (MPa) -4(Kp是以分压表示的平衡常数) ;若其他条件不变,A点对应起始反应物置于某刚性密闭容器,则平衡时CO2的转化率___________ 50%(填“>”“=”或“<”)。
(6)用熔融碳酸盐为电解质将2C2H5OH(1) +6NO2( g) 3N2(g)+4CO2(g) +6H2O(1)反应设计为原电池,以达到利用NO2废气的目的,正极电极反应式为
3N2(g)+4CO2(g) +6H2O(1)反应设计为原电池,以达到利用NO2废气的目的,正极电极反应式为___________ ,若电路中通过2 mol电子,理论上处理NO2___________ L( 标准状况下)。
I.工业上主要采用乙烯直接水合法(CH2 =CH2+H2O→CH3CH2OH)制乙醇。
(1)在磷酸/硅藻土催化剂作用下,乙烯进行气相水合的反应机理大致如下:
i. CH2 =CH2+H3O+

 +H2O
+H2Oii.
 +H2O
+H2O

iii.
 +H2O
+H2O CH3CH2OH+H3O+
CH3CH2OH+H3O+随着反应进程,该过程能量变化如图1所示。

下列有关说法正确的是
a.该反应过程中i~ iii步均释放能量
b.第i步反应的活化能最大,决定总反应速率
c.
 和
和 是反应的中间产物
是反应的中间产物(2)已知:C2H4(g) +H2O(g)
 C2H5OH(g)的反应速率表达式为v正=k正c(C2H4)·c(H2O),v 逆=k逆c( C2H5OH) ,其中k正、k 逆为速率常数。若其他条件不变时,降低温度,则下列推断合理的是___________。
C2H5OH(g)的反应速率表达式为v正=k正c(C2H4)·c(H2O),v 逆=k逆c( C2H5OH) ,其中k正、k 逆为速率常数。若其他条件不变时,降低温度,则下列推断合理的是___________。| A.k正增大,k 逆减小 | B.k正减小,k 逆增大 |
| C.k正减小的倍数大于k 逆 | D.k正减小的倍数小于k 逆 |
II.工业用二氧化碳加氢可合成乙醇:2CO2(g)+6H2(g)
 C2H5OH(g) +3H2O(g)保持压强为5MPa,向密闭容器中投入一定量CO2和H2发生上述反应, CO2的平衡转化率与温度、投料比m[
C2H5OH(g) +3H2O(g)保持压强为5MPa,向密闭容器中投入一定量CO2和H2发生上述反应, CO2的平衡转化率与温度、投料比m[ ]的关系如图2所示。
]的关系如图2所示。
(3)投料比由大到小的顺序为
(4)若投料比m=1,一定温度下发生反应,下列说法不能作为反应是否达平衡依据的是
a.容器内气体密度不再变化
b.容器内气体中均相对分子质量不再变化
c. CO2的体积分数不再变化
d.容器内
 不再变化
不再变化e.断裂3NA个H-H键的同时生成l.5NA个水分子
(5)若m3=3,则A点温度下,该反应的平衡常数Kp的数值为
(6)用熔融碳酸盐为电解质将2C2H5OH(1) +6NO2( g)
 3N2(g)+4CO2(g) +6H2O(1)反应设计为原电池,以达到利用NO2废气的目的,正极电极反应式为
3N2(g)+4CO2(g) +6H2O(1)反应设计为原电池,以达到利用NO2废气的目的,正极电极反应式为
您最近一年使用:0次
【推荐2】工业上通常采用CO(g)和H2(g)催化合成甲醇CH3OH(g),其反应是:CO(g)+2H2(g)⇌CH3OH(g)△H=-128.8kJ·mol-1。
(1)在一定温度和压强下,若将10amolCO和20amolH2放入2L的密闭容器中,充分反应后测得CO的转化率为60%,则该反应的平衡常数为_______ (用含a的代数式表示)。若此时再向该容器中投入10amolCO、20amolH2和10amolCH3OH(g),判断平衡移动的方向是_______ (填“正向移动”、“逆向移动”或“不移动”)。
(2)在恒温恒容条件下,判断上述反应已达到平衡状态的依据是_______ (填字母序号)。
A.混合气体的密度不变
B.容器内CO、H2、CH3OH的浓度之比为1∶2∶1
C.2v逆(H2)=v正(CO)
D.CH3OH的物质的量浓度不再发生变化
E.该反应的热量不再发生变化
(3)一定条件下,在容积相同的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得上述反应达到平衡时的有关数据如下
则a+b=_______ ;α1+α3_______ 1(填“<”、“>”或“=”,下同);2p2_______ p3。
(1)在一定温度和压强下,若将10amolCO和20amolH2放入2L的密闭容器中,充分反应后测得CO的转化率为60%,则该反应的平衡常数为
(2)在恒温恒容条件下,判断上述反应已达到平衡状态的依据是
A.混合气体的密度不变
B.容器内CO、H2、CH3OH的浓度之比为1∶2∶1
C.2v逆(H2)=v正(CO)
D.CH3OH的物质的量浓度不再发生变化
E.该反应的热量不再发生变化
(3)一定条件下,在容积相同的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得上述反应达到平衡时的有关数据如下
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO、2molH2 | 1molCH3OH | 2molCH3OH | |
| 平衡时 数据 | 反应能量变化的绝对值(kJ) | a | b | c |
| 反应物转化率 | α1 | α2 | α3 | |
| 体系压强(Pa) | P1 | p2 | p3 | |
则a+b=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某同学进行Na2S2O3与H2SO4反应的有关实验,实验过程的数据记录如下(见表格),请结合表中信息,回答有关问题:
(1)写出该反应的离子方程式为:_______ 。
(2)教材中利用了出现乳白色浑浊的快慢来比较反应速率的快慢,请你分析为何不通过观察气泡产生快慢来进行比较:_______ 。
(3)根据你所掌握的知识判断,上表中空白处的数据是_______ 。
(4)在比较某一因素对实验产生的影响时,必须控制变量,其中能说明温度对该反应速率影响的组合是_______ (填实验序号);B和C的组合比较,所研究的问题是_______ 。
(5)一定条件下,向体积为2L的恒容密闭容器中充入1molCO2(g)和3molH2(g),发生反应CO2(g)+3H2(g)⇌ CH3OH(g)+H2O(g),20s时,测得混合气体的压强是反应前的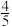 倍,则用二氧化碳表示该反应的速率为
倍,则用二氧化碳表示该反应的速率为_______ 。下列可作为上述可逆反应达到平衡状态的依据是_______ (填序号)。
A.v正(CH3OH)=v逆(H2)
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、H2O、CO2、H2的浓度都不再发生变化
| 实验 序号 | 反应温 度/℃ | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
| A | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| B | 20 | 0.1 | 10 | 0.1 | 5 | |
| C | 20 | 10 | 0.1 | 5 | 0.1 | 5 |
| D | 40 | 10 | 0.1 | 10 | 0.1 | 0 |
(2)教材中利用了出现乳白色浑浊的快慢来比较反应速率的快慢,请你分析为何不通过观察气泡产生快慢来进行比较:
(3)根据你所掌握的知识判断,上表中空白处的数据是
(4)在比较某一因素对实验产生的影响时,必须控制变量,其中能说明温度对该反应速率影响的组合是
(5)一定条件下,向体积为2L的恒容密闭容器中充入1molCO2(g)和3molH2(g),发生反应CO2(g)+3H2(g)⇌ CH3OH(g)+H2O(g),20s时,测得混合气体的压强是反应前的
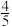 倍,则用二氧化碳表示该反应的速率为
倍,则用二氧化碳表示该反应的速率为A.v正(CH3OH)=v逆(H2)
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、H2O、CO2、H2的浓度都不再发生变化
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】乙烯的分子式为 ,是一种重要的化工原料和清洁能源,研究乙烯的制备和综合利用具有重要意义。请回答下列问题:
,是一种重要的化工原料和清洁能源,研究乙烯的制备和综合利用具有重要意义。请回答下列问题:
(1)乙烯的制备:工业上常利用反应 制备乙烯。
制备乙烯。
已知:Ⅰ. ;
;
Ⅱ. ;
;
Ⅲ. 。
。
则
___________ kJ/mol。
(2)乙烯可用于制备乙醇: 。向某恒容密闭容器中充入
。向某恒容密闭容器中充入 和
和 ,测得
,测得 的平衡转化率与温度的关系如图所示:
的平衡转化率与温度的关系如图所示:

①该反应为___________ (填“吸”或“放”)热反应,理由为___________ 。
②A点时容器中气体的总物质的量为___________ 。已知分压=总压×气体物质的量分数,用气体分压替代浓度计算的平衡常数叫压强平衡常数(Kp),测得300℃时,反应达到平衡时该容器内的压强为bMPa,则A点对应温度下的Kp=___________  (用含b的分数表示)
(用含b的分数表示)
③若保持其他条件不变,将容器改为恒压密闭容器,则300℃时, 的平衡转化率
的平衡转化率___________ 10%(填“>”“<”或“=”)。
 ,是一种重要的化工原料和清洁能源,研究乙烯的制备和综合利用具有重要意义。请回答下列问题:
,是一种重要的化工原料和清洁能源,研究乙烯的制备和综合利用具有重要意义。请回答下列问题:(1)乙烯的制备:工业上常利用反应
 制备乙烯。
制备乙烯。已知:Ⅰ.
 ;
;Ⅱ.
 ;
;Ⅲ.
 。
。则

(2)乙烯可用于制备乙醇:
 。向某恒容密闭容器中充入
。向某恒容密闭容器中充入 和
和 ,测得
,测得 的平衡转化率与温度的关系如图所示:
的平衡转化率与温度的关系如图所示:
①该反应为
②A点时容器中气体的总物质的量为
 (用含b的分数表示)
(用含b的分数表示)③若保持其他条件不变,将容器改为恒压密闭容器,则300℃时,
 的平衡转化率
的平衡转化率
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】燃煤及硫酸工业尾气中的SO2是重要的大气污染物,可以用以下方法处理尾气中的SO2。
方法一:通过活性炭作用回收
(1)配平反应方程式。____ C(s)+____ SO2(g)
_____ S2(g)+_____ CO2(g)
(2)反应的化学平衡常数表达式为______________________ ;若在某密闭容器中进行上述反应,为了加快吸收SO2,可采取的措施有_____________________________ 。
方法二:利用亚硫酸钠溶液进行吸收
(3)把尾气(含二氧化硫)不断通入到饱和亚硫酸钠溶液中,生成亚硫酸氢钠,pH值的变化如图所示,请根据图示,解释pH值变化的原因:_________________________________________ 。
方法三:利用氯气和干燥的二氧化硫在活性炭催化剂存在下反应制取氯化硫酰:SO2(g)+Cl2(g) SO2Cl2(l)+97.3kJ,已知氯化硫酰(SO2Cl2)主要用作氯化剂。它是一种无色液体,熔点-54.1℃,沸点69.1℃。
SO2Cl2(l)+97.3kJ,已知氯化硫酰(SO2Cl2)主要用作氯化剂。它是一种无色液体,熔点-54.1℃,沸点69.1℃。
(4)若反应的容器体积为2L,2分钟内液体质量增加了2.7克,用氯气表示这两分钟内的化学反应速率____ 。
(5)(以下写出一种措施即可)。若在此条件下,为了提高SO2的转化率,可采取的措施有______________ ,当___________________________ 时说明上述反应已达到平衡状态。
方法一:通过活性炭作用回收
(1)配平反应方程式。

(2)反应的化学平衡常数表达式为
方法二:利用亚硫酸钠溶液进行吸收
(3)把尾气(含二氧化硫)不断通入到饱和亚硫酸钠溶液中,生成亚硫酸氢钠,pH值的变化如图所示,请根据图示,解释pH值变化的原因:

方法三:利用氯气和干燥的二氧化硫在活性炭催化剂存在下反应制取氯化硫酰:SO2(g)+Cl2(g)
 SO2Cl2(l)+97.3kJ,已知氯化硫酰(SO2Cl2)主要用作氯化剂。它是一种无色液体,熔点-54.1℃,沸点69.1℃。
SO2Cl2(l)+97.3kJ,已知氯化硫酰(SO2Cl2)主要用作氯化剂。它是一种无色液体,熔点-54.1℃,沸点69.1℃。(4)若反应的容器体积为2L,2分钟内液体质量增加了2.7克,用氯气表示这两分钟内的化学反应速率
(5)(以下写出一种措施即可)。若在此条件下,为了提高SO2的转化率,可采取的措施有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】(1)已知: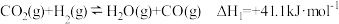

写出 催化氢化合成甲醇和水的热化学方程式:
催化氢化合成甲醇和水的热化学方程式:_______ 。
(2)工业上在恒容密闭容器中用下列反应合成甲醇:

①该反应的平衡常数表达式为_______ ;
②如表所列数据是反应在不同温度下的化学平衡常数(K)
a.由表中数据判断该反应的
_______ 0(填“>”、“=”或“<”);
b.某温度下,将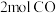 和
和 充入
充入 的密闭容器中,充分反应
的密闭容器中,充分反应 后达到平衡时测得
后达到平衡时测得 ,则CO的转化率为
,则CO的转化率为_______ ,此时的温度为_______ ;
③要提高CO的转化率,可以采取的措施是_______ ;
a.升温 b.加入催化剂 c.增加CO的浓度 d.恒容充入 e.分离出甲醇
e.分离出甲醇
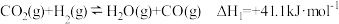

写出
 催化氢化合成甲醇和水的热化学方程式:
催化氢化合成甲醇和水的热化学方程式:(2)工业上在恒容密闭容器中用下列反应合成甲醇:

①该反应的平衡常数表达式为
②如表所列数据是反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
a.由表中数据判断该反应的

b.某温度下,将
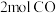 和
和 充入
充入 的密闭容器中,充分反应
的密闭容器中,充分反应 后达到平衡时测得
后达到平衡时测得 ,则CO的转化率为
,则CO的转化率为③要提高CO的转化率,可以采取的措施是
a.升温 b.加入催化剂 c.增加CO的浓度 d.恒容充入
 e.分离出甲醇
e.分离出甲醇
您最近一年使用:0次



