氟代硼酸钾(KBe2BO3F2)是激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。请回答下列问题:
(1)第一电离能介于B和N之间的第二周期的元素共有________ 种。
(2)基态K+离子电子占据最高能级的电子云轮廓图为_________ 形。
(3)BeCl2中的化学键具有明显的共价性,蒸汽状态下BeCl2以双聚分子存在,其结构式为________ ,其中Be原子的电子排布图为_________ 。
(4)四氟硼酸钠(NaBF4)是纺织工业的催化剂。其阴离子的中心原子的杂化轨道类型为_________ 。四氟硼酸钠中存在_______ (填序号):
a. 氢键 b. 范德华力 c. 离子键 d. 配位键 e. σ键 f. π键
(1)第一电离能介于B和N之间的第二周期的元素共有
(2)基态K+离子电子占据最高能级的电子云轮廓图为
(3)BeCl2中的化学键具有明显的共价性,蒸汽状态下BeCl2以双聚分子存在,其结构式为
(4)四氟硼酸钠(NaBF4)是纺织工业的催化剂。其阴离子的中心原子的杂化轨道类型为
a. 氢键 b. 范德华力 c. 离子键 d. 配位键 e. σ键 f. π键
更新时间:2020-01-24 16:45:11
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】钢化玻璃因其优良的性能广泛应用于日常生活,但由于制作玻璃时里面含有极少量硫化镍,使得钢化玻璃在极限条件下的使用受到限制。
(1)基态硫原子价层电子的轨道表达式 电子排布图
电子排布图 为
为__ ,基态镍原子中核外电子占据最高能层的符号为__ 。
(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为__ 晶体,Ni(CO)4空间构型与甲烷相同,中心原子的杂化轨道类型为__ ,写出与配体互为等电子体的阴离子__  任写一种
任写一种 。
。
(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱__ >__  填化学式
填化学式 ,理由是
,理由是__ 。
(4)H2S的键角__ 填“大于”“小于”“等于”)H2O的键角,请从电负性的角度说明理由__ 。
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的__ 空隙中,已知Ni2+半径为69nm,O2-半径为140nm,阿伏加 德罗常数为NA,NiO晶体的密度为__ g/cm3(只列出计算式 。
。

(1)基态硫原子价层电子的轨道表达式
 电子排布图
电子排布图 为
为(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为
 任写一种
任写一种 。
。(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱
 填化学式
填化学式 ,理由是
,理由是(4)H2S的键角
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的
 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】分析下列化学式中画有横线的元素,选出符合要求的物质,填空。
A.NH3 B.H2O C.HCl D.CH4 E.C2H6 F.N2
(1)所有的价电子都参与形成共价键的是_________________ ;
(2)只有一个价电子参与形成共价键的是_______________ ;
(3)最外层有未参与成键的电子对的是______________ ;
(4)既有σ键又有π键的是_____________ 。
A.NH3 B.H2O C.HCl D.CH4 E.C2H6 F.N2
(1)所有的价电子都参与形成共价键的是
(2)只有一个价电子参与形成共价键的是
(3)最外层有未参与成键的电子对的是
(4)既有σ键又有π键的是
您最近一年使用:0次
【推荐1】中国古代四大发明之一﹣﹣黑火药,它的爆炸反应为:2KNO3+3C+S A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
①除S外,上列元素的电负性从大到小依次为___________ 。除K、S外第一电离能从大到小的顺序为___________ 。N2 与CO2熔沸点高低顺序为___________ 。
②在生成物中,A的晶体类型为___________ ,含极性共价键的分子的中心原子轨道杂化类型为___________ 。
③CN﹣与N2互为___________ ,推算HCN分子中σ键与π键数目之比___________ 。
 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)①除S外,上列元素的电负性从大到小依次为
②在生成物中,A的晶体类型为
③CN﹣与N2互为
您最近一年使用:0次
【推荐2】IIIA族元素及其化合物在材料化学中具有广泛的应用。回答下列问题:
(1)基态硼原子核外价电子的轨道表示式为___________ 。
(2)氨硼烷(NH3BH3)是目前最具潜力的储氢材料之一、氨硼烷分子中与N相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键。NH3BH3所含元素电负性由大到小的顺序为___________ ;还原性:NH3BH3___________ NH3(填“>”或“<”)。
(3)N、O、F三元素对应氢化物的稳定性有强到弱的顺序为___________ (用化学式表示)。
(4)基态铝原子核外有___________ 个空间运动状态,第一电离能介于Al、P之间的第3周期元素有___________ 种。
(1)基态硼原子核外价电子的轨道表示式为
(2)氨硼烷(NH3BH3)是目前最具潜力的储氢材料之一、氨硼烷分子中与N相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键。NH3BH3所含元素电负性由大到小的顺序为
(3)N、O、F三元素对应氢化物的稳定性有强到弱的顺序为
(4)基态铝原子核外有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】回答下列问题:
(1)氟原子激发态的电子排布式有______ ,其中能量较高的是______ 。(填标号)
a.1s22s22p43s1 b.1s22s22p43d2 c.1s22s12p5 d.1s22s22p33p2
(2)某元素原子的位于周期表的第四周期,元素原子的最外层只有一个电子,其次外层内的所以轨道电子均成对。该元素位于周期表的______ 区,写出该基态原子电子排布式为______ 。
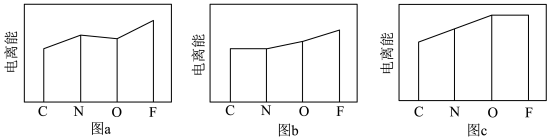
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是______ (填标号),判断的根据是______ ;第三电离能的变化图是______ (填标号)。
(4)短周期元素X、Y、Z、W的原子序数依次增大。根据表中信息完成下列空白。
①元素的电负性:Z______ W(填“大于”“小于”或“等于”)。
②简单离子半径:W______ Y(填“大于”“小于”或“等于”)。
③氢化物的稳定性:X______ Z(填“大于”“小于”或“等于”)。
(1)氟原子激发态的电子排布式有
a.1s22s22p43s1 b.1s22s22p43d2 c.1s22s12p5 d.1s22s22p33p2
(2)某元素原子的位于周期表的第四周期,元素原子的最外层只有一个电子,其次外层内的所以轨道电子均成对。该元素位于周期表的
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(4)短周期元素X、Y、Z、W的原子序数依次增大。根据表中信息完成下列空白。
| 元素 | X | Y | Z | W |
| 最高价氧化物的水化物 | H3ZO4 | |||
| 0.1 mol∙L−1溶液对应的pH(25℃) | 1.00 | 13.00 | 1.57 | 0.70 |
②简单离子半径:W
③氢化物的稳定性:X
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】磷是生物体中不可缺少的元素之一,它能形成多种化合物。
(1)基态磷原子中,电子占据的最高能层符号为________ ;该能层能量最高的电子云在空间有________ 个伸展方向,原子轨道呈________ 形。
(2)磷元素与同周期相邻两元素相比,第一电离能由大到小的顺序为________ 。
(3)单质磷与Cl2反应,可以生成PCl3和PCl5,其中各原子均满足8电子稳定结构的化合物中,P原子的杂化轨道类型为________ ,其分子的空间构型为________ 。
(4)H3PO4为三元中强酸,与Fe3+形成H3[Fe(PO4)2],此性质常用于掩蔽溶液中的Fe3+。基态Fe3+的核外电子排布式为____________________ ;PO43-作为________ 为Fe提供________ 。
(1)基态磷原子中,电子占据的最高能层符号为
(2)磷元素与同周期相邻两元素相比,第一电离能由大到小的顺序为
(3)单质磷与Cl2反应,可以生成PCl3和PCl5,其中各原子均满足8电子稳定结构的化合物中,P原子的杂化轨道类型为
(4)H3PO4为三元中强酸,与Fe3+形成H3[Fe(PO4)2],此性质常用于掩蔽溶液中的Fe3+。基态Fe3+的核外电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】钴的一种配位聚合物的化学式为{[Co(bte)2(H2O)2](NO3)2}n。
(1)Co2+基态核外电子排布式为___________ 。
(2)NO 的空间结构为
的空间结构为___________ 。
(3)bte的分子式为C6H8N6,其结构简式如图所示。

①[Co(bte)2(H2O)2]2+中,与Co2+形成配位键的原子是___________ 和___________ (填元素符号)。
②C、H、N的电负性从大到小顺序为___________ 。
③bte分子中碳原子轨道杂化类型为___________ 和___________ 。
④1mol bte分子中含 键的数目为
键的数目为___________ mol。
(1)Co2+基态核外电子排布式为
(2)NO
 的空间结构为
的空间结构为(3)bte的分子式为C6H8N6,其结构简式如图所示。

①[Co(bte)2(H2O)2]2+中,与Co2+形成配位键的原子是
②C、H、N的电负性从大到小顺序为
③bte分子中碳原子轨道杂化类型为
④1mol bte分子中含
 键的数目为
键的数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】2016年9月南开大学学者首次测试了一种新型锌离子电池,该电池以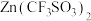 为电解质,用有阳离子型缺陷的
为电解质,用有阳离子型缺陷的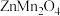 为电极,成功的获得了稳定的大功率电流。
为电极,成功的获得了稳定的大功率电流。
(1)写出基态 原子核外M能层的电子排布式
原子核外M能层的电子排布式_____ 。
(2)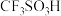 是一种有机强酸,结构式如图所示,通常用
是一种有机强酸,结构式如图所示,通常用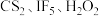 等为主要原料制取。
等为主要原料制取。
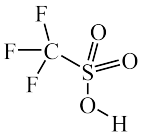
①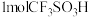 分子中含有的
分子中含有的 键的数目为
键的数目为_____ 。
② 分子中O原子的杂化方式与
分子中O原子的杂化方式与 中硫原子杂化方式
中硫原子杂化方式_____ (填“相同”或“不同”)
③ 难溶于水的原因是
难溶于水的原因是_____ 。与 互为等电子体的一种分子为
互为等电子体的一种分子为_____ 。
④ 遇水完全水解生成两种酸,写出相关化学方程式:
遇水完全水解生成两种酸,写出相关化学方程式:_____ 。
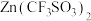 为电解质,用有阳离子型缺陷的
为电解质,用有阳离子型缺陷的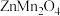 为电极,成功的获得了稳定的大功率电流。
为电极,成功的获得了稳定的大功率电流。(1)写出基态
 原子核外M能层的电子排布式
原子核外M能层的电子排布式(2)
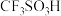 是一种有机强酸,结构式如图所示,通常用
是一种有机强酸,结构式如图所示,通常用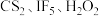 等为主要原料制取。
等为主要原料制取。
①
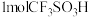 分子中含有的
分子中含有的 键的数目为
键的数目为②
 分子中O原子的杂化方式与
分子中O原子的杂化方式与 中硫原子杂化方式
中硫原子杂化方式③
 难溶于水的原因是
难溶于水的原因是 互为等电子体的一种分子为
互为等电子体的一种分子为④
 遇水完全水解生成两种酸,写出相关化学方程式:
遇水完全水解生成两种酸,写出相关化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】钛和钛的合金已广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题:
①Ti 元素在元素周期表中的位置是第_____ 周期,第_____ 族;基态原子的电子排布式为_____ ;按电子排布Ti 元素在元素周期表分区中_____ 区
②现有 Ti3+的配合物化学式为[TiCl(H2O)5 ]Cl2H2O。配离子[TiCl(H2O)5]2+ 中含有的化学键类型是_____ ,_____ 。该配合物的配体是_____ 、_____
①Ti 元素在元素周期表中的位置是第
②现有 Ti3+的配合物化学式为[TiCl(H2O)5 ]Cl2H2O。配离子[TiCl(H2O)5]2+ 中含有的化学键类型是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】配合物的形成对物质性质有什么影响_____ ?
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】氢能的存储是其应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为________ ,该能层具有的原子轨道数为________ 。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2 2NH3实现储氢和输氢。下列说法正确的是
2NH3实现储氢和输氢。下列说法正确的是( )
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是___________ 。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2
 2NH3实现储氢和输氢。下列说法正确的是
2NH3实现储氢和输氢。下列说法正确的是| A.NH3分子中氮原子的轨道杂化方式为sp2杂化 |
| B.NH4+与PH4+、CH4、BH4-、ClO4-互为等电子体 |
| C.相同压强下,NH3沸点比PH3的沸点高 |
| D.[Cu(NH3)4]2+中,N原子是配位原子 |
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是
您最近一年使用:0次

 ,杂化方式为
,杂化方式为 、CS2、CO
、CS2、CO 键角由大到小的顺序是
键角由大到小的顺序是
 (填“>”或“<”),原因是
(填“>”或“<”),原因是 

