某温度下,向 恒容密闭容器中充入
恒容密闭容器中充入 和
和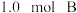 ,发生反应
,发生反应 ,经过一段时间后反应达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
,经过一段时间后反应达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是

 恒容密闭容器中充入
恒容密闭容器中充入 和
和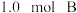 ,发生反应
,发生反应 ,经过一段时间后反应达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
,经过一段时间后反应达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是

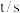 | 0 | 5 | 15 | 25 | 35 |
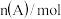 |  |  | 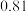 | 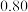 | 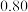 |
A.前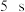 的平均反应速率 的平均反应速率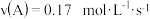 |
B.保持其他条件不变,升高温度,平衡时 ,则反应的 ,则反应的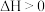 |
C.相同温度下,起始时向容器中充入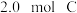 ,达到平衡时C的转化率大于 ,达到平衡时C的转化率大于 |
D.相同温度下,起始时向容器中充入 、 、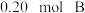 和 和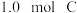 ,反应达到平衡前 ,反应达到平衡前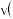 正 正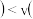 逆 逆 |
更新时间:2020-02-07 14:15:30
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】某温度下,在2L恒容密闭容器中投入4mol 发生如下反应
发生如下反应
 有关数据如下:
有关数据如下:
下列说法错误的是
 发生如下反应
发生如下反应
 有关数据如下:
有关数据如下:| 时间段/min |  的平均生成速率/ 的平均生成速率/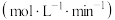 |
| 0-1 | 0.4 |
| 0-2 | 0.3 |
| 0-3 | 0.2 |
A.30秒时, 的浓度大于 的浓度大于 |
B.0-1min内,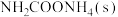 的反应速率为 的反应速率为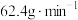 |
C.2min30秒时 物质的量小于2.8mol 物质的量小于2.8mol |
D.当 的体积百分数不变时,不能说明此反应达到了平衡状态 的体积百分数不变时,不能说明此反应达到了平衡状态 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】利用反应: 可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入
可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入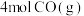 和
和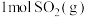 发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
 可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入
可实现从燃煤烟气中回收硫。在恒温恒容条件下,向两个体积均为VL的密闭容器中各充入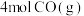 和
和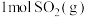 发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
发生该反应,在不同温度下两个反应体系的总压强随时间的变化如图所示。
A.容器Ⅰ中CO的体积分数: |
B.容器Ⅱ中 的平衡转化率是80% 的平衡转化率是80% |
C.平衡常数: |
D. 内用 内用 表示容器I中的平均反应速率为 表示容器I中的平均反应速率为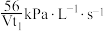 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】在常温、常压和光照条件下,N2在催化剂表面与H2O发生反应:2N2(g)+6H2O(l) =4NH3(g)+3O2(g)。在2 L的密闭容器中,起始反应物用量相同,催化剂的使用情况也相同,控制不同温度分别进行4组实验,3 h后测定NH3的生成量,所得数据如下表:
下列说法不正确 的是
| 实验级别 | 实验1 | 实验2 | 实验3 | 实验4 |
| 温度/K | 303 | 313 | 323 | 353 |
| NH3生成量/10−6mol | 4.8 | 5.9 | 6.0 | 2.0 |
下列说法
| A.温度为303 K时,在3 h内用氮气表示的平均反应速率为4×10−7mol·L−1·h−1 |
| B.实验1和实验3中,3 h内N2的转化率之比为4:5 |
| C.分析四组实验数据可得出,温度升高可加快反应速率,也可能减慢反应速率 |
| D.353 K时,可能是催化剂催化活性下降或部分水脱离催化剂表面,致使化学反应速率减慢 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在恒温时,一固定容积的容器内通入1mol PCl5(g)发生如下反应:PCl5(g)⇌PCl3(g)+Cl2(g), 达到平衡时,再向容器内通入一定量的PCl5(g),重新达到平衡后,与第一次平衡时相比,PCl5的体积分数( )
| A.增大 | B.减小 | C.不变 | D.无法判断 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】臭氧是理想的烟气脱硝剂,其脱硝反应为2NO2(g)+O3(g) N2O5(g)+O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
N2O5(g)+O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
下列有关说法正确的是
 N2O5(g)+O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
N2O5(g)+O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:| t/s | 0 | 3 | 6 | 12 | 24 |
| n(O2)/mol | 0 | 0.36 | 0.60 | 0.80 | 0.80 |
下列有关说法正确的是
| A.反应在0~3 s内的平均速率v(NO2)=0.24 mol·L-1·s-1 |
| B.24 s后,若保持其他条件不变,降低温度,达到新平衡时测得c(O2)=0.44 mol·L-1,则反应的ΔH>0 |
| C.在T温度下,起始时向容器中充入2.0 mol N2O5和2.0 mol O2,达到平衡时,N2O5的转化率大于20% |
| D.在T温度下,起始时向容器中充入1.0 mol NO2、0.5 mol O3和0.50 mol N2O5、0.50 mol O2,反应达到平衡时,压强为起始时的0.88倍 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g) xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
 xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )| A.平衡时甲中A的体积分数为0.4 |
| B.平衡时甲、乙两容器中A、B的物质的量之比不相等 |
| C.若平衡时两容器中的压强不相等,则两容器中压强之比为8:5 |
| D.若平衡时甲、乙两容器中A的物质的量相等,则x=4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】某温度下,在容积为2L的恒容密闭容器中充入1
 和2
和2
 ,加入合适的催化剂(体积可以忽略不计)后发生反应
,加入合适的催化剂(体积可以忽略不计)后发生反应
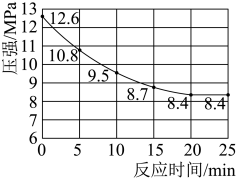
 ,反应过程中用压力计测得容器内压强的变化如图所示。下列说法正确的是
,反应过程中用压力计测得容器内压强的变化如图所示。下列说法正确的是

 和2
和2
 ,加入合适的催化剂(体积可以忽略不计)后发生反应
,加入合适的催化剂(体积可以忽略不计)后发生反应
 ,反应过程中用压力计测得容器内压强的变化如图所示。下列说法正确的是
,反应过程中用压力计测得容器内压强的变化如图所示。下列说法正确的是
| A.升高温度既能增大该反应的速率又能提高产率 |
B.向体系中充入一定量的氮气, 的转化率增大 的转化率增大 |
C.25min时向容器内再充入 和 和 各0.5 各0.5 ,平衡正向移动 ,平衡正向移动 |
D.该温度下平衡常数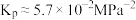 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】某同学设计实验方案,利用沉淀滴定法测定“Ag++Fe2+ Fe3++Ag↓”的平衡常数K。一定温度下,先将0.0100mol·L-1Ag2SO4溶液与0.0400mol·L-1FeSO4溶液(pH=1)等体积混合,待反应达到平衡时,过滤,取vmL滤液用c1mol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液v1mL。
Fe3++Ag↓”的平衡常数K。一定温度下,先将0.0100mol·L-1Ag2SO4溶液与0.0400mol·L-1FeSO4溶液(pH=1)等体积混合,待反应达到平衡时,过滤,取vmL滤液用c1mol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液v1mL。
已知:Ag++SCN- AgSCN↓(白色) K1
AgSCN↓(白色) K1
Fe3++SCN- FeSCN2+(红色) K2
FeSCN2+(红色) K2
下列说法正确的是
 Fe3++Ag↓”的平衡常数K。一定温度下,先将0.0100mol·L-1Ag2SO4溶液与0.0400mol·L-1FeSO4溶液(pH=1)等体积混合,待反应达到平衡时,过滤,取vmL滤液用c1mol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液v1mL。
Fe3++Ag↓”的平衡常数K。一定温度下,先将0.0100mol·L-1Ag2SO4溶液与0.0400mol·L-1FeSO4溶液(pH=1)等体积混合,待反应达到平衡时,过滤,取vmL滤液用c1mol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液v1mL。已知:Ag++SCN-
 AgSCN↓(白色) K1
AgSCN↓(白色) K1Fe3++SCN-
 FeSCN2+(红色) K2
FeSCN2+(红色) K2下列说法正确的是
| A.Ag2SO4溶液和FeSO4溶液(pH=1)可替换为AgNO3溶液和Fe(NO3)2溶液(pH=1) |
| B.K1>>K2,Fe3+是滴定终点的指示剂 |
| C.若不过滤,直接用浊液做滴定实验测定c(Ag+),则所测K值偏大 |
| D.若改为测定滤液中c(Fe3+),选择合适的滴定方法直接滴定滤液,也能达到目的 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】向某密闭容器中加入0.6 mol A、0.2 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如甲图所示[其中t0-t1阶段c(B)未画出]。t2时刻后改变条件反应体系中反应速率随时间变化的情况如乙图所示,且四个阶段都各改变一种条件并且改变的条件均不相同。下列说法正确的是( )
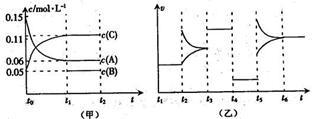

A.反应的方程式为3A(g)+B(g)  2C(g) 2C(g) |
| B.t3~t4,t4~t5,t5~t6各阶段可能改变的条件依次为:加催化剂,降低反应温度,增大压强 |
| C.B的起始物质的量为0.08 mol |
| D.若t1=10 s,A在t0~t1时间段的反应速率为0.00225 mol·L-1·s-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g) +Y(g) 2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
下列说法不正确的是
 2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A.反应前2min的平均速率v(Z)=4.0×10-3mol/(L·min) |
| B.其他条件不变,降低温度,反应达到新平衡前v(逆)<v(正) |
| C.该温度下此反应的平衡常数K=1.44 |
| D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大 |
您最近一年使用:0次

 ,充分反应达平衡后,测得微粒浓度如下:
,充分反应达平衡后,测得微粒浓度如下:



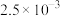

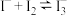 的
的
 ,振荡静置,水层
,振荡静置,水层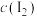 降低
降低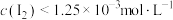
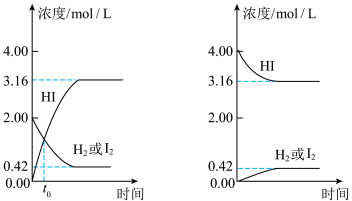
 时,反应达到平衡状态
时,反应达到平衡状态 H2(g)+I2(g)
H2(g)+I2(g)

