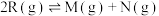将等物质的量A、B混合于2L的密闭容器中发生反应:3A(g)+B(g)⇌xC(g)+D(g)。经4min后,测得D的浓度为0.4 mol·L-1,C的平均反应速率为0.lmol·L-1·min-1,c(A):c(B)=3:5。下列说法不正确的是
| A.x的值是1 | B.4min末,A的转化率为60% |
| C.起始时A的浓度为2.4mol·L-1 | D.4min内v(B)=0.1 mol·L-1·min-1 |
更新时间:2020-02-08 12:12:51
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】反应4NH3(g) + 5O2(g)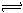 4NO(g) + 6H2O(g) 在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率为
4NO(g) + 6H2O(g) 在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率为
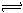 4NO(g) + 6H2O(g) 在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率为
4NO(g) + 6H2O(g) 在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率为| A.v(O2) =0.01 mol/(L·s) | B.v(NO) =0.002 mol/(L·s) |
| C.v (H2O) =0.006 mol/(L·s) | D.v(NH3) = 0.008 mol/(L·s) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】恒温恒容,4A(s)+3B(g) 2C(g)+D(g)经2min,B的浓度减少0.6mol•L-1,下列说法正确的是
2C(g)+D(g)经2min,B的浓度减少0.6mol•L-1,下列说法正确的是
 2C(g)+D(g)经2min,B的浓度减少0.6mol•L-1,下列说法正确的是
2C(g)+D(g)经2min,B的浓度减少0.6mol•L-1,下列说法正确的是| A.用A表示的反应速率是0.4mol•L-1•min-1 |
| B.气体的密度不再变化,则证明反应已经达到平衡状态 |
| C.2min末的反应速率v(B)=0.3mol•L-1•min-1 |
| D.分别用B、C表示反应的速率,其关系是:3v(B)=2v(C) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】一定条件下,下列表示4NH3(g)+5O2(g) 4NO(g)+6H2O(g)的反应速率中,最快的是
4NO(g)+6H2O(g)的反应速率中,最快的是
 4NO(g)+6H2O(g)的反应速率中,最快的是
4NO(g)+6H2O(g)的反应速率中,最快的是| A.v(NH3)=0.8mol·L-1·s-1 | B.v(O2)=0.9mol·L-1·s-1 |
| C.v(NO)=0.6mol·L-1·s-1 | D.v(H2O)=1.0mol·L-1·s-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】反应A(s)+3B(g)⇌2C(g)+2D(g),在不同情况下测得反应速率,反应最快的是
| A.v(D)=0.4mol/(L·s) | B.v(C)=0.6mol/(L·min) |
| C.v(B)=0.5mol/(L·s) | D.v(A)=0.25mol/(L·s) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】氢还原辉钼矿并用碳酸钠作固硫剂的原理为:MoS2(s) + 4H2(g) + 2Na2CO3(s)⇌MoS2(s) + 2CO(g) + 4H2O(g) + 2Na2S(s) ΔH。平衡时的有关变化曲线如图。下列说法正确的是
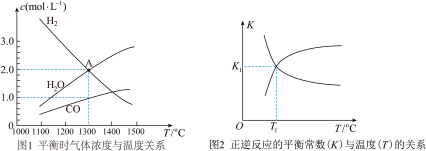

| A.该反应ΔH < 0 |
B.若图1中A点对应温度下体系总压强为20 MPa,则p(CO)= MPa MPa |
| C.图2中T1对应图1中的温度为1300 ℃ |
| D.粉碎矿物和增大压强都有利于提高H2的平衡转化率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】一定温度下,反应2A(g) B(g)+D(g),密闭容器中达到平衡时,测得c(A)=0.11mol•L-1,c(B)=0.11mol•L-1,c(D)=1.54mol•L-1。相同温度下,按下列4组初始浓度进行实验,反应逆向进行的是
B(g)+D(g),密闭容器中达到平衡时,测得c(A)=0.11mol•L-1,c(B)=0.11mol•L-1,c(D)=1.54mol•L-1。相同温度下,按下列4组初始浓度进行实验,反应逆向进行的是
 B(g)+D(g),密闭容器中达到平衡时,测得c(A)=0.11mol•L-1,c(B)=0.11mol•L-1,c(D)=1.54mol•L-1。相同温度下,按下列4组初始浓度进行实验,反应逆向进行的是
B(g)+D(g),密闭容器中达到平衡时,测得c(A)=0.11mol•L-1,c(B)=0.11mol•L-1,c(D)=1.54mol•L-1。相同温度下,按下列4组初始浓度进行实验,反应逆向进行的是| A | B | C | D | |
| c(A)/mol•L-1 | 1.00 | 0.22 | 0.40 | 0.11 |
| c(B)/mol•L-1 | 1.00 | 0.22 | 0.40 | 0.22 |
| c(D)/mol•L-1 | 1.00 | 3.08 | 4.00 | 1.54 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
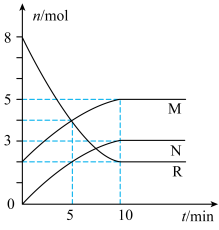
【推荐1】在某密闭容器中发生可逆反应: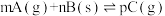 。图(I)中α(A)表示A气体的转化率,图(Ⅱ)中Y为未知物理量。下列说法正确的是
。图(I)中α(A)表示A气体的转化率,图(Ⅱ)中Y为未知物理量。下列说法正确的是

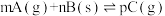 。图(I)中α(A)表示A气体的转化率,图(Ⅱ)中Y为未知物理量。下列说法正确的是
。图(I)中α(A)表示A气体的转化率,图(Ⅱ)中Y为未知物理量。下列说法正确的是
| A.其他条件不变时,反应达平衡后加入A再次达到平衡时B的转化率不变 |
| B.其他条件不变时,反应达平衡后加入A再次达平衡,A的体积分数增大 |
C.图Ⅱ中a、b、c三点的平衡常数: |
| D.图Ⅱ中Y可以表示A的平衡转化率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】往某恒容密闭容器中充入2 mol X(g)和a mol Y(g)发生反应:nX(g)+3Y(g)⇌R(g)+2Q(g)。达平衡时测得生成0.125 mol R,此时X的转化率为25%,则n值为
| A.4 | B.3 | C.2 | D.1 |
您最近一年使用:0次

 4NO+6H2O在5 L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3 mol,则此反应的平均速率
4NO+6H2O在5 L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3 mol,则此反应的平均速率 (表示反应物的消耗速率或生成物的生成速率)为(
(表示反应物的消耗速率或生成物的生成速率)为( = 0.01 mol / (L·s)
= 0.01 mol / (L·s) = 0.008 mol / (L·s)
= 0.008 mol / (L·s) = 0.004 mol / (L·s)
= 0.004 mol / (L·s) N2(g)+O2(g) K1=1×1030
N2(g)+O2(g) K1=1×1030