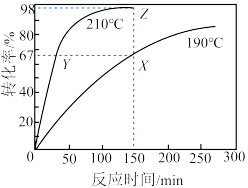
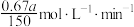汽车尾气污染已成为突出的环境问题之一,反应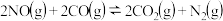
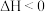 可用于净化汽车尾气,已知该反应的反应速率极慢,
可用于净化汽车尾气,已知该反应的反应速率极慢, 时平衡常数为
时平衡常数为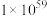 。下列说法正确的是
。下列说法正确的是
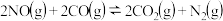
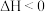 可用于净化汽车尾气,已知该反应的反应速率极慢,
可用于净化汽车尾气,已知该反应的反应速率极慢, 时平衡常数为
时平衡常数为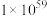 。下列说法正确的是
。下列说法正确的是| A.提高尾气净化效率的最佳途径是研制高效催化剂 |
| B.提高尾气净化效率的常用方法是降低温度 |
| C.装有该尾气净化装置的汽车排出的气体中不再含有NO和CO |
D.570K时及时抽走 和 和 ,可使平衡正向移动,同时化学平衡常数将增大,尾气净化效率更佳 ,可使平衡正向移动,同时化学平衡常数将增大,尾气净化效率更佳 |
更新时间:2020-02-07 16:33:36
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】化学与生活关系密切,下列说法错误的是
| A.在NO2和N2O4的平衡体系中,加压后颜色变深,可用勒夏特列原理解释 |
| B.将SOCl2与AlCl3·6H2O混合并加热,可得到无水氯化铝 |
| C.打开剧烈摇动后的碳酸饮料产生大量气泡的原因是压强对化学平衡的影响 |
| D.NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知化合物A与 在一定条件下反应生成化合物B与
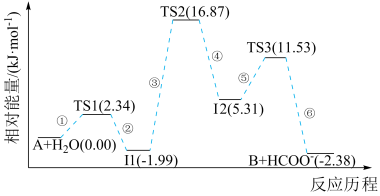
在一定条件下反应生成化合物B与 ,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法正确的是
,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法正确的是
 在一定条件下反应生成化合物B与
在一定条件下反应生成化合物B与 ,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法正确的是
,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法正确的是
| A.TS2所在的基元反应中活化分子百分数最大 |
B.该历程中的最大能垒(活化能) 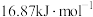 |
| C.使用催化剂只降低正反应的活化能,反应的焓变不变 |
| D.反应达到平衡状态后,升温使平衡逆向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】工业合成氨的反应原理为:N2(g) + 3H2(g)⇌2NH3(g) ΔH=-Q kJ/mol。下列说法正确的是
| A.工业上一般充入较多的氢气,以提高氢气的转化率 |
| B.合成氨的反应是放热反应,所以工业上选择反应温度越低越好 |
| C.若键能E(N≡N)=a kJ/mol,E(H-H)=b kJ/mol,E(H-N)=c kJ/mol,则Q=6c-a-3b |
| D.已知标况下44.8 L氢气燃烧生成水蒸气放热为571.6 kJ,则氢气燃烧热的热化学方程式可表示为2H2(g) + O2(g) = 2H2O(l) ΔH=-571.6 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】合成氨所需要的H2可由煤和水反应制得:
(1)H2O(g)+C(s) CO(g)+H2(g) ΔH>0
CO(g)+H2(g) ΔH>0
(2)CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0
CO2(g)+H2(g) ΔH<0
工业生产中,欲提高CO的转化率,所采用的下列措施最佳组合是
①降低温度 ②增大压强 ③使用催化剂 ④增大CO的浓度 ⑤增大H2O(g)的浓度
(1)H2O(g)+C(s)
 CO(g)+H2(g) ΔH>0
CO(g)+H2(g) ΔH>0(2)CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH<0
CO2(g)+H2(g) ΔH<0工业生产中,欲提高CO的转化率,所采用的下列措施最佳组合是
①降低温度 ②增大压强 ③使用催化剂 ④增大CO的浓度 ⑤增大H2O(g)的浓度
| A.①⑤ | B.②③ | C.②④⑤ | D.③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于物质工业制法的叙述不正确的是
| A.陶瓷、玻璃、水泥的生产中均用到了石灰石 |
| B.工业上合成氨需控制各项反应条件,实现反应速率和限度的综合最优 |
| C.工业制硫酸过程中,常用98.3%的浓硫酸吸收SO3 |
| D.氨催化氧化是工业制硝酸的基础 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】工业制硫酸的一步重要反应是SO2在400~600℃下的催化氧化:2SO2(g)+O2(g) 2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法正确的是
2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法正确的是
 2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法正确的是
2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法正确的是| A.使用催化剂可加快反应速率,提高SO3产率 |
| B.其它条件保持不变,温度越高,速率越快,生产效益越好 |
| C.实际生产中选定400~600℃作为操作温度,其原因是在此温度下催化剂的活性最高,SO2能100%转化为SO3 |
| D.增大压强可以提高SO3产率,但高压对动力和设备要求太高,会增加生产成本 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g) 2Z(g)+W(s) ΔH<0,下列叙述正确的是( )
2Z(g)+W(s) ΔH<0,下列叙述正确的是( )
 2Z(g)+W(s) ΔH<0,下列叙述正确的是( )
2Z(g)+W(s) ΔH<0,下列叙述正确的是( )| A.达到平衡时,X、Y的平衡转化率不同 |
| B.升高温度,平衡常数K值增大 |
| C.平衡常数K值越大,X的转化率越大 |
| D.达到平衡时,反应速率v正(X)=2v逆(Z) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知某密闭容器中发生可逆反应3H2(g) +N2(g)⇌2NH3(g) ΔH <0,t1时刻反应达到平衡,t2时刻改变某条件,其反应过程如图所示,下列说法正确的是
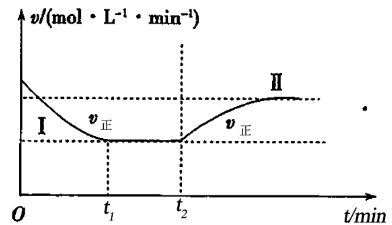

| A.t2时刻改变的条件可能是加入了催化剂 |
| B.过程I与过程II达到平衡后,平衡常数相等 |
| C.过程I与过程II达到平衡后,N2的转化率: I< II |
| D.若断裂3mol H-H键的同时形成6mol N-H键,则该反应达到平衡状态 |
您最近一年使用:0次

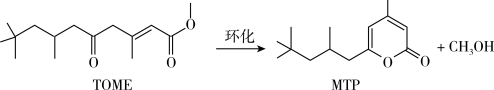
 ,反应过程中液体体积变化忽略不计。下列说法错误的是
,反应过程中液体体积变化忽略不计。下列说法错误的是