对常温下0.1mol·L-1的醋酸溶液,以下说法不正确的是( )
| A.由水电离出来的c(H+)>1.0×10-13mol·L-1 |
| B.c(CH3COOH)>c(H+)>c(CH3COO-)>c(OH-) |
| C.与同浓度的盐酸分别加水稀释10倍:pH(醋酸)>pH(盐酸) |
| D.与等浓度等体积NaOH溶液反应后的溶液中:c(CH3COOH)+c(CH3COO-)=0.1mol·L-1 |
更新时间:2020-02-12 15:16:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】化合物M是日常生活中常见的化学物质,其水溶液显碱性,结构为 。已知X、Y、Z、W为原子序数依次增大的短周期主族元素,X与W同主族。下列说法正确的是
。已知X、Y、Z、W为原子序数依次增大的短周期主族元素,X与W同主族。下列说法正确的是
 。已知X、Y、Z、W为原子序数依次增大的短周期主族元素,X与W同主族。下列说法正确的是
。已知X、Y、Z、W为原子序数依次增大的短周期主族元素,X与W同主族。下列说法正确的是| A.Z是空气中含量最高的元素 |
| B.X、W元素的简单离子均能影响水的电离 |
C.氧化物的熔点: |
| D.X与Y、X与Z元素均可形成10电子或18电子分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】与纯水的电离相似,液氨中也存在着微弱的电离:2NH3  NH4++NH2-.某温度下,液氨的离子积常数K=c(NH4+)·c(NH2-)=1.6×10-29 ,若用定义pH一样来规定pN=-lg c(NH4+),则在该温度下,下列叙述正确的是
NH4++NH2-.某温度下,液氨的离子积常数K=c(NH4+)·c(NH2-)=1.6×10-29 ,若用定义pH一样来规定pN=-lg c(NH4+),则在该温度下,下列叙述正确的是
 NH4++NH2-.某温度下,液氨的离子积常数K=c(NH4+)·c(NH2-)=1.6×10-29 ,若用定义pH一样来规定pN=-lg c(NH4+),则在该温度下,下列叙述正确的是
NH4++NH2-.某温度下,液氨的离子积常数K=c(NH4+)·c(NH2-)=1.6×10-29 ,若用定义pH一样来规定pN=-lg c(NH4+),则在该温度下,下列叙述正确的是| A.纯净的液氨中,pN=7 |
| B.液氨达到电离平衡时c(NH3)=c(NH4+)+c(NH2-) |
| C.1 L溶解有0.001 mol NH4C1的液氨溶液,其pN=3 |
| D.1 L溶解有0.001 mol NaNH2的液氨溶液,其pN=11 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法不正确的是

| A.常温下,pH均为3的盐酸和醋酸溶液等体积混合,pH不变 |
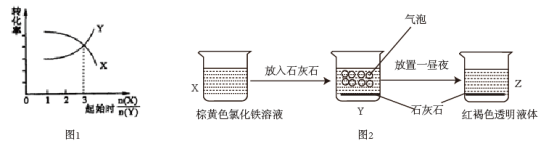
B.在一定条件下,将X和Y两种物质按不同的比例放入密闭容器中反应生成Z,平衡后测得X、Y的转化率与起始时两物质的物质的量之比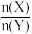 的关系如图1所示,则X与Y的反应方程式可表示为:X+3Y⇌nZ 的关系如图1所示,则X与Y的反应方程式可表示为:X+3Y⇌nZ |
| C.某同学在实验室进行了如图2所示的实验,则Y中反应的离子方程式为:3CaCO3+2Fe3++3H2O=2Fe(OH)3+3CO2↑+3Ca2+ |
D.在25℃时,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应完全时溶液中c( )=c(Cl-),用含a的代数式表示反应完全时NH3·H2O的电离常数 )=c(Cl-),用含a的代数式表示反应完全时NH3·H2O的电离常数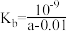 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列图像与对应实验操作相符合的是
A.在水中慢慢通入氨气至过量 |
B.在氢氧化钠和氢氧化钙混合溶液中通入二氧化碳至过量 |
C.在醋酸溶液中慢慢滴加同浓度的氨水至过量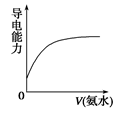 |
D.在氯化铝溶液中滴加氨水至过量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】NA代表阿伏加德罗常数的值。下列说法正确的是
| A.5.6 g 铁粉与足量硝酸加热充分反应后,产生H2的分子数为0.1NA |
| B.标准状况下22.4 LO2与足量H2反应生成H2O,转移的电子数为4NA |
| C.1 L0.1 mol/L硫酸钠溶液中含有的氧原子数为0.4NA |
| D.1 LpH=13的Ba(OH)2溶液中Ba2+数目为0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列叙述中,正确的是
| A.中和10mL 0.1mol·L-1 盐酸与中和100mL 0.01mol·L-1 的醋酸所需同种溶液的量不同 |
| B.等体积pH=3的酸溶液pH=11的碱溶液相混合后,溶液的pH=7 |
| C.体积相等,pH相等的盐酸和硫酸溶液中,H+离子的物质的量相等 |
| D.pH=3的盐酸溶液的H+的物质的量与pH=11的氨水溶液的OH-物质的量相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关实验的操作、现象和结论都正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 将装有 和 和 混合气体的烧瓶分别浸入冷水和热水中,并与常温情况进行对比( 混合气体的烧瓶分别浸入冷水和热水中,并与常温情况进行对比(  ) ) | 冷水中烧瓶内气体颜色变深,热水中烧瓶内气体颜色变浅 | 升高温度,化学平衡向吸热方向移动,降低温度,向放热方向移动 |
B | 在两个烧杯中分别盛有等体积、等浓度的烧碱溶液和氨水,插入电极,连接灯泡,接通电源,分别进行导电实验 | 盛有烧碱溶液的灯泡亮度大 | 强电解质导电能力大于弱电解质 |
C | 向盛有 溶液(显黄色)的①、②两支试管中分别滴加淀粉溶液、 溶液(显黄色)的①、②两支试管中分别滴加淀粉溶液、 溶液 溶液 | ①中溶液变蓝,②中产生黄色沉淀 | 溶液中存在平衡: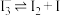 |
D | 用pH试纸分别测定等物质的量浓度的 和NaClO的pH 和NaClO的pH | pH: | 酸性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 H++OH-,在纯水中加入下列物质,能够使水的电离平衡向右移动的是
H++OH-,在纯水中加入下列物质,能够使水的电离平衡向右移动的是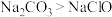
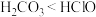
 ,下列叙述正确的是
,下列叙述正确的是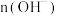 增大
增大 增大
增大 溶液,电离平衡正向移动,溶液中
溶液,电离平衡正向移动,溶液中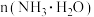 增大
增大 固体,电离平衡逆向移动,溶液中
固体,电离平衡逆向移动,溶液中 减少
减少

