某小型化工厂生产皓矾(ZnSO4·7H2O)的工艺流程如下图所示:
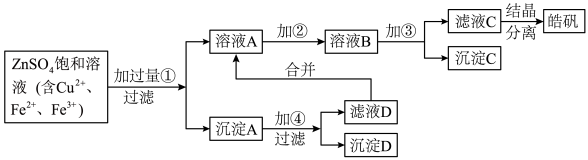
已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为Fe(OH)3:2.7~3.7;Fe(OH)2:7.6~9.6;Zn(OH)2:5.7~8.0。
试回答下列问题:
(1)加入的试剂①应是________ ,其目的是____________________________________ 。
(2)加入的试剂②,供选择使用的有:氨水、NaClO溶液、20% H2O2溶液、浓硫酸、浓硝酸等,应选用________ ,其理由是_____________________ 。
(3)加入的试剂③是________ ,目的是______________________________________ 。

已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为Fe(OH)3:2.7~3.7;Fe(OH)2:7.6~9.6;Zn(OH)2:5.7~8.0。
试回答下列问题:
(1)加入的试剂①应是
(2)加入的试剂②,供选择使用的有:氨水、NaClO溶液、20% H2O2溶液、浓硫酸、浓硝酸等,应选用
(3)加入的试剂③是
更新时间:2020-02-20 19:13:03
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌(含有少量的FeO、MnO、NiO等杂质)的工艺流程如下:

已知:①在本实验条件下,Ni2+不能被氧化;高锰酸钾的还原产物是MnO2。
②氧化性:Ni2+> Zn2+。
回答下列问题:
(1)为了加快工业级ZnO与稀硫酸的反应速率,通常采用的方法是___________ (填一种即可)。
(2)过滤时,常用到的玻璃仪器有玻璃棒、烧杯和___________ ,其中玻璃棒的主要作用是___________ 。
(3)在加高锰酸钾溶液前,若pH较低,则对除杂的影响是___________ 。
(4)“过滤I”得到的滤液中含有的阳离子为___________ (填离子符号)。
(5)写出②中发生反应的化学方程式:___________ 。
(6)“滤饼”的主要成分可能是ZnCO3·xZn(OH)2.取干燥后的滤饼21.1 g,煅烧后可得到产品16.2 g,则x=___________ 。

已知:①在本实验条件下,Ni2+不能被氧化;高锰酸钾的还原产物是MnO2。
②氧化性:Ni2+> Zn2+。
回答下列问题:
(1)为了加快工业级ZnO与稀硫酸的反应速率,通常采用的方法是
(2)过滤时,常用到的玻璃仪器有玻璃棒、烧杯和
(3)在加高锰酸钾溶液前,若pH较低,则对除杂的影响是
(4)“过滤I”得到的滤液中含有的阳离子为
(5)写出②中发生反应的化学方程式:
(6)“滤饼”的主要成分可能是ZnCO3·xZn(OH)2.取干燥后的滤饼21.1 g,煅烧后可得到产品16.2 g,则x=
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】SO2、NO是大气污染物。吸收废气中的SO2和NO,获得Na2SO3和NH4NO3产品的流程如图:

(1)操作Ⅰ的名称是___________ 。
(2)写出NO与NaOH溶液、O2反应,生成等物质的量的 和
和 的离子方程式:
的离子方程式:___________ 。
(3)由NaNO2、NaNO3制备NH4NO3时再次通入O2的目的是___________ 。
(4)Na2SO3存放时易被部分氧化,检验所获得的无水)Na2SO3产品中是否混有Na2SO4所需要的试剂是___________ 。
(5)某化学兴趣小组设计了如图实验方案来测定某无水亚硫酸钠试剂的纯度。实验过程如图:

a.如何判断实验④中沉淀已完全___________ 。
b.①称量样品的质量为a克,⑦称量的质量为b克,样品中无水亚硫酸钠的质量分数是:___________ 。
c.若⑤中沉淀未洗涤干净,测定结果将___________ (填“偏高”、“偏低”、“无影响”)。

(1)操作Ⅰ的名称是
(2)写出NO与NaOH溶液、O2反应,生成等物质的量的
 和
和 的离子方程式:
的离子方程式:(3)由NaNO2、NaNO3制备NH4NO3时再次通入O2的目的是
(4)Na2SO3存放时易被部分氧化,检验所获得的无水)Na2SO3产品中是否混有Na2SO4所需要的试剂是
(5)某化学兴趣小组设计了如图实验方案来测定某无水亚硫酸钠试剂的纯度。实验过程如图:

a.如何判断实验④中沉淀已完全
b.①称量样品的质量为a克,⑦称量的质量为b克,样品中无水亚硫酸钠的质量分数是:
c.若⑤中沉淀未洗涤干净,测定结果将
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室制备苯乙酮的化学方程式为: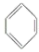 +(CH3CO)2O
+(CH3CO)2O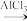
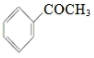 +CH3COOH。制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑
+CH3COOH。制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑ 等副反应。主要实验装置和步骤如图:
等副反应。主要实验装置和步骤如图:
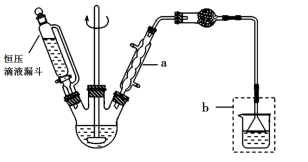
(I)合成:
在三颈烧瓶中加入20g无水AlCl3和30mL无水苯。边搅拌边慢慢滴加6mL乙酸酐和10mL无水苯的混合液,使反应液缓缓回流。滴加完毕后加热回流1小时,形成黑黄色液体。
(Ⅱ)分离与提纯:
将冷却后的反应瓶置于冰水浴中,加入15mL苯,慢慢加入混合的盐酸冰水,静置分层,分液,无机相用乙醚萃取,与有机相合并,有机相用10%NaOH溶液洗涤,分液,弃去无机层,有机层用9mL水洗,分液,弃去无机层,有机层用MgSO4干燥,得到苯乙酮粗产品。
回答下列问题:
(1)仪器a的名称:___ ;使用恒压滴定漏斗的优点是:___ 。
(2)球形干燥管的作用是___ 。
(3)若将乙酸酐和苯的混合液一次性倒入三颈烧瓶,可能导致__ 。
A.反应太剧烈 B.液体太多搅不动 C.反应变缓慢 D.副产物增多
(4)分离和提纯操作中是否可改用乙醇萃取?___ (填“是”或“否”),原因是___ 。
(5)分液漏斗使用前须___ 并洗净备用。萃取时,先后加入待萃取液和萃取剂,经振荡并__ 后,将分液漏斗置于铁架台的铁圈上静置片刻,分层。分离上下层液体时,应先___ ,然后打开活塞放出下层液体,上层液体从上口倒出。
(6)已知常压下:
则从粗产品中提纯苯乙酮使用的操作是___ ;为了收集纯净的苯乙酮馏分,分离苯乙酮应使用下面的图___ 装置。
 +(CH3CO)2O
+(CH3CO)2O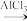
 +CH3COOH。制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑
+CH3COOH。制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑ 等副反应。主要实验装置和步骤如图:
等副反应。主要实验装置和步骤如图:
(I)合成:
在三颈烧瓶中加入20g无水AlCl3和30mL无水苯。边搅拌边慢慢滴加6mL乙酸酐和10mL无水苯的混合液,使反应液缓缓回流。滴加完毕后加热回流1小时,形成黑黄色液体。
(Ⅱ)分离与提纯:
将冷却后的反应瓶置于冰水浴中,加入15mL苯,慢慢加入混合的盐酸冰水,静置分层,分液,无机相用乙醚萃取,与有机相合并,有机相用10%NaOH溶液洗涤,分液,弃去无机层,有机层用9mL水洗,分液,弃去无机层,有机层用MgSO4干燥,得到苯乙酮粗产品。
回答下列问题:
(1)仪器a的名称:
(2)球形干燥管的作用是
(3)若将乙酸酐和苯的混合液一次性倒入三颈烧瓶,可能导致
A.反应太剧烈 B.液体太多搅不动 C.反应变缓慢 D.副产物增多
(4)分离和提纯操作中是否可改用乙醇萃取?
(5)分液漏斗使用前须
(6)已知常压下:
| 熔点/℃ | 沸点/℃ | |
| 苯 | 5.5 | 80.1 |
| 乙醚 | -116.3 | 34.6 |
| 苯乙酮 | 19.6 | 202 |

您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】苯胺(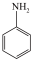 )是重要的化工原料。某兴趣小组在实验室里制取并纯化苯胺。
)是重要的化工原料。某兴趣小组在实验室里制取并纯化苯胺。
已知:① 与NH3相似,与盐酸反应生成
与NH3相似,与盐酸反应生成 (易溶于水的盐)。
(易溶于水的盐)。
②用硝基苯制取苯胺的反应为:2 +3Sn+12HCl
+3Sn+12HCl 2
2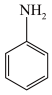 +3SnCl4+4H2O
+3SnCl4+4H2O
③有关物质的部分物理性质见下表:
Ⅰ.制备苯胺
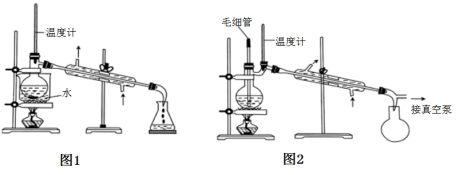
图1所示装置中加入20mL浓盐酸(过量),置于热水浴中回流20min,使硝基苯充分还原;冷却后,向三颈烧瓶中滴入一定量50%NaOH溶液,至溶液呈碱性。
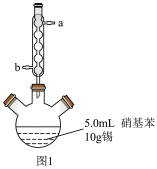
(1)滴加适量NaOH溶液的目的是___ ,写出主要反应的离子方程式___ 。
Ⅱ.纯化苯胺
ⅰ.取出图l所示装置中的三颈烧瓶,改装为图2所示装置。加热装置A产生水蒸气。用“水蒸气蒸馏”的方法把B中苯胺逐渐吹出,在烧瓶C中收集到苯胺与水的混合物;分离混合物得到粗苯胺和水溶液甲。
ⅱ.向所得水溶液甲中加入氯化钠固体至饱和,再用乙醚萃取,得到乙醚萃取液。
iii.合并粗苯胺和乙醚萃取液,用NaOH固体干燥,蒸馏后得到苯胺1.86g。

(2)装置A中玻璃管的作用是__ 。
(3)在苯胺吹出完毕后,应进行的操作是先__ ,再___ 。
(4)该实验中苯胺的产率为___ (保留三位有效数字)。
(5)欲在不加热条件下除去苯胺中少量的硝基苯杂质,简述实验方案___ 。
 )是重要的化工原料。某兴趣小组在实验室里制取并纯化苯胺。
)是重要的化工原料。某兴趣小组在实验室里制取并纯化苯胺。已知:①
 与NH3相似,与盐酸反应生成
与NH3相似,与盐酸反应生成 (易溶于水的盐)。
(易溶于水的盐)。②用硝基苯制取苯胺的反应为:2
 +3Sn+12HCl
+3Sn+12HCl 2
2 +3SnCl4+4H2O
+3SnCl4+4H2O③有关物质的部分物理性质见下表:
| 物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度/g·cm-3 |
| 苯胺 | 93 | 6.3 | 184 | 微溶于水,易溶于乙醚 | 1.02 |
| 硝基苯 | 123 | 5.7 | 210.9 | 难溶于水,易溶于乙醚 | 1.23 |
| 乙醚 | 74 | 116.2 | 34.6 | 微溶于水 | 0.7134 |
图1所示装置中加入20mL浓盐酸(过量),置于热水浴中回流20min,使硝基苯充分还原;冷却后,向三颈烧瓶中滴入一定量50%NaOH溶液,至溶液呈碱性。

(1)滴加适量NaOH溶液的目的是
Ⅱ.纯化苯胺
ⅰ.取出图l所示装置中的三颈烧瓶,改装为图2所示装置。加热装置A产生水蒸气。用“水蒸气蒸馏”的方法把B中苯胺逐渐吹出,在烧瓶C中收集到苯胺与水的混合物;分离混合物得到粗苯胺和水溶液甲。
ⅱ.向所得水溶液甲中加入氯化钠固体至饱和,再用乙醚萃取,得到乙醚萃取液。
iii.合并粗苯胺和乙醚萃取液,用NaOH固体干燥,蒸馏后得到苯胺1.86g。

(2)装置A中玻璃管的作用是
(3)在苯胺吹出完毕后,应进行的操作是先
(4)该实验中苯胺的产率为
(5)欲在不加热条件下除去苯胺中少量的硝基苯杂质,简述实验方案
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】轻质氧化镁是新型功能复合材料的重要添加剂,可以菱镁矿(含MgCO3、CaCO3、Fe2O3、Al2O3、SiO2)为原料制备,其制备流程如图:
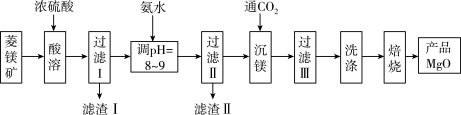
(1)酸溶时,为了提高矿物的浸取率可采取的措施有__ 。(答一条即可)
(2)浓硫酸与Al2O3反应的化学方程式为__ ;滤渣Ⅰ的主要成分为__ (填化学式)。
(3)用氨水调节溶液pH=8~9的目的是__ ,若氨水加的量较多使pH>9,则最终氧化镁的产量会__ (填“增大”“不变”或“减小”)。
(4)沉镁时发生反应的离子方程式为__ 。
(5)流程中“焙烧”操作若在实验室中进行,样品应放在__ (填实验仪器)中加热,当__ 时,说明固体样品已分解完全。

(1)酸溶时,为了提高矿物的浸取率可采取的措施有
(2)浓硫酸与Al2O3反应的化学方程式为
(3)用氨水调节溶液pH=8~9的目的是
(4)沉镁时发生反应的离子方程式为
(5)流程中“焙烧”操作若在实验室中进行,样品应放在
您最近半年使用:0次
【推荐3】Li2CO3是生产锂电池的重要原料,电解铝废渣(主要含AlF3、LiF、NaF、CaO等物质)可用于制备Li2CO3。
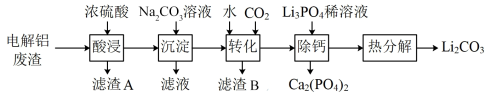
已知:①Li2CO3的溶解度:0 ℃ 1.54 g;20 ℃ 1.33 g;80 ℃ 0.85 g。
②20 ℃,Ksp[Ca3(PO4)2]=2×10-33,Ksp(CaHPO4)=1×10-7。
(1)在加热条件下酸浸,反应生成能腐蚀玻璃的气体,写出AlF3发生反应的化学方程式:______ 。
(2)滤渣B的主要成分是________ 。
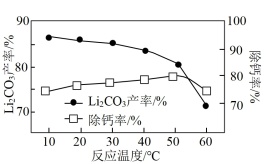
(3)“转化”后所得LiHCO3溶液中含有的Ca2+需要加入Li3PO4除去。除钙步骤中其他条件不变,反应相同时间,温度对除钙率和Li2CO3产率的影响如右图所示。
①随着温度升高最终Li2CO3的产率逐渐减小的原因是___________ 。
②当温度高于50 ℃时,除钙率下降的原因可能是__________________ 。
(4)热分解后,获得Li2CO3需趁热过滤的原因是_______________________ 。
(5)将酸浸时产生的气体通入Al(OH)3和Na2SO4溶液的混合物中可产生难溶物冰晶石(Na3AlF6),该反应的离子方程式为_______________________________________ 。

已知:①Li2CO3的溶解度:0 ℃ 1.54 g;20 ℃ 1.33 g;80 ℃ 0.85 g。
②20 ℃,Ksp[Ca3(PO4)2]=2×10-33,Ksp(CaHPO4)=1×10-7。
(1)在加热条件下酸浸,反应生成能腐蚀玻璃的气体,写出AlF3发生反应的化学方程式:

(2)滤渣B的主要成分是
(3)“转化”后所得LiHCO3溶液中含有的Ca2+需要加入Li3PO4除去。除钙步骤中其他条件不变,反应相同时间,温度对除钙率和Li2CO3产率的影响如右图所示。
①随着温度升高最终Li2CO3的产率逐渐减小的原因是
②当温度高于50 ℃时,除钙率下降的原因可能是
(4)热分解后,获得Li2CO3需趁热过滤的原因是
(5)将酸浸时产生的气体通入Al(OH)3和Na2SO4溶液的混合物中可产生难溶物冰晶石(Na3AlF6),该反应的离子方程式为
您最近半年使用:0次



