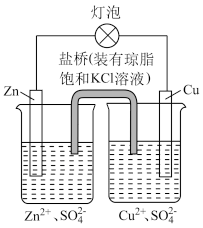
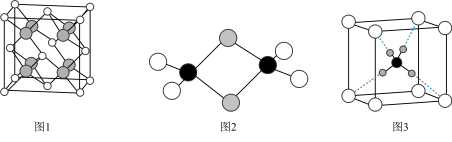
下列说法错误的是( )
| A.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B.强电解质在液态时,有的导电,有的不导电 |
| C.反应速率常数与浓度无关,但受温度、催化剂、固体表面性质等因素的影响 |
| D.温度一定,当溶液中Ag+和Cl-浓度的乘积等于Ksp时,溶液为AgCl的饱和溶液 |
更新时间:2020-02-24 12:44:01
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s)+2NO(g) CO(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
CO(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )

 CO(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
CO(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
| A.该反应的△H>0 |
| B.若该反应在T1、T2℃时的平衡常数分别为K1、K2,则K1<K2 |
| C.在T2℃时,若反应体系处于状态D,则此时v正>v逆 |
| D.若状态B、C、D的速率分别为v(B)、 v(C)、 v(D),则v(C)=v(D)>v(B) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某MOFs多孔材料孔径大小和形状恰好将N2O4“固定”,能将工业废气中的NO2高效转化为HNO3.原理示意图如下。
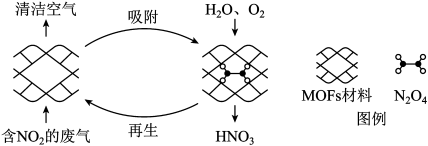
已知:2NO2(g) N2O4(g)
N2O4(g)  <0。下列说法不正确的是
<0。下列说法不正确的是

已知:2NO2(g)
 N2O4(g)
N2O4(g)  <0。下列说法不正确的是
<0。下列说法不正确的是| A.MOFs-N2O4是一种超分子 |
| B.温度升高时不利于N2O4被MOFs固定 |
C.一定温度下,多孔材料“固定”N2O4,可提高2NO2(g) N2O4(g)的平衡常数 N2O4(g)的平衡常数 |
| D.每获得0.1molHNO3时,转移电子的数目为6.02×1022 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】用活性炭还原NO2可防止空气污染,其反应原理为2C(s)+2NO2(g) N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。
N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。
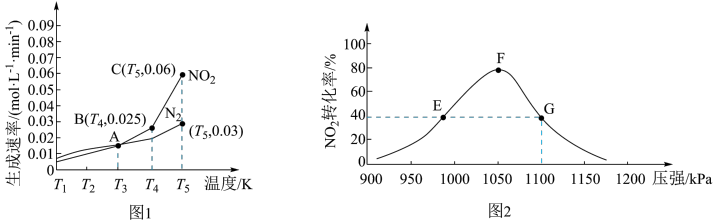
下列说法正确的是
 N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。
N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。 
下列说法正确的是
A.图1中的A、B、C三个点中只有A点的 正= 正= 逆 逆 |
B.图2中E点的 逆大于F点的 逆大于F点的 正 正 |
| C.图2中平衡常数K(E)=K(G),则NO2的平衡浓度c(E)=c(G) |
| D.G点时NO2的分压为550kPa |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法不正确的是
| A.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| B.已知常温下Ksp[Mg(OH)2]=1.8×10-11,则Mg(OH)2在pH=12的NaOH溶液中的溶解度约为1.044×10-6g |
| C.水能、风能、生物质能是可再生能源,煤、石油、天然气是不可再生能源 |
| D.用酚醛树脂制成的塑料可反复加热熔融加工 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验操作、现象和所得出结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向淀粉溶液中加入稀硫酸,加热一段时间后,再加入新制Cu(OH)2,加热 | 没有出现砖红色沉淀 | 淀粉没有水解 |
| B | 取少量Mg(OH)2悬浊液,向其中滴加适量浓CH3COONH4溶液 | Mg(OH)2溶解 | CH3COONH4溶液呈酸性 |
| C | 将浸透石蜡油的石棉放置在硬质试管底部,加入少量碎瓷片并加强热,将生成的气体通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色 | 石蜡油分解产物中含有不饱和烃 |
| D | 将海带剪碎,灼烧成灰,加蒸馏水浸泡,取滤液滴加硫酸溶液,再加入淀粉溶液 | 溶液变蓝 | 海带中含有丰富的I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验中,实验现象与结论均匹配的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 取5 mL 0.1mol·L-1 KI溶液于试管中,加入1 mL 0.1 mol·L-1FeCl3溶液,充分反应后萃取分液,向水层滴KSCN溶液 | 溶液变血红色 | KI与FeCl3的反应有一定限度 |
| B | 向酸性KMnO4溶液中滴加H2O2溶液 | 紫色褪去并产生气泡 | H2O2具有氧化性 |
| C | 取等浓度等体积的Na2S、NaCl溶液于试管中,分别滴入几滴酚酞 | Na2S溶液变红、NaCl溶液无色 | 非金属性:Cl>S |
| D | 向2 mL 1 mol/L NaOH溶液中先加入3滴1 mol/L MgCl2溶液,再加入3滴1 mol/L FeCl2溶液 | 先产生白色沉淀,后生成红褐色沉淀 | 证明KspMg(OH)2]>Ksp[Fe(OH)3] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。下列叙述正确的是


| A.溶液中的K+移向b电极 |
| B.a极的电极反应式为:2H++2e—= H2↑ |
| C.b极为负极,该电极上发生氧化反应 |
| D.电子由a极经电解质溶液移向b极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NaBH4-H2O2 燃料电池有望成为低温环境下工作的便携式燃料电池,其工作原理如图所示。下列有关 NaBH4-H2O2 燃料电池的说法错误的是
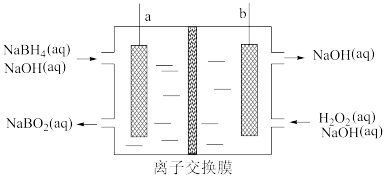

| A.b 为正极,电极反应为:H2O2+2e-=2OH- |
| B.放电过程中,a 极区 B 元素被氧化 |
| C.放电过程中,b 极区 NaOH 浓度增大 |
| D.电池中的离子交换膜为阳离子交换膜 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列的排序不 正确的是
| A.晶体熔点由低到高:CF4 < CCl4 < CBr4 < CI4 | B.沸点由高到低:Na>Mg>Al |
| C.硬度由大到小:金刚石 > SiC >晶体硅 | D.晶格能由大到小: MgF2> NaCl > NaBr |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在通常情况下,下列各组物质的物理性质排列正确的是( )
| A.水溶性:HCl >SO2>NH3 | B.熔点:H2O>HBr>HCl |
| C.沸点:乙烷>丁烷>己烷 | D.密度:K>Na>Li |
您最近一年使用:0次