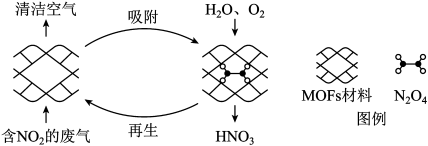
某MOFs多孔材料孔径大小和形状恰好将N2O4“固定”,能将工业废气中的NO2高效转化为HNO3.原理示意图如下。
已知:2NO2(g) N2O4(g)
N2O4(g)  <0。下列说法不正确的是
<0。下列说法不正确的是

已知:2NO2(g)
 N2O4(g)
N2O4(g)  <0。下列说法不正确的是
<0。下列说法不正确的是| A.MOFs-N2O4是一种超分子 |
| B.温度升高时不利于N2O4被MOFs固定 |
C.一定温度下,多孔材料“固定”N2O4,可提高2NO2(g) N2O4(g)的平衡常数 N2O4(g)的平衡常数 |
| D.每获得0.1molHNO3时,转移电子的数目为6.02×1022 |
更新时间:2024-03-05 09:54:20
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】室温下,下列实验探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 将两只装有NO2的玻璃球分别置于冷水和热水中 | 温度对化学平衡产生影响 |
| B | 向盛有淀粉、KI的溶液中滴加HNO3酸化的 溶液,振荡 溶液,振荡 | 比较Fe3+和I2的氧化性 |
| C | 用pH计分别测量等体积HCOOH和CH3COOH溶液的pH | 推电子基团对羧基酸性影响的比较 |
| D | 向溴水中滴加少量乙醇,振荡 | 比较Br2在水中和乙醇中溶解度的大小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在一定条件下,取相同初始量的A和B,分别在2L、6L刚性密闭容器中发生下列反应:aA(g)+bB(s) mM(g)+nN(g) △H=
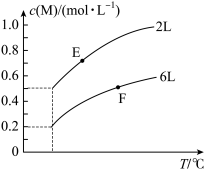
mM(g)+nN(g) △H= 。达到平衡时,M的浓度与温度、容器的容积的关系如图所示。下列有关判断正确的是
。达到平衡时,M的浓度与温度、容器的容积的关系如图所示。下列有关判断正确的是
 mM(g)+nN(g) △H=
mM(g)+nN(g) △H= 。达到平衡时,M的浓度与温度、容器的容积的关系如图所示。下列有关判断正确的是
。达到平衡时,M的浓度与温度、容器的容积的关系如图所示。下列有关判断正确的是
| A.在E点增大压强,A的体积分数变小 |
| B.达到平衡后,增大B的量将会提高A的转化率 |
| C.降低温度,气体的总质量减小 |
| D.其他条件不变,增大压强能使状态F转变到E |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列叙述正确的是
| A.常温下,将pH=4的醋酸溶液加水稀释,溶液中所有离子的浓度均降低 |
| B.反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)常温下能自发进行,该反应的ΔH>0 |
C.在一容积可变的密闭容器中反应2SO2(g)+O2(g)⇌ 2SO3(g)达平衡后,保持温度不变,缩小体积,平衡正向移动,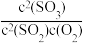 的值不变 的值不变 |
| D.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】CO2催化加氢制取甲醇、乙醇等低碳醇的研究,对于环境问题和能源文体都具有非常重要的意义。已知一定条件下的如下反应:
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=﹣49.0kJ•mol-1
2CO2(g)+6H2(g)⇌CH3CH2OH(g)+3H2O(g) △H=﹣173.6kJ•mol-1
下列说法不正确的是
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=﹣49.0kJ•mol-1
2CO2(g)+6H2(g)⇌CH3CH2OH(g)+3H2O(g) △H=﹣173.6kJ•mol-1
下列说法不正确的是
| A.CH3OH(g)+CO2(g)+3H2(g)⇌CH3CH2OH(g)+2H2O(g) △H<0 |
| B.增大压强,有利于反应向生成低碳醇的方向移动,平衡常数增大 |
| C.升高温度,可加快生成低碳醇的速率,但反应限度减小 |
| D.增大氢气浓度可以提高二氧化碳的转化率 |
您最近一年使用:0次

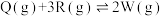
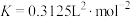
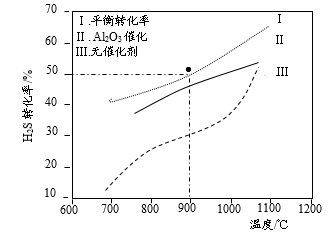
 ,控制不同温度和分别在有、无
,控制不同温度和分别在有、无 催化时进行
催化时进行 的分解实验[反应为:
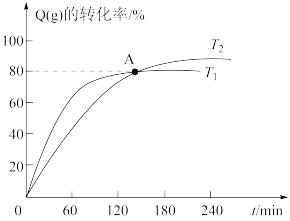
的分解实验[反应为: ]。测得的结果如下图所示(曲线II、III表示经过相同时间且未达到化学平衡时
]。测得的结果如下图所示(曲线II、III表示经过相同时间且未达到化学平衡时