(1)取7.90gKMnO4(Mr=158)固体加热后收集a mol气体剩余固体W g,在剩余固体中加入足够盐酸又收集到b mol气体(此时产物中锰元素全部以Mn2+存在),请计算
①如W为7.26g,则KMnO4的分解率_____________
②a+b的最小值为_____________
(2)称取 (Mr=132)和
(Mr=132)和 (Mr=15)混合物样品7.24g,加入含0.1 mol NaOH溶液全反应,生成NH3体积1792mL(标准状况),则
(Mr=15)混合物样品7.24g,加入含0.1 mol NaOH溶液全反应,生成NH3体积1792mL(标准状况),则 和
和 的物质的之比为
的物质的之比为___________ (答成小数形式,保留2位小数)请简要写出推理和计算过程。
①如W为7.26g,则KMnO4的分解率
②a+b的最小值为
(2)称取
 (Mr=132)和
(Mr=132)和 (Mr=15)混合物样品7.24g,加入含0.1 mol NaOH溶液全反应,生成NH3体积1792mL(标准状况),则
(Mr=15)混合物样品7.24g,加入含0.1 mol NaOH溶液全反应,生成NH3体积1792mL(标准状况),则 和
和 的物质的之比为
的物质的之比为
19-20高二·浙江·期末 查看更多[1]
(已下线)【新东方】2020-77
更新时间:2020-02-27 21:56:53
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】按要求回答下列问题:
(1)含有相同碳原子数的CO和CO2,其质量比为________ 。
(2)标准状况下有①44.8L CH4,②9.03×1023个NH3分子,③85g H2S三种气体,这三种气体的物质的量从大到小的顺序是________ 。
(3)若1g CO2中含有x个原子,则阿伏加 德罗常数可表示为________ 。
(4)4.9g H2SO4含________ 个H2SO4分子,能和________ mol NaOH完全反应。
(1)含有相同碳原子数的CO和CO2,其质量比为
(2)标准状况下有①44.8L CH4,②9.03×1023个NH3分子,③85g H2S三种气体,这三种气体的物质的量从大到小的顺序是
(3)若1g CO2中含有x个原子,则阿伏加 德罗常数可表示为
(4)4.9g H2SO4含
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)有以下四种物质 ①22g二氧化碳;②5g氢气;③1.204╳1024个氮气分子; ④4℃时18g水,它们所含分子数最多的是_________________ ;质量最大的是____________ ;常温时体积最大的是_______________ (填序号)。
(2)V L Fe2(SO4)3溶液中含Fe3+mg,则溶液中SO42-的物质的量浓度为________ mol·L-1
(3)标况下,mg 气体A和ng气体B具有相等的体积,则同温同压下的密度之比为________ , 同质量的A、B的分子数目之比为________ 。
(4)在无土栽培中,配制1 L内含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为_____________ 、_________________ 。
(2)V L Fe2(SO4)3溶液中含Fe3+mg,则溶液中SO42-的物质的量浓度为
(3)标况下,mg 气体A和ng气体B具有相等的体积,则同温同压下的密度之比为
(4)在无土栽培中,配制1 L内含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)与16gO2所含原子总数相同的NH3标准状况下体积是________ L;
(2)已知2LAl2(SO4)3溶液中c(Al3+)=3mol/L,则c(SO42-)=__________ ,与3L__________ mol/LNa2SO4中SO42-的物质的量浓度相等。
(3)同温同压下,同体积的NH3和H2S气体的质量比为_____________ ;同质量的NH3和H2S气体的体积比为___________ ;若二者氢原子数相等,它们的体积比为____________ 。
(4)在标准状况下,8.96L的CH4和CO的混合气体,混合气体对氢气相对密度是9.5,混合气体平均摩尔质量为__________ ,混合气体中CH4的体积为__________ ,一氧化碳的质量分数为__________ ,二者原子个数比为_______________ 。
(2)已知2LAl2(SO4)3溶液中c(Al3+)=3mol/L,则c(SO42-)=
(3)同温同压下,同体积的NH3和H2S气体的质量比为
(4)在标准状况下,8.96L的CH4和CO的混合气体,混合气体对氢气相对密度是9.5,混合气体平均摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】称取一定质量镁铝合金放入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图(生成沉淀阶段的图象斜率视为恒定)。
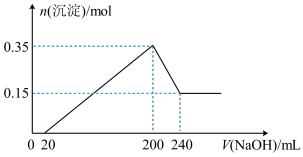
计算:
(1)合金中Al的质量为多少____ ?
(2)所加NaOH溶液的物质的量浓度为多少____ ?

计算:
(1)合金中Al的质量为多少
(2)所加NaOH溶液的物质的量浓度为多少
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)在2L的密闭容器中,加入2molSO2、1.2molO2,充分反应后,容器内压强为反应前的3/4,则SO2、O2 的转化率分别为多少?___________ 、 __________ 。
(2)将11. 2L标准状况下的甲烷和乙烯的混合气体通入足量的溴的四氯化碳溶液中充分反应,溴的四氯化碳溶液增加了5.6g,求原混合气体中甲烷与乙烯的质量之比。__________ 。
(2)将11. 2L标准状况下的甲烷和乙烯的混合气体通入足量的溴的四氯化碳溶液中充分反应,溴的四氯化碳溶液增加了5.6g,求原混合气体中甲烷与乙烯的质量之比。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)若1.92 g Cu粉与一定量浓HNO3反应,当Cu完全反应时,收集到标准状况下1.12L气体,则消耗硝酸________ mol,生成NO2________ mol;
(2)若向Cu中加入硫酸和硝酸的混酸溶液制取CuSO4溶液,则混酸中硫酸与硝酸的最佳物质的量之比为__________ 。
(2)若向Cu中加入硫酸和硝酸的混酸溶液制取CuSO4溶液,则混酸中硫酸与硝酸的最佳物质的量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)用KMnO4氧化盐酸溶液,反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,若产生的Cl2在标准状况下体积为56L,计算:参加反应的HCl的物质的量_______ 反应中被氧化的HCl的物质的量_______
(2)向某硝酸银溶液中,逐滴加入密度为1.10g·mL-1的盐酸溶液,恰好完全反应时,过滤所得沉淀的质量恰好与盐酸溶液的质量相等。求盐酸的质量分数_______ (需要过程)。
(2)向某硝酸银溶液中,逐滴加入密度为1.10g·mL-1的盐酸溶液,恰好完全反应时,过滤所得沉淀的质量恰好与盐酸溶液的质量相等。求盐酸的质量分数
您最近一年使用:0次

 、
、 、
、 、
、 四种气体中,含有分子数目最多的是
四种气体中,含有分子数目最多的是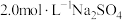 溶液和
溶液和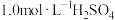 溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和),则
溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和),则 的物质的量浓度为
的物质的量浓度为
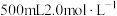 的盐酸中,金属完全溶解,再加入
的盐酸中,金属完全溶解,再加入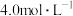 的NaOH溶液,若要生成的沉淀最多,则应加入NaOH溶液的体积是
的NaOH溶液,若要生成的沉淀最多,则应加入NaOH溶液的体积是

