某一反应体系中,有反应物和生成物共六种物质,这六种物质是:Cl2、KMnO4、MnCl2、H2O、HCl(浓)、KCl,其中KMnO4→ MnCl2。
(1)该反应中的化学方程式为_____________________________________________ 。
(2)该反应中,氧化产物与还原产物的物质的量之比为_____________________________ 。
(3)若产生的气体在标准状况下体积为2.24 L,则反应过程中被氧化的物质为________ NA(NA表示阿伏加德罗常数的值)。
(4)市售的浓盐酸(密度为1.19g/cm3)在工业上是用500 L HCl气体(标准状况)与1 L H2O的比例配制成的,则该盐酸的物质的量浓度是___________ mol/L(结果保留一位小数)。
(5)现需用1.20 mol/L的稀盐酸480 mL, 应量取市售浓盐酸________ mL进行配制。
(6)取6.00 g硬铝合金(假设只含铝铜硅),与 (5) 中所配稀盐酸进行充分反应,收集到气体5.60 L(标准状况),则硬铝合金中铝的质量分数为____________ 。
(1)该反应中的化学方程式为
(2)该反应中,氧化产物与还原产物的物质的量之比为
(3)若产生的气体在标准状况下体积为2.24 L,则反应过程中被氧化的物质为
(4)市售的浓盐酸(密度为1.19g/cm3)在工业上是用500 L HCl气体(标准状况)与1 L H2O的比例配制成的,则该盐酸的物质的量浓度是
(5)现需用1.20 mol/L的稀盐酸480 mL, 应量取市售浓盐酸
(6)取6.00 g硬铝合金(假设只含铝铜硅),与 (5) 中所配稀盐酸进行充分反应,收集到气体5.60 L(标准状况),则硬铝合金中铝的质量分数为
12-13高一上·重庆·期末 查看更多[2]
(已下线)2011-2012学年重庆市西南大学附属中学高一上学期期末考试化学试卷(已下线)第二章 元素与物质世界(基础过关)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)
更新时间:2016-12-09 02:50:32
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】酸性条件下,许多氧化剂可使KI溶液中的I-氧化,例如KIO3(IO3-→I2)、H2O2(H2O2→H2O)、FeCl3(Fe3+→Fe2+)、K2Cr2O7(Cr2O72-→Cr3+).请根据题目要求填空:
(1)写出在醋酸存在的条件下KIO3溶液与KI溶液反应的离子方程式______________ 。
(2)在酸性条件下(足量),各取1L浓度为1mol•L-1的KI溶液分别与上述列举四种溶液进行完全反应,则需要溶质的物质的量之比为n(KIO3):n(H2O2):n(FeCl3):n(K2Cr2O7)=______________________ (要求写出最简比)
(1)写出在醋酸存在的条件下KIO3溶液与KI溶液反应的离子方程式
(2)在酸性条件下(足量),各取1L浓度为1mol•L-1的KI溶液分别与上述列举四种溶液进行完全反应,则需要溶质的物质的量之比为n(KIO3):n(H2O2):n(FeCl3):n(K2Cr2O7)=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】计算
(1)已知酸性条件下, 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,
①写出该反应的离子方程式______ 。
②被还原的 的质量为
的质量为______ 。
(2)为了检验某含有 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为______ (用含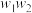 的代数式来表示)。
的代数式来表示)。
(3)有一块表面氧化成氧化钠的金属钠,总质量为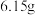 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程_____ 。
(1)已知酸性条件下,
 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,①写出该反应的离子方程式
②被还原的
 的质量为
的质量为(2)为了检验某含有
 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为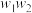 的代数式来表示)。
的代数式来表示)。(3)有一块表面氧化成氧化钠的金属钠,总质量为
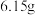 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】硝酸盐受热分解的产物与硝酸盐的组成以及受热的温度等因素有关。
(1)一定条件下硝酸铵受热分解的未配平化学反应方程式为:NH4NO3 =HNO3 + N2 + H2O在反应中被氧化与被还原的氮原子数之比为__________
(2)某硝酸盐受热分解的产物为不含氮元素的固体物质和NO2、O2气体,若产生NO2和O2的物质的量之比为8︰1,则金属元素的价态在反应过程中________ (填“升高”、“降低”、“不变”)。若该硝酸盐的化学式表示为M(NO3)2,则其受热分解的化学方程式为_______________________________________ 。
(3)2mol Cu(NO3)2和AgNO3混合物,加热使其分解,得到NO2、O2二种气体和CuO、Ag二种固体,将产生的NO2、O2混合气体经水充分吸收后,剩余气体是________ ,其物质的量(mol)范围是________________ 。
(1)一定条件下硝酸铵受热分解的未配平化学反应方程式为:NH4NO3 =HNO3 + N2 + H2O在反应中被氧化与被还原的氮原子数之比为
(2)某硝酸盐受热分解的产物为不含氮元素的固体物质和NO2、O2气体,若产生NO2和O2的物质的量之比为8︰1,则金属元素的价态在反应过程中
(3)2mol Cu(NO3)2和AgNO3混合物,加热使其分解,得到NO2、O2二种气体和CuO、Ag二种固体,将产生的NO2、O2混合气体经水充分吸收后,剩余气体是
您最近一年使用:0次
【推荐2】已知:①Fe+H2SO4(稀)=FeSO4+H2↑
②Cu+2H2SO4(浓) CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑
③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
请回答下列问题:
(1)当反应①转移3摩尔电子时,消耗H2SO4的质量是______ g,产生氢气的体积(标准状况)_________ L。
(2)反应②中_________ 作氧化剂,___________ 是氧化产物。
(3)当反应②中生成11.2LSO2气体(标准状况下)时,被还原的H2SO4的物质的量是____________ 。
(4)用单线桥法表示反应③电子转移的方向和数目。KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
______________
(5)反应③中盐酸表现_________________ 性。
②Cu+2H2SO4(浓)
 CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
请回答下列问题:
(1)当反应①转移3摩尔电子时,消耗H2SO4的质量是
(2)反应②中
(3)当反应②中生成11.2LSO2气体(标准状况下)时,被还原的H2SO4的物质的量是
(4)用单线桥法表示反应③电子转移的方向和数目。KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
(5)反应③中盐酸表现
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】酸性条件下,许多氧化剂可使KI溶液中的I-氧化,例如KIO3(IO3-→I2)、H2O2(H2O2→H2O)、FeCl3(Fe3+→Fe2+)、K2Cr2O7(Cr2O72-→Cr3+).请根据题目要求填空:
(1)写出在醋酸存在的条件下KIO3溶液与KI溶液反应的离子方程式______________ 。
(2)在酸性条件下(足量),各取1L浓度为1mol•L-1的KI溶液分别与上述列举四种溶液进行完全反应,则需要溶质的物质的量之比为n(KIO3):n(H2O2):n(FeCl3):n(K2Cr2O7)=______________________ (要求写出最简比)
(1)写出在醋酸存在的条件下KIO3溶液与KI溶液反应的离子方程式
(2)在酸性条件下(足量),各取1L浓度为1mol•L-1的KI溶液分别与上述列举四种溶液进行完全反应,则需要溶质的物质的量之比为n(KIO3):n(H2O2):n(FeCl3):n(K2Cr2O7)=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将15.6g表面已被氧化的铝片投入300mL的稀硫酸中,恰好完全反应,产生标准状况下H2的体积为6.72L。计算下列问题并写出过程。
(1)铝片中Al和Al2O3的物质的量______ ;
(2)稀硫酸的物质的量浓度______ ;
(3)若该稀硫酸用18.0mol/L的浓硫酸配制,求所需浓硫酸的体积为______ ?
(1)铝片中Al和Al2O3的物质的量
(2)稀硫酸的物质的量浓度
(3)若该稀硫酸用18.0mol/L的浓硫酸配制,求所需浓硫酸的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】一定量氢气在氯气中燃烧,所得混合气体用480mL0.1mol/LNaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量浓度为0.03mol/L(假设溶液体积不变)。
(1)实验室需480mL0.1mol/LNaOH溶液,若用固体NaOH配制,下列说法正确的是_______。
(2)所得溶液中NaCl的物质的量浓度为_______ mol/L;
(3)参加反应的H2的质量为_______ g。
(1)实验室需480mL0.1mol/LNaOH溶液,若用固体NaOH配制,下列说法正确的是_______。
| A.配制此溶液需要1.92g固体NaOH |
| B.将固体NaOH放在垫有滤纸托盘上进行称量 |
| C.定容时仰视刻度线会导致所配溶液浓度偏低 |
| D.用容量瓶配制溶液,定容时若加水超过刻度线,应立即用滴管吸出多余液体 |
(3)参加反应的H2的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)19 g某二价金属氯化物(ACl2)中含有0.4 molCl−,则ACl2的摩尔质量是____ g/mol;ACl2的化学式是_____ 。
(2)配制480 mL 0.1mol/L的硫酸铜溶液,需用托盘天平称取CuSO4·5H2O____ g;在配制过程中,若其它操作均正确,则下列操作会使所配溶液物质的量浓度偏低的是_________ (填字母序号)。
A.溶解后小烧杯、玻璃棒没有洗涤
B.所用容量瓶中,已有少量蒸馏水
C.定容、加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线
D.定容时俯视刻度线
(3)将适量铁粉加到三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是______ 。
(1)19 g某二价金属氯化物(ACl2)中含有0.4 molCl−,则ACl2的摩尔质量是
(2)配制480 mL 0.1mol/L的硫酸铜溶液,需用托盘天平称取CuSO4·5H2O
A.溶解后小烧杯、玻璃棒没有洗涤
B.所用容量瓶中,已有少量蒸馏水
C.定容、加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线
D.定容时俯视刻度线
(3)将适量铁粉加到三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】合金的性能往往优于组成金属,因而用途非常广泛。钠钾合金可在核反应堆中用作导热剂。5.05g钠钾合金溶于200mL水生成0.075mol氢气。
1.计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
2.计算并确定该钠-钾合金的化学式。
镁铝合金广泛用于火箭、导弹和飞机制造业等。取不同质量的镁铝合金样品分别和30mL相同浓度的盐酸反应,所取合金质量与产生气体体积(标况下)如下表所示:
3.计算镁铝合金中镁铝的质量之比。
铜锡合金,又称青铜,是人类使用最早的合金。不同的铜锡比例可以产生不同的效用,若含锡量为1/4—1/7(质量比)的青铜被称作重青铜,受敲击时能发出洪亮的声音。
4.现有一铜锡合金样品,可通过至少增加ag铜或至少减少bg锡恰好使其成为钟青铜,且最终得到的钟青铜质量正好相差一半。求原铜锡合金样品中铜锡的物质的量之比。
1.计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
2.计算并确定该钠-钾合金的化学式。
镁铝合金广泛用于火箭、导弹和飞机制造业等。取不同质量的镁铝合金样品分别和30mL相同浓度的盐酸反应,所取合金质量与产生气体体积(标况下)如下表所示:
| 实验序号 | A | B | C |
| 合金质量/mg | 510 | 765 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
3.计算镁铝合金中镁铝的质量之比。
铜锡合金,又称青铜,是人类使用最早的合金。不同的铜锡比例可以产生不同的效用,若含锡量为1/4—1/7(质量比)的青铜被称作重青铜,受敲击时能发出洪亮的声音。
4.现有一铜锡合金样品,可通过至少增加ag铜或至少减少bg锡恰好使其成为钟青铜,且最终得到的钟青铜质量正好相差一半。求原铜锡合金样品中铜锡的物质的量之比。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某纯净的天然碱可看做二氧化碳和氢氧化钠反应的产物。取6.64g天然碱用酒精灯充分加热至恒重,将生成的气体依次通过过量的浓硫酸、过量澄清石灰水后,浓硫酸增重0.9g,澄清石灰水中生成沉淀1g。
(1)充分加热后,剩余固体重______ g;
(2)该天然碱成分中除含有碳酸钠外,还含有_________ (填化学式);
(3)6.64g天然碱中,含碳酸钠的物质的量为_________ mol;
(4)该天然碱的化学式为______________ 。
(1)充分加热后,剩余固体重
(2)该天然碱成分中除含有碳酸钠外,还含有
(3)6.64g天然碱中,含碳酸钠的物质的量为
(4)该天然碱的化学式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】I.将200mLH2SO4 和Fe2(SO4)3的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少4.48g;向另一份中加入足量BaCl2溶液,经过滤、洗涤、干 燥、称量,得到46.6g 白色沉淀。则:
(1)原溶液中c( )=
)=_______ ;
(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为_______ 。
(3)实验室中的FeSO4溶液常因氧化而变质。除杂的方法是______________________ ,检验是否变质的方法是_______
II.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4 g,则这种铁的氧化物为_______
(1)原溶液中c(
 )=
)=(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为
(3)实验室中的FeSO4溶液常因氧化而变质。除杂的方法是
II.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4 g,则这种铁的氧化物为
您最近一年使用:0次

 。
。

