氢氧化镁:①是中强碱;②广泛用作阻燃剂和填充剂.以白云石(化学式:MgCO3•CaCO3)为原料制备氢氧化镁的工艺流程如下:

(1)根据流程图,白云石“轻烧”后固体产物的主要成分是MgO和_______ (写化学式)。
(2)流程图中“加热反应”有氨气生成的化学方程式为_________________________ 。
(3)洗涤Mg(OH)2沉淀所用玻璃仪器有:_______ 、烧杯、玻璃棒;检验洗净的方法是____________ 。
(4)传统工艺是将白云石高温分解为氧化镁和氧化钙后提取,而该工艺采用轻烧白云石的方法,其优点是__________________ 。
(5)25℃时Mg(OH)2饱和溶液的中:c(Mg2+)=2.80×10﹣4mol/L,Mg(O2)22﹣、Mg(OH)42﹣的浓度共为2.35×10﹣4mol/L,则溶液的pH=_______ (取整数值);若经过循环利用,每制得5.8t Mg(OH)2时排出200m3的废水,其中Mg2+、Mg(O2)22﹣、Mg(OH)42﹣的浓度共为1.50×10﹣4mol/L,则该工艺的产率为___________ (保留4位小数)。

(1)根据流程图,白云石“轻烧”后固体产物的主要成分是MgO和
(2)流程图中“加热反应”有氨气生成的化学方程式为
(3)洗涤Mg(OH)2沉淀所用玻璃仪器有:
(4)传统工艺是将白云石高温分解为氧化镁和氧化钙后提取,而该工艺采用轻烧白云石的方法,其优点是
(5)25℃时Mg(OH)2饱和溶液的中:c(Mg2+)=2.80×10﹣4mol/L,Mg(O2)22﹣、Mg(OH)42﹣的浓度共为2.35×10﹣4mol/L,则溶液的pH=
2015·上海静安·二模 查看更多[1]
更新时间:2020-03-24 20:29:30
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:
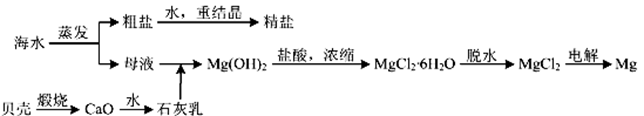
(1)在实验室中由粗盐“重结晶”的操作包括溶解、过滤、蒸发、_________ (填操作方法)、洗涤等步骤;有关其中“蒸发”步骤的叙述错误的是____________ 。
a. 蒸发的目的是得到热饱和溶液 b. 蒸发的目的是析出晶体
c. 应用余热蒸干溶液 d. 应蒸发至有较多晶体析出时为止
(2)由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶解度曲线,蒸发的目的是_________ 。
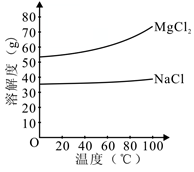
a. 得到热饱和溶液 b. 析出晶体
(3)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,写出反应的化学方程式:__________ 。
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是_____________________________________ 。
(5)MgCl2可电解制Mg,MgO则是重要的耐火材料。在550℃时,MgCl2·6H2O会分解生成MgO、MgCl2、HCl和H2O,若不补充其它原料,使一定量的MgCl2·6H2O全部生成a mol MgO、b mol MgCl2和36.5%的盐酸,则a∶b为______________ (取整数值)。

(1)在实验室中由粗盐“重结晶”的操作包括溶解、过滤、蒸发、
a. 蒸发的目的是得到热饱和溶液 b. 蒸发的目的是析出晶体
c. 应用余热蒸干溶液 d. 应蒸发至有较多晶体析出时为止
(2)由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶解度曲线,蒸发的目的是

a. 得到热饱和溶液 b. 析出晶体
(3)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,写出反应的化学方程式:
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是
(5)MgCl2可电解制Mg,MgO则是重要的耐火材料。在550℃时,MgCl2·6H2O会分解生成MgO、MgCl2、HCl和H2O,若不补充其它原料,使一定量的MgCl2·6H2O全部生成a mol MgO、b mol MgCl2和36.5%的盐酸,则a∶b为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】碳酸锶(SrCO3)难溶于水,主要用于电磁材料和金属冶炼。一种由工业碳酸锶(含少量Ba2+、Ca2+、Mg2+、 Pb2+等)制备高纯碳酸锶的工艺流程如下:
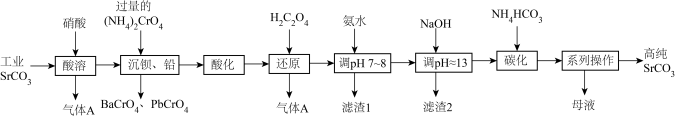
已知:
I. Cr(OH)3为两性氢氧化物;
II.常温下,各物质的溶度积常数如下表所示。
回答下列问题:
(1)气体A的电子式为_______ 。
(2)“除钡、铅”时,pH过低会导致(NH4)2CrO4的利用率降低,原因为_______ (用离子方程式解释);“还原”时含铬微粒发生反应的离子方程式为_______ 。
(3)“滤渣1”的主要成分为_______ (填化学式)。
(4)用氨水和NaOH分步调节pH,而不是直接调节溶液的pH≈13的原因为_______ 。
(5)“调pH ≈13”后需对溶液进行煮沸并趁热过滤出滤渣2,煮沸并趁热过滤的原因为_______ 。
(6)“系列操作”中包含“200℃烘干”操作,烘干过程中除蒸发水分外,还能够除去SrCO3中的微量可溶性杂质,该杂质除NH4HCO3外还可能为_______ (填化学式)。

已知:
I. Cr(OH)3为两性氢氧化物;
II.常温下,各物质的溶度积常数如下表所示。
| 化合物 | Cr(OH)3 | Ca(OH)2 | Mg(OH)2 | SrCO3 |
| Ksp近似值 | 1×10-31 | 5.5×10-6 | 1.8×10-11 | 5.6×10-10 |
(1)气体A的电子式为
(2)“除钡、铅”时,pH过低会导致(NH4)2CrO4的利用率降低,原因为
(3)“滤渣1”的主要成分为
(4)用氨水和NaOH分步调节pH,而不是直接调节溶液的pH≈13的原因为
(5)“调pH ≈13”后需对溶液进行煮沸并趁热过滤出滤渣2,煮沸并趁热过滤的原因为
(6)“系列操作”中包含“200℃烘干”操作,烘干过程中除蒸发水分外,还能够除去SrCO3中的微量可溶性杂质,该杂质除NH4HCO3外还可能为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.完成下列问题
(1)下列氯化物中,既能由金属与氯气直接化合得到,也能由金属与盐酸反应制得_______
(2)用化学方法鉴别氯化氢和氯气,不能选用的是_______
(3)能一次性鉴别AgNO3、Na2CO3、NaCl三种溶液的试剂是_______
(4)下列关于含氯消毒剂的解释正确的是_______
(5)下列物质能使干燥的蓝色石蕊试纸变红又褪色的是_______
(1)氯气(2)液氯(3)新制氯水(4)盐酸(5)氯化氢气体(6)盐酸酸化的漂粉精溶液
(6)某小组用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是_______
Ⅱ.某同学设计如下方案从粗食盐水中除去Ca2+、Mg2+、SO 等离子,以制得精盐水。并进行电解饱和食盐水的实验:
等离子,以制得精盐水。并进行电解饱和食盐水的实验:

(7)以下说法不正确的是_______
(8)电解饱和食盐水装置如图所示,其总反应的化学方程式为___________ 。
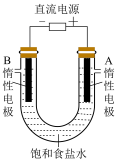
(9)向两极附近各加入酚酞溶液,___________ 极(填“A”或“B”)附近溶液变红色。A是___________ 极,检验该极产物的实验方法是___________ (必须有所用试剂或药品、现象和对应的结论)。
(1)下列氯化物中,既能由金属与氯气直接化合得到,也能由金属与盐酸反应制得_______
| A.FeCl3 | B.FeCl2 | C.CuCl2 | D.ZnCl2 |
(2)用化学方法鉴别氯化氢和氯气,不能选用的是_______
| A.湿润蓝色石蕊试纸 | B.湿润红色石蕊试纸 |
| C.湿润的淀粉KI试纸 | D.硝酸银溶液 |
(3)能一次性鉴别AgNO3、Na2CO3、NaCl三种溶液的试剂是_______
| A.盐酸 | B.NaOH溶液 | C.BaCl2溶液 | D.KNO3溶液 |
(4)下列关于含氯消毒剂的解释正确的是_______
| A.室温下,氯气通入NaOH溶液中制得漂白液:Cl2+OH-=Cl-+ClO-+H2O |
| B.氯水具有杀菌消毒作用:Cl2+H2O=HCl+HClO |
C.氯水应避光保存的原因是:2HClO H2O+Cl2↑ H2O+Cl2↑ |
| D.向Ca(ClO)2溶液中通入适量CO2可增强漂白效果:Ca(ClO)2+CO2+H2O=CaCO3+2HClO |
(5)下列物质能使干燥的蓝色石蕊试纸变红又褪色的是_______
(1)氯气(2)液氯(3)新制氯水(4)盐酸(5)氯化氢气体(6)盐酸酸化的漂粉精溶液
| A.(1)(2)(3) | B.(1)(2)(3)(6) |
| C.(3)(6) | D.(3)(4)(6) |
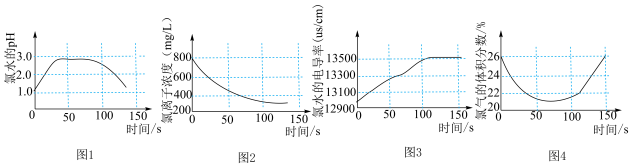
(6)某小组用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是_______

| A.图1表示氯水pH随时间的变化 |
| B.图2表示溶液中氯离子浓度随时间的变化 |
| C.图3表示氯水的电导率随时的变化 |
| D.图4表示液面上方氧气体积分数随时间的变化 |
Ⅱ.某同学设计如下方案从粗食盐水中除去Ca2+、Mg2+、SO
 等离子,以制得精盐水。并进行电解饱和食盐水的实验:
等离子,以制得精盐水。并进行电解饱和食盐水的实验:
(7)以下说法不正确的是_______
| A.E中主要有Mg(OH)2和BaSO4,也可能有一些Ca(OH)2 |
| B.②中加入过量Na2CO3溶液的主要目的是为了除去Ca2+ |
| C.N溶液呈碱性 |
D.③目的是除去CO 和OH- 和OH- |
(8)电解饱和食盐水装置如图所示,其总反应的化学方程式为

(9)向两极附近各加入酚酞溶液,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】NaNO3是重要的化工原料,可通过下列方法制备:
第一步:在吸收塔中,将硝酸生产中排出的尾气(体积分数:含0.5% NO、1.5% NO2)用纯碱溶液完全吸收,得到NaNO2、NaNO3和Na2CO3的混合液及CO2气体。
第二步:将吸收塔中的混合液送入转化塔中,加入50%HNO3溶液,同时通入足量的压缩空气搅拌,充分反应,得到 NaNO3和硝酸的混合液。
第三步:将转化塔中的混合液用纯碱中和后,经蒸发浓缩、冷却结晶、离心分离、干燥,得NaNO3成品。
已知:每生产1.0 t纯净的NaNO3固体,需消耗0.65 t无水Na2CO3、消耗氧气的体积为33.6 m3(标准状况下)和一定量的HNO3.生产过程中排出的尾气中均不含氮氧化物。
回答下列问题:
(1)第一步生产过程中发生反应的总化学方程式是_______ 。
(2)检验NaNO3成品中是否含少量的Na2CO3杂质的方法是_______ 。
(3)生产过程中Na2CO3的利用率是_______ (计算结果精确到小数点后两位)。
(4)生产1.0 t纯净的NaNO3固体,可以处理硝酸生产中排出的尾气的体积至少为_______ m3
(标准状况下)。
第一步:在吸收塔中,将硝酸生产中排出的尾气(体积分数:含0.5% NO、1.5% NO2)用纯碱溶液完全吸收,得到NaNO2、NaNO3和Na2CO3的混合液及CO2气体。
第二步:将吸收塔中的混合液送入转化塔中,加入50%HNO3溶液,同时通入足量的压缩空气搅拌,充分反应,得到 NaNO3和硝酸的混合液。
第三步:将转化塔中的混合液用纯碱中和后,经蒸发浓缩、冷却结晶、离心分离、干燥,得NaNO3成品。
已知:每生产1.0 t纯净的NaNO3固体,需消耗0.65 t无水Na2CO3、消耗氧气的体积为33.6 m3(标准状况下)和一定量的HNO3.生产过程中排出的尾气中均不含氮氧化物。
回答下列问题:
(1)第一步生产过程中发生反应的总化学方程式是
(2)检验NaNO3成品中是否含少量的Na2CO3杂质的方法是
(3)生产过程中Na2CO3的利用率是
(4)生产1.0 t纯净的NaNO3固体,可以处理硝酸生产中排出的尾气的体积至少为
(标准状况下)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】由难溶性磷酸锂渣(主要成分为Li3PO4)为原料制备电池级Li2CO3的流程如下:

已知:①Li2CO3在不同温度下的溶解度: 0℃ 1.54g,20℃ 1.33g, 90℃ 0.78g。
②碳酸锂:水溶液煮沸时容易发生水解。
(1)溶解除磷。将一定量磷酸锂渣与CaCl2溶液、盐酸中的一种配成悬浊液,加入到三颈烧瓶中(装置如图),一段时间后,通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤,得到LiCl溶液。
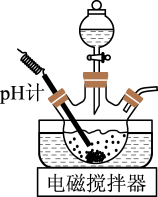
①滴液漏斗中的液体是_______ 。
②Li3PO4转化为LiCl和CaHPO4的离子方程式为_______ 。
(2)除钙。通过离子交换法除去溶液中Ca2+。若要使后续得到的Li2CO3 中不含CaCO3(设沉淀后溶液中Li+浓度为0.1 mol·L-1),需控制除钙后溶液中c(Ca2+)≤_______ 。[Ksp(Li2CO3)=2.5×10-2,Ksp(CaCO3)=2.8×10-9]
(3)制备Li2CO3。向除杂后的LiCl溶液中加入N235萃取剂(50%三辛癸烷基叔胺与50% ,异辛醇的混合液),边搅拌边向混合液中通CO2,过滤洗涤得到Li2CO3。
①方法能制得Li2CO3的原因是_______ 。
②检验滤渣是否洗涤完全的实验方法是_______ 。
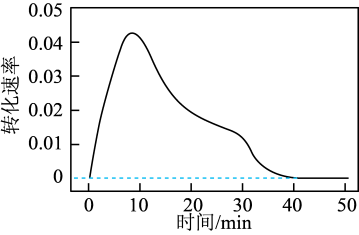
(4)若粗品碳酸锂中含少量难溶性杂质,为获得较高产率的纯Li2CO3,请补充完整实验 方案:向粗品Li2CO3中加水,按一定速率通入CO2,边通边搅拌,_______ 。(已知:①LiHCO3受热易分解;②实验过程中Li2CO3转化速率与时间的关系图如图所示。)

已知:①Li2CO3在不同温度下的溶解度: 0℃ 1.54g,20℃ 1.33g, 90℃ 0.78g。
②碳酸锂:水溶液煮沸时容易发生水解。
(1)溶解除磷。将一定量磷酸锂渣与CaCl2溶液、盐酸中的一种配成悬浊液,加入到三颈烧瓶中(装置如图),一段时间后,通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤,得到LiCl溶液。

①滴液漏斗中的液体是
②Li3PO4转化为LiCl和CaHPO4的离子方程式为
(2)除钙。通过离子交换法除去溶液中Ca2+。若要使后续得到的Li2CO3 中不含CaCO3(设沉淀后溶液中Li+浓度为0.1 mol·L-1),需控制除钙后溶液中c(Ca2+)≤
(3)制备Li2CO3。向除杂后的LiCl溶液中加入N235萃取剂(50%三辛癸烷基叔胺与50% ,异辛醇的混合液),边搅拌边向混合液中通CO2,过滤洗涤得到Li2CO3。
①方法能制得Li2CO3的原因是
②检验滤渣是否洗涤完全的实验方法是
(4)若粗品碳酸锂中含少量难溶性杂质,为获得较高产率的纯Li2CO3,请补充完整实验 方案:向粗品Li2CO3中加水,按一定速率通入CO2,边通边搅拌,

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】高锰酸钾是强氧化剂,它的用途遍布各个行业。
(1) 工业上由软锰矿(主要成分为MnO2)生产高锰酸钾分为两个步骤:
①步骤一将软锰矿与过量的固体KOH和空气在高温下反应,生成锰酸钾(K2MnO4), 该反应的化学方程式是___________________________________________________ 。
②步骤二以石墨为阳极,铁为阴极,电解锰酸钾(K2MnO4)溶液,在_______ (填“阴极区”或“阳极区”)得到高锰酸钾。阴极反应的化学方程式是____________________________ 。
(2) 某研究小组用工业生产高锰酸钾产生的废渣——锰泥(含K2MnO4、MnO2及Pb、Ca等元素)和轧钢废酸液制取工业级碳酸锰(MnCO3),其流程如下:

①轧钢废酸中Fe2+的作用是_____________________________________________ 。
②操作I、操作Ⅱ、操作Ⅲ的名称是_______________ ,
用到的玻璃仪器有_______________________________________________________ 。
③溶液C中除含有Ca2+、Mn2+、H+外,还含有的阳离子是___________________ 。
(1) 工业上由软锰矿(主要成分为MnO2)生产高锰酸钾分为两个步骤:
①步骤一将软锰矿与过量的固体KOH和空气在高温下反应,生成锰酸钾(K2MnO4), 该反应的化学方程式是
②步骤二以石墨为阳极,铁为阴极,电解锰酸钾(K2MnO4)溶液,在
(2) 某研究小组用工业生产高锰酸钾产生的废渣——锰泥(含K2MnO4、MnO2及Pb、Ca等元素)和轧钢废酸液制取工业级碳酸锰(MnCO3),其流程如下:

①轧钢废酸中Fe2+的作用是
②操作I、操作Ⅱ、操作Ⅲ的名称是
用到的玻璃仪器有
③溶液C中除含有Ca2+、Mn2+、H+外,还含有的阳离子是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】乙二酸( )俗名草酸,是一种有还原性的有机弱酸,在化学上有广泛应用。实验室有一瓶混有泥沙的乙二酸样品,用
)俗名草酸,是一种有还原性的有机弱酸,在化学上有广泛应用。实验室有一瓶混有泥沙的乙二酸样品,用
 溶液测定泥沙的乙二酸的含量。原理为:
溶液测定泥沙的乙二酸的含量。原理为: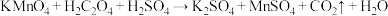 (未配平),具体操作为:
(未配平),具体操作为:
(1)配制250mL溶液:准确称量5.000g乙二酸样品,配成250mL溶液。滴定:准确量取25.00mL所配溶液于锥形瓶中,加少量硫酸酸化,将
 标准溶液装入
标准溶液装入___________ (填“酸式”或“碱式”)滴定管,进行滴定操作。
(2)在滴定过程中发现,刚滴下少量 标准溶液时,溶液紫红色并没有马上褪去。将锥形瓶摇动一段时间后,紫红色才慢慢消失;再继续滴加时,紫红色就很快褪去,可能的原因是
标准溶液时,溶液紫红色并没有马上褪去。将锥形瓶摇动一段时间后,紫红色才慢慢消失;再继续滴加时,紫红色就很快褪去,可能的原因是___________ ;判断滴定达到终点的现象是___________ 。
(3)计算:重复上述操作2次,记录实验数据如下表,此样品的纯度为___________ 。
(4)误差分析:下列操作会导致测定结果偏高的是___________。
 )俗名草酸,是一种有还原性的有机弱酸,在化学上有广泛应用。实验室有一瓶混有泥沙的乙二酸样品,用
)俗名草酸,是一种有还原性的有机弱酸,在化学上有广泛应用。实验室有一瓶混有泥沙的乙二酸样品,用
 溶液测定泥沙的乙二酸的含量。原理为:
溶液测定泥沙的乙二酸的含量。原理为: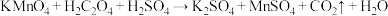 (未配平),具体操作为:
(未配平),具体操作为:(1)配制250mL溶液:准确称量5.000g乙二酸样品,配成250mL溶液。滴定:准确量取25.00mL所配溶液于锥形瓶中,加少量硫酸酸化,将

 标准溶液装入
标准溶液装入(2)在滴定过程中发现,刚滴下少量
 标准溶液时,溶液紫红色并没有马上褪去。将锥形瓶摇动一段时间后,紫红色才慢慢消失;再继续滴加时,紫红色就很快褪去,可能的原因是
标准溶液时,溶液紫红色并没有马上褪去。将锥形瓶摇动一段时间后,紫红色才慢慢消失;再继续滴加时,紫红色就很快褪去,可能的原因是(3)计算:重复上述操作2次,记录实验数据如下表,此样品的纯度为
| 序号 | 滴定前读数 | 滴定后读数 |
| 1 | 1.50 | 23.70 |
| 2 | 1.02 | 21.03 |
| 3 | 2.00 | 21.99 |
A.未用 待测溶液润洗滴定管 待测溶液润洗滴定管 |
B.锥形瓶水洗后,用 溶液润洗 溶液润洗 |
C.盛放 标准溶液的滴定管,滴定前尖嘴部分有气泡,滴定后气泡消失 标准溶液的滴定管,滴定前尖嘴部分有气泡,滴定后气泡消失 |
D.读取 溶液体积时,滴定前平视,滴定结束后俯视读数 溶液体积时,滴定前平视,滴定结束后俯视读数 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】铝氢化钠(NaAlH4)是有机合成的重要还原剂,其合成线路如下图所示:
(1)制备无水AlCl3实验装置如下,已知AlCl3易升华(178℃),在潮湿空气中易水解。
实验时应先点燃________ (填“A”或“D”)处酒精灯。装置F的作用是________________________ 。
(2)制取铝氢化钠的化学方程式是___________________________________ 。
(3)铝氢化钠样品性质探究和纯度测定。已知铝氢化钠样品中仅含有少量杂质NaH,NaH也会与水反应。
①铝氢化钠与水反应的化学方程式为__________________ ;
②取少量上述样品,滴加足量的水,向反应后的溶液中逐滴滴加盐酸并振荡,直至盐酸过量。滴加盐酸过程中可观察到的现象是__________________ 。
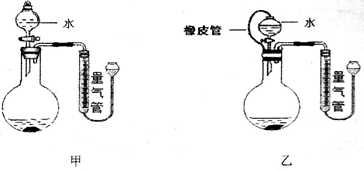
③称取1.56g上述样品与水完全反应后,测得气体在标准状况下的体积为2240mL,样品中铝氢化钠的质量分数为_________ %(结果保留两位有效数字)。若实验室用如下两种装置分别测定生成气体的体积(其他操作一致),用甲装置测得铝氢化钠的含量________________ 乙装置。(填“大于”、“小于”或“等于”)。

(1)制备无水AlCl3实验装置如下,已知AlCl3易升华(178℃),在潮湿空气中易水解。

实验时应先点燃
(2)制取铝氢化钠的化学方程式是
(3)铝氢化钠样品性质探究和纯度测定。已知铝氢化钠样品中仅含有少量杂质NaH,NaH也会与水反应。
①铝氢化钠与水反应的化学方程式为
②取少量上述样品,滴加足量的水,向反应后的溶液中逐滴滴加盐酸并振荡,直至盐酸过量。滴加盐酸过程中可观察到的现象是
③称取1.56g上述样品与水完全反应后,测得气体在标准状况下的体积为2240mL,样品中铝氢化钠的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验.
方案Ⅰ.甲组同学用质量法,按如下图所示的实验流程进行实验:

(1)实验时,蒸发结晶操作中,除了酒精灯外,还要用到的仪器是_______
(2)有同学认为“加入适量盐酸”不好操控,应改为“过量盐酸”,便于操作且不影响测定的准确性,你认为对或错_______ ,为什么___________________
(3)若实验中测得样品质量为46.4g,固体质量为40.95g,则碳酸钠的质量分数为_______ .(保留3位有效数字)
(4)蒸发结晶过程中若有固体飞溅,测得碳酸钠的质量分数____________ (填偏大 偏小 无影响).
方案Ⅱ:乙组同学的主要实验流程图如下:
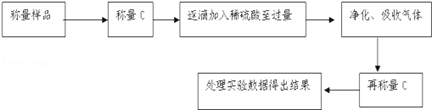
按如下图所示装置进行实验:
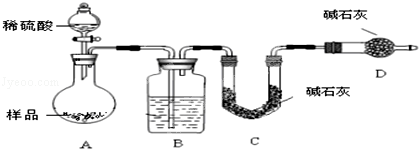
(5)在C中装碱石灰来吸收净化后的气体.D装置的作用是_____________________ .
(6)有的同学认为为了减少实验误差,在反应前后都通入N2,反应后通入N2的目的是______________________________ .
方案Ⅲ:气体分析法
(7)把一定量样品与足量稀硫酸反应后,用如图装置测量产生CO2气体的体积,B溶液最好采用_________ (以下选项中选择)使测量误差较小.

方案Ⅰ.甲组同学用质量法,按如下图所示的实验流程进行实验:

(1)实验时,蒸发结晶操作中,除了酒精灯外,还要用到的仪器是
(2)有同学认为“加入适量盐酸”不好操控,应改为“过量盐酸”,便于操作且不影响测定的准确性,你认为对或错
(3)若实验中测得样品质量为46.4g,固体质量为40.95g,则碳酸钠的质量分数为
(4)蒸发结晶过程中若有固体飞溅,测得碳酸钠的质量分数
方案Ⅱ:乙组同学的主要实验流程图如下:

按如下图所示装置进行实验:

(5)在C中装碱石灰来吸收净化后的气体.D装置的作用是
(6)有的同学认为为了减少实验误差,在反应前后都通入N2,反应后通入N2的目的是
方案Ⅲ:气体分析法
(7)把一定量样品与足量稀硫酸反应后,用如图装置测量产生CO2气体的体积,B溶液最好采用

| A.饱和碳酸钠溶液 | B.饱和碳酸氢钠溶液 |
| C.饱和氢氧化钠溶液 | D.饱和硫酸铜溶液 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】钛被誉为“21世纪的金属”,在工农业生产、医疗、国防、科技等方面中有着极其广泛而重要的用途。四氯化钛是工业上制备金属钛的重要原料。在常温下,它是一种极易水解的无色液体,沸点为136.4℃。工业制备TiCl4的反应原理为:TiO2+2C+2Cl2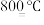 TiCl4+2CO。
TiCl4+2CO。
下图是实验室模拟工业生产制备四氯化钛的反应装置,其主要操作步骤有(顺序已打乱):
①连接好整套装置,并检查装置的气密性;
②当锥形瓶中的TiCl4的量不再增加时,停止加热,改通CO2气体直至电炉中的瓷管冷却为止;
③将TiO2、炭粉混合均匀后,装入管式电炉中;
④将电炉升温至800℃,一段时间后改通Cl2,同时在冷凝管中通冷凝水;
⑤通入干燥的CO2气体并持续一段时间。

试回答:
(1)仪器F的名称是_______________ ,装置A所用的试剂名称是_______________ 。
(2)正确的操作程序是(填写操作步骤的序号)________________________ 。
(3)操作⑤的目的是________________________ 。
(4)装置中冷凝管进水口的位置是(填a或b)_______________ ,装置E的作用_______________ 。
(5)将少量TiCl4露置于空气中,可能看到的现象是________________________ 。
(6)利用化合物TiCl4可制备TiO2,请结合化学用语解释该过程:_______________ 。
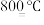 TiCl4+2CO。
TiCl4+2CO。下图是实验室模拟工业生产制备四氯化钛的反应装置,其主要操作步骤有(顺序已打乱):
①连接好整套装置,并检查装置的气密性;
②当锥形瓶中的TiCl4的量不再增加时,停止加热,改通CO2气体直至电炉中的瓷管冷却为止;
③将TiO2、炭粉混合均匀后,装入管式电炉中;
④将电炉升温至800℃,一段时间后改通Cl2,同时在冷凝管中通冷凝水;
⑤通入干燥的CO2气体并持续一段时间。

试回答:
(1)仪器F的名称是
(2)正确的操作程序是(填写操作步骤的序号)
(3)操作⑤的目的是
(4)装置中冷凝管进水口的位置是(填a或b)
(5)将少量TiCl4露置于空气中,可能看到的现象是
(6)利用化合物TiCl4可制备TiO2,请结合化学用语解释该过程:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学小组采用类似制乙酸乙酯的装置用环己醇制备环己烯,装置如图1所示。
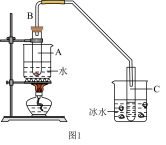
已知: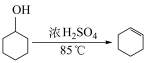 +H2O。
+H2O。
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①试管A中碎瓷片的作用是___ ,导管B除了导气外还具有的作用是__ 。
②将试管C置于冰水中的目的是__ 。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在___ (填“上”或“下”)层,分液后用___ (填字母)洗涤。
a.酸性KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
②再将提纯后的环己烯按如图2所示装置进行蒸馏,冷却水从__ (填字母)口进入,目的是___ 。蒸馏时要加入生石灰,目的是___ 。
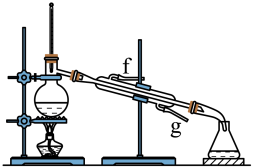
③收集产品时,应控制温度在___ 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是___ (填字母)。
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗产品时环己醇随产品一起蒸出
(3)以下用来区分环己烯精品和粗品的试剂或方法中,合理的是__ (填字母)。
a.酸性高锰酸钾溶液 b.金属钠 c.测定沸点

已知:
 +H2O。
+H2O。| 密度/ g·cm-3 | 熔点/℃ | 沸点/℃ | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①试管A中碎瓷片的作用是
②将试管C置于冰水中的目的是
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
a.酸性KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
②再将提纯后的环己烯按如图2所示装置进行蒸馏,冷却水从

③收集产品时,应控制温度在
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗产品时环己醇随产品一起蒸出
(3)以下用来区分环己烯精品和粗品的试剂或方法中,合理的是
a.酸性高锰酸钾溶液 b.金属钠 c.测定沸点
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】光气(COCl2)是一种重要的有机中间体,无色剧毒,易水解生成两种酸性物质。实验室常用CCl4与发烟硫酸反应制备光气,化学方程式为CCl4+SO3+H2SO4=COCl2↑+2ClSO3H。装置如图所示(夹持及加热仪器略去):

已知:光气的熔点-127.84℃,沸点7.94℃;CCl4沸点76.8℃;ClSO3H沸点151℃。
回答下列问题:
(1)A装置中冷凝管进水口为___________ (填“a”或“b”),仪器甲的名称是___________ 。
(2)A装置加热的温度不宜超过76.8℃的原因是___________ 。
(3)D装置中可观察到的现象是___________ 。
(4)E装置的作用是___________ 。
(5)F装置用于吸收多余的光气,反应的离子方程式为___________ 。
(6)光气纯度测定:用注射器抽取光气注入m1g装有氢氧化钠溶液的密封碘量瓶中,称得碘量瓶为m2g,充分反应后用硝酸调节pH至6.5,加入少量K2CrO4作指示剂,用c mol/L硝酸银标准液滴定至终点,消耗硝酸银标准液V mL。(已知Ag2CrO4为砖红色沉淀)
①滴定终点的现象是___________ 。
②光气的纯度是___________ 。

已知:光气的熔点-127.84℃,沸点7.94℃;CCl4沸点76.8℃;ClSO3H沸点151℃。
回答下列问题:
(1)A装置中冷凝管进水口为
(2)A装置加热的温度不宜超过76.8℃的原因是
(3)D装置中可观察到的现象是
(4)E装置的作用是
(5)F装置用于吸收多余的光气,反应的离子方程式为
(6)光气纯度测定:用注射器抽取光气注入m1g装有氢氧化钠溶液的密封碘量瓶中,称得碘量瓶为m2g,充分反应后用硝酸调节pH至6.5,加入少量K2CrO4作指示剂,用c mol/L硝酸银标准液滴定至终点,消耗硝酸银标准液V mL。(已知Ag2CrO4为砖红色沉淀)
①滴定终点的现象是
②光气的纯度是
您最近一年使用:0次



