解题方法
1 . 小芳从一瓶未知浓度的过氧化氢溶液中倒出107克,再加入8.7克的二氧化锰固体,完全反应后共生成氧气的质量为8克。试计算:
(1)计算107克过氧化氢溶液中含有过氧化氢多少克。
(2)计算反应后剩余物中氧元素的质量分数(保留1位小数点)。
(1)计算107克过氧化氢溶液中含有过氧化氢多少克。
(2)计算反应后剩余物中氧元素的质量分数(保留1位小数点)。
您最近一年使用:0次
2 . 我国的酒文化源远流长,但现实生活中因饮用劣质酒引发的中毒事件时有发生,原因是劣质酒中的甲醇(化学式为( )含量严重超标。甲醇易引起视神经萎缩、甚至导致双目失明。请回答下列问题:
)含量严重超标。甲醇易引起视神经萎缩、甚至导致双目失明。请回答下列问题:
(1)甲醇中 、
、 、
、 三种元素的质量比是
三种元素的质量比是______ 。
(2)甲醇中氧元素的质量分数是______ 。
(3)交通安全人人有责,为了严禁醉驾,交通警察对驾驶员必检的物质是______ (写序号)。
①水 ②甲醇 ③乙醇
(4)酒能醉人,但酒有许多用途,如作酒精灯的燃料等,酒精燃烧的化学方程式是______ 。
 )含量严重超标。甲醇易引起视神经萎缩、甚至导致双目失明。请回答下列问题:
)含量严重超标。甲醇易引起视神经萎缩、甚至导致双目失明。请回答下列问题:(1)甲醇中
 、
、 、
、 三种元素的质量比是
三种元素的质量比是(2)甲醇中氧元素的质量分数是
(3)交通安全人人有责,为了严禁醉驾,交通警察对驾驶员必检的物质是
①水 ②甲醇 ③乙醇
(4)酒能醉人,但酒有许多用途,如作酒精灯的燃料等,酒精燃烧的化学方程式是
您最近一年使用:0次
解题方法
3 . 《本草纲目》记载:“三七近时始出,南人军中,用为金疮要药,云有奇功”。三七中止血的活性成分主要是田七氨酸(C5H8N2O5),下列说法正确的是
| A.田七氨酸中含氮气 |
| B.田七氨酸中碳、氢、氮、氧元素的质量比为5:8:2:5 |
| C.田七氨酸中碳元素的质量分数最大 |
| D.田七氨酸是由碳、氢、氮、氧四种元素组成 |
您最近一年使用:0次
解题方法
4 . 乙硫醇(化学式为C2H6S)易挥发,有蒜臭味,人对该气味极其敏感,下列有关乙硫醇的说法正确的是
| A.硫元素的质量分数是51.6% |
| B.乙硫醇是由2个碳原子、6个氢原子、1个硫原子构成 |
| C.乙硫醇中C、H、S三种元素的质量比是2:6:1 |
| D.每个乙硫醇分子由2个碳原子和6个氢分子与1个硫原子构成 |
您最近一年使用:0次
名校
解题方法
5 . 茶氨酸(化学式为C7H14N2O3)是茶叶中特有的一种氨基酸,具有降低血压的功效。下列关于茶氨酸说法不正确的是
| A.一个茶氨酸分子由26个原子构成 |
| B.茶氨酸属于氧化物 |
| C.茶氨酸由四种元素组成 |
| D.茶氨酸中碳元素的质量分数最大 |
您最近一年使用:0次
2024-01-17更新
|
44次组卷
|
2卷引用:广西壮族自治区防城港市2023-2024学年九年级上学期期末化学试题
名校
解题方法
6 . 银杏果中含有银杏酸(C12H34O3)具有抗肿瘤、抗病毒等生物学活性。下列关于银杏酸的说法正确的是
| A.银杏酸属于氧化物 |
| B.银杏酸中氢元素的质量分数最小 |
| C.银杏酸中碳元素和氢元素的质量比为6:17 |
| D.银杏酸是由12个碳原子、34个氢原子和3个氧原子构成 |
您最近一年使用:0次
2024-01-17更新
|
47次组卷
|
3卷引用:广西钦州市浦北县2023-2024学年九年级上学期期末化学试题
解题方法
7 . 乙醇( )俗称酒精,可以做酒精灯、内燃机等的燃料。下列有关乙醇的说法正确的是
)俗称酒精,可以做酒精灯、内燃机等的燃料。下列有关乙醇的说法正确的是
 )俗称酒精,可以做酒精灯、内燃机等的燃料。下列有关乙醇的说法正确的是
)俗称酒精,可以做酒精灯、内燃机等的燃料。下列有关乙醇的说法正确的是| A.乙醇由9个原子组成 |
| B.乙醇的相对分子质量为46g |
| C.乙醇中碳、氢、氧元素质量比为12:3:8 |
| D.乙醇中碳元素的质量分数约为22.2% |
您最近一年使用:0次
名校
8 . 某校化学兴趣小组的同学设计以下实验对质量守恒定律进行探究,请你参与探究并填写下列空格。
【提出问题】化学反应前后各物质的质量总和是否相等?
【猜想与假设】猜想1:化学反应前后各物质的质量总和相等;猜想2:化学反应前后各物质的质量总和不相等。
【实验探究】甲、乙两组同学用托盘天平分别称量反应前、后物质的质量。
(1)请回答下列问题。
【反思评价】
(2)通过讨论,同学们发现造成乙组天平不平衡的原因是______ 。为了解决以上装置的问题,同学们对乙组装置进行了如下图三种改进,你认为最佳装置是______ (填序号)。
A.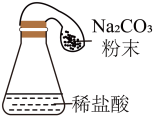 B.
B.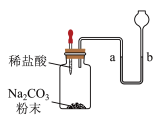 C.
C.
【得出结论】同学们利用改进后的最佳装置再次进行探究,均得出猜想1正确,即化学反应前后各物质的质量总和相等。
【启示】
(3)在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在______ 中进行。
【拓展实验】两组同学利用燃烧法来探究某种含碳元素的物质的元素组成,装置如下图。先往A中加入某种试剂a后产生氧气,往整个装置中通入一段时间氧气后再用电炉加热玻璃管使该物质样品充分燃烧,根据产物的质量确定该物质的组成。已知:B、D中的浓硫酸用于吸收水分,C中的氧化铜是确保该物质样品中的碳元素完全转化为二氧化碳,E中的氢氧化钠溶液可以吸收二氧化碳。回答下列问题:
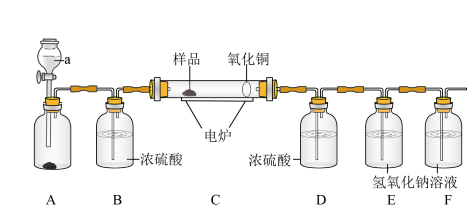
(4)装置a中盛放的物质是______ 。
(5)F的作用是______ 。
(6)若准确称取 样品(样品只含C、H、O三种元素中的两种或三种)。经充分燃烧后,D装置增重
样品(样品只含C、H、O三种元素中的两种或三种)。经充分燃烧后,D装置增重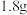 ,E装置增重
,E装置增重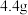 ,则该物质样品中所含的元素为
,则该物质样品中所含的元素为______ (填元素符号),质量分数最高的元素与质量分数最低的元素的原子个数比为______ (化成最简比)。
【提出问题】化学反应前后各物质的质量总和是否相等?
【猜想与假设】猜想1:化学反应前后各物质的质量总和相等;猜想2:化学反应前后各物质的质量总和不相等。
【实验探究】甲、乙两组同学用托盘天平分别称量反应前、后物质的质量。
(1)请回答下列问题。
| 甲组 | 乙组 | |
| 实验方案 | 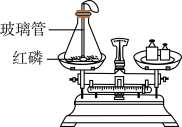 | 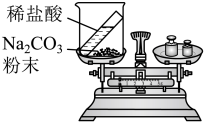 |
| 实验现象 | 红磷燃烧,放出热量,产生大量白烟, 冷却后称量,天平指针没有偏转。 | 有气泡产生,天平指针向 偏转(填“左”或“右”) |
| 结论 | 猜想1正确 | 猜想2正确 |
【反思评价】
(2)通过讨论,同学们发现造成乙组天平不平衡的原因是
A.
 B.
B. C.
C.
【得出结论】同学们利用改进后的最佳装置再次进行探究,均得出猜想1正确,即化学反应前后各物质的质量总和相等。
【启示】
(3)在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在
【拓展实验】两组同学利用燃烧法来探究某种含碳元素的物质的元素组成,装置如下图。先往A中加入某种试剂a后产生氧气,往整个装置中通入一段时间氧气后再用电炉加热玻璃管使该物质样品充分燃烧,根据产物的质量确定该物质的组成。已知:B、D中的浓硫酸用于吸收水分,C中的氧化铜是确保该物质样品中的碳元素完全转化为二氧化碳,E中的氢氧化钠溶液可以吸收二氧化碳。回答下列问题:

(4)装置a中盛放的物质是
(5)F的作用是
(6)若准确称取
 样品(样品只含C、H、O三种元素中的两种或三种)。经充分燃烧后,D装置增重
样品(样品只含C、H、O三种元素中的两种或三种)。经充分燃烧后,D装置增重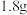 ,E装置增重
,E装置增重 ,则该物质样品中所含的元素为
,则该物质样品中所含的元素为
您最近一年使用:0次
2024-01-17更新
|
79次组卷
|
2卷引用:广西柳州市柳北区鱼峰区2023-2024学年九年级上学期第一次期末联考化学试题
解题方法
9 . 2023年9月21日,第19周杭州亚运会开幕式首次使用废碳再生的绿色甲醇(CH3OH)作为主火炬塔燃料,实现循环内碳的零排放,助力打造首届碳中和亚运会。其反应的微观示意图如图所示。
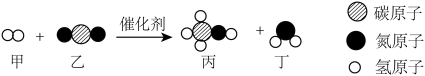
(1)从宏观上看,甲醇中质量分数最小的元素是_____ ;从微观上看,甲醇是由_____ 构成。
(2)参加反应乙与生成的丙的质量之比为_____ 。
(3)该反应的化学方程式为_____ 。

(1)从宏观上看,甲醇中质量分数最小的元素是
(2)参加反应乙与生成的丙的质量之比为
(3)该反应的化学方程式为
您最近一年使用:0次
解题方法
10 . 2021年9月,我国科学家在世界上、首次实现利用二氧化碳人工合成淀粉【(C6H10O5)n】,如图为人工合战淀粉过程中第一步反应的微观示意图,反应生成物之一为甲醇(CH3OH)。
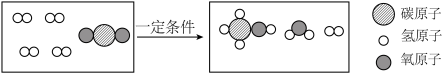
(1)写出该反应的化学方程式:______ 。
(2)从微观角度看,图中共有______ 种分子。
(3)3.2克甲醇中碳元素的质量为______ 克。
(4)若人工合成淀粉实现了工厂化、规模化生产,在一定程度上能______ (填字母)。
a.缓解粮食危机 b.缓解温室效应 c.节省耕地资源

(1)写出该反应的化学方程式:
(2)从微观角度看,图中共有
(3)3.2克甲醇中碳元素的质量为
(4)若人工合成淀粉实现了工厂化、规模化生产,在一定程度上能
a.缓解粮食危机 b.缓解温室效应 c.节省耕地资源
您最近一年使用:0次



