名校
解题方法
1 . 下列溶液中Cl-的物质的量浓度最大的是
| A.250mL 1mol/L AlCl3溶液 | B.1000mL 2.5mol/L NaCl溶液 |
| C.300mL 5mol/L KClO3溶液 | D.200mL 2mol/L MgCl2溶液 |
您最近一年使用:0次
名校
解题方法
2 . 下列溶液中氯离子浓度最大的是
A.20mL2mol L-1的CaCl2 L-1的CaCl2 | B.25mL1mol L-1的FeCl3 L-1的FeCl3 |
C.10mL4.5mol L-1的KClO3 L-1的KClO3 | D.30mL1.5mol L-1的KCl L-1的KCl |
您最近一年使用:0次
名校
解题方法
3 . NA为阿伏加德罗常数的数值,下列说法中正确的是
A.56g铁与足量的氯气反应,转移的电子数为 |
B.物质的量浓度为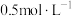  溶液中,含有Cl⁻个数为NA 溶液中,含有Cl⁻个数为NA |
C.常温常压下,14g  、 、 的混合物含有的分子数为NA 的混合物含有的分子数为NA |
D.标准状况下,17g  中含有的电子总数为 中含有的电子总数为 |
您最近一年使用:0次
名校
4 . 下面是生产生活中常见的物质。
①硫酸铝溶液②干冰③液氯④小苏打⑤ ⑥
⑥ ⑦胆矾⑧
⑦胆矾⑧ ⑨过氧化钠
⑨过氧化钠
(1)①~⑥属于电解质的是___________ (填编号),非电解质___________ (填编号)。
(2)过氧化钠常用于呼吸面具或潜水艇,其供氧原理为___________ 、___________ (写出相关化学方程式)。
(3)澄清的⑤溶液与少量④反应的离子方程式:___________ 。
(4)从 ①中取出
①中取出 ,向其中加入
,向其中加入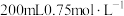 的
的 溶液恰好使
溶液恰好使 完全沉淀,则原溶液中
完全沉淀,则原溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(5)配制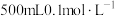 的
的 溶液时,用托盘天平称取胆矾
溶液时,用托盘天平称取胆矾___________ g。
①硫酸铝溶液②干冰③液氯④小苏打⑤
 ⑥
⑥ ⑦胆矾⑧
⑦胆矾⑧ ⑨过氧化钠
⑨过氧化钠(1)①~⑥属于电解质的是
(2)过氧化钠常用于呼吸面具或潜水艇,其供氧原理为
(3)澄清的⑤溶液与少量④反应的离子方程式:
(4)从
 ①中取出
①中取出 ,向其中加入
,向其中加入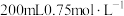 的
的 溶液恰好使
溶液恰好使 完全沉淀,则原溶液中
完全沉淀,则原溶液中 的物质的量浓度为
的物质的量浓度为(5)配制
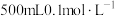 的
的 溶液时,用托盘天平称取胆矾
溶液时,用托盘天平称取胆矾
您最近一年使用:0次
名校
解题方法
5 . 将3.64gFe2O3、Al2O3样品恰好溶解在200mL0.9 mol∙L−1的盐酸中,然后向其中加入NaOH溶液使Fe3+、Al3+刚好完全沉淀,消耗NaOH溶液50mL,则NaOH溶液的浓度为
| A.3.6 mol∙L−1 | B.2.4 mol∙L−1 | C.0.9 mol∙L−1 | D.无法计算 |
您最近一年使用:0次
名校
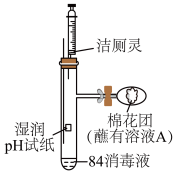
6 . 某家用防疫用品“84消毒液”的包装说明如下,请回答下列问题:
(1)该“84消毒液”有效成分NaClO的物质的量浓度为___________ mol∙L-1。
(2)欲将“84消毒液”原液稀释配制成450mLc(NaClO)=0.100 mol∙L-1的溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、___________ 、___________ 。
②配制时,需要取用___________ mL“84消毒液”原液。
③下列操作会使溶液中NaClO浓度偏低的是___________ 。
A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.容量瓶底部有蒸馏水未干燥即用来配制溶液
E.定容摇匀后,液面低于刻度线,再加水至刻度线
(3)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到pH试纸的现象是___________ 。
| 【名称】84消毒液 【规格】1000mL 【密度】1.192g/cm3 【质量分数】25%NaClO (有效成分) 注:①按一定比例稀释后使用 ②不得与酸性产品(如洁厕灵)同时使用。 |
(1)该“84消毒液”有效成分NaClO的物质的量浓度为
(2)欲将“84消毒液”原液稀释配制成450mLc(NaClO)=0.100 mol∙L-1的溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、
②配制时,需要取用
③下列操作会使溶液中NaClO浓度偏低的是
A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.容量瓶底部有蒸馏水未干燥即用来配制溶液
E.定容摇匀后,液面低于刻度线,再加水至刻度线
(3)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到pH试纸的现象是

您最近一年使用:0次
解题方法
7 . 甲醛(HCHO)是主要的室内环境污染物,同时又是重要的化工原料。
Ⅰ.利用分光光度法测定室内HCHO含量
(1)测定原理:将痕量HCHO加入过量酸性 溶液中,
溶液中, 被还原为
被还原为 ,再加入过量KI-淀粉溶液,溶液显蓝色。
,再加入过量KI-淀粉溶液,溶液显蓝色。
已知:溶液吸光度大小与溶液颜色深浅成正比。
①基态Cr原子的核外电子排布式:___________ 。
②完成离子方程式:_______
___________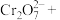 ___________
___________ ___________
___________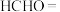 ___________
___________ ___________
___________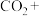 ___________
___________
(2)测定方法:
实验①:向一定量待测HCHO溶液中滴加过量酸性K2Cr2O7溶液,振荡后加入过量的淀粉-KI溶液。
实验②:用等体积去离子水代替实验①中的HCHO溶液,重复上述操作。
两组实验充分反应后,测得不同波长下吸光度A,绘制吸收光谱曲线如下图所示。
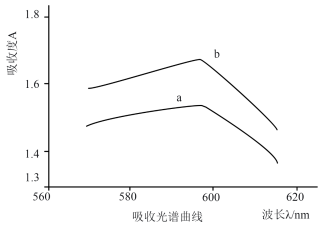
①请你判断表现实验①中溶液吸光度的曲线为___________ 。
②根据上图曲线,选定在波长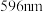 下,测定不同浓度
下,测定不同浓度 溶液的吸光度A,得到
溶液的吸光度A,得到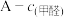 之间的关系为:
之间的关系为: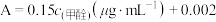 。
。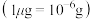 ,某待测溶液的吸光度A为0.182,则该溶液中HCHO含量为
,某待测溶液的吸光度A为0.182,则该溶液中HCHO含量为___________  。
。
Ⅱ.甲醛的制备:甲醇脱氢法
已知反应a:

反应b:
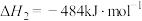
反应c: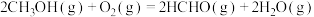
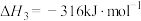
反应d:
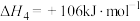
(3)
___________  。
。
(4)在一个2L恒容密闭容器中充入1molCH3OH(g),在催化剂作用下发生反应a、d,在不同温度下连续反应20min后,测得甲醇的转化率 、甲醛的选择性
、甲醛的选择性 与温度的关系如下图所示。
与温度的关系如下图所示。
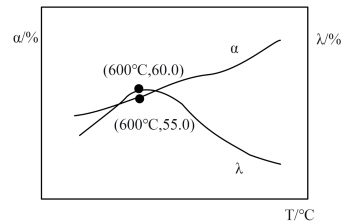
①600℃时,体系中H2的物质的量为___________  ,
,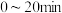 平均反应速率
平均反应速率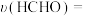
___________ mol/(L·min)。
②当温度高于650℃,甲醛的选择性下降的原因不可能是___________ 。
A.升高温度使催化剂活性降低 B.升高温度使反应a逆向移动
C.温度升高反应d速率加快 D.升高温度使反应d正向移动
Ⅰ.利用分光光度法测定室内HCHO含量
(1)测定原理:将痕量HCHO加入过量酸性
 溶液中,
溶液中, 被还原为
被还原为 ,再加入过量KI-淀粉溶液,溶液显蓝色。
,再加入过量KI-淀粉溶液,溶液显蓝色。已知:溶液吸光度大小与溶液颜色深浅成正比。
①基态Cr原子的核外电子排布式:
②完成离子方程式:
___________
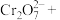 ___________
___________ ___________
___________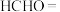 ___________
___________ ___________
___________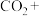 ___________
___________(2)测定方法:
实验①:向一定量待测HCHO溶液中滴加过量酸性K2Cr2O7溶液,振荡后加入过量的淀粉-KI溶液。
实验②:用等体积去离子水代替实验①中的HCHO溶液,重复上述操作。
两组实验充分反应后,测得不同波长下吸光度A,绘制吸收光谱曲线如下图所示。

①请你判断表现实验①中溶液吸光度的曲线为
②根据上图曲线,选定在波长
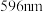 下,测定不同浓度
下,测定不同浓度 溶液的吸光度A,得到
溶液的吸光度A,得到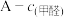 之间的关系为:
之间的关系为: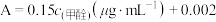 。
。 ,某待测溶液的吸光度A为0.182,则该溶液中HCHO含量为
,某待测溶液的吸光度A为0.182,则该溶液中HCHO含量为 。
。Ⅱ.甲醛的制备:甲醇脱氢法
已知反应a:


反应b:

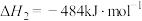
反应c:
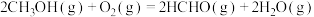
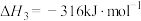
反应d:

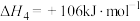
(3)

 。
。(4)在一个2L恒容密闭容器中充入1molCH3OH(g),在催化剂作用下发生反应a、d,在不同温度下连续反应20min后,测得甲醇的转化率
 、甲醛的选择性
、甲醛的选择性 与温度的关系如下图所示。
与温度的关系如下图所示。
①600℃时,体系中H2的物质的量为
 ,
,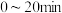 平均反应速率
平均反应速率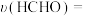
②当温度高于650℃,甲醛的选择性下降的原因不可能是
A.升高温度使催化剂活性降低 B.升高温度使反应a逆向移动
C.温度升高反应d速率加快 D.升高温度使反应d正向移动
您最近一年使用:0次
名校
8 . 现有八种物质: ①铁粉 ②NH3 ③稀盐酸 ④熔融FeCl3 ⑤CH4 ⑥CaCO3固体 ⑦CuSO4溶液 ⑧Fe3O4。
(1)①-⑥属于电解质的是_______ 。
(2)写出③与⑧反应的离子方程式_______ 。将③与⑧反应后的溶液和⑦混合,再加入过量的①,反应结束后,一定没有的阳离子为_________ 。
(3)标准状况下,4.8g⑤中所含氢原子数与______ molH2O所含氢原子数相等。
(4)标准状况下,将22.4L②溶于83mL水中形成溶液的密度为0.88g/cm3,该氨水溶质的物质的量浓度为______ mol/L ,溶质的质量分数为_______ 。
(1)①-⑥属于电解质的是
(2)写出③与⑧反应的离子方程式
(3)标准状况下,4.8g⑤中所含氢原子数与
(4)标准状况下,将22.4L②溶于83mL水中形成溶液的密度为0.88g/cm3,该氨水溶质的物质的量浓度为
您最近一年使用:0次
名校
解题方法
9 . 如图所示,甲、乙、丙常温下都为气体,2mol甲完全反应生成1mol丙和3mol乙,所得混合气体的平均摩尔质量为M g∙mol-1 ,下列判断不正确的是
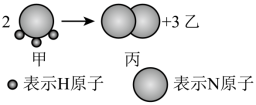

| A.同温同压下,生成丙和乙的体积比为1:3 |
| B.生成的混合气体在标准状况下的密度约为0.38g·L-1 |
| C.若 4mol甲完全反应,所得混合气体平均摩尔质量仍为M g∙mol-1 |
| D.标准状况下,将22.4L甲溶于100mL水中形成溶液,所得溶液中甲的物质的量浓度10mol·L-1 |
您最近一年使用:0次
名校
解题方法
10 . 已知Na2S溶液中含有Na+的数目为N,溶液的体积为100mL,该溶液中Na2S的物质的量浓度为
| A.N×10-2 mol/L | B. mol/L mol/L | C.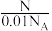 mol/L mol/L | D.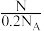 mol/L mol/L |
您最近一年使用:0次



