名校
解题方法
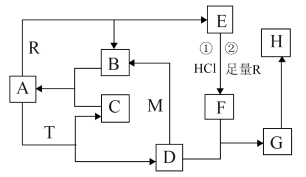
1 . A常温常压下为无色液体,B、C是无色无味的气体,M、R是两种常见的金属,且M是地壳中含量最多的金属元素的单质,T是淡黄色固体,E是具有磁性的黑色晶体,G和H组成元素相同。各物质在一定条件下有如下转化关系。___________ 。
(2)D和M在溶液中反应生成B的离子反应方程式为___________ 。
(3)T和F反应只生成C、H和一种盐,其化学反应方程式为___________ 。
(4)若向E和R的混合物中加入100mL1mol/L的盐酸,恰好使混合物完全溶解,生成FeCl2并放出448mL(标准状况)气体。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为___________ g。
(2)D和M在溶液中反应生成B的离子反应方程式为
(3)T和F反应只生成C、H和一种盐,其化学反应方程式为
(4)若向E和R的混合物中加入100mL1mol/L的盐酸,恰好使混合物完全溶解,生成FeCl2并放出448mL(标准状况)气体。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为
您最近半年使用:0次
解题方法
2 . 下表是元素周期表前20号元素的有关信息:
已知:Li的半径为0.152nm,Be的半径为0.111nm。回答下列问题:
(1)元素e在周期表中的位置为_______ ,元素y与e同主族且多一电子层,y的原子结构示意图为_______ 。
(2)c、d、g原子半径由大到小的顺序为_______ (填元素符号)。
(3)BaCl2溶液中先加入d元素最高价氧化物对应的水化物,再通入eb2,可观察到的现象是_______ ,发生反应的离子方程式为_______ 。
| 元素 | a | b | c | d | e | f | g | h |
| 原子半径/nm | 0.030 | 0.066 | 0.117 | 0.232 | 0.106 | 0.186 | 0.143 | 0.099 |
| 最高正化合价 | +1 | +4 | +1 | +6 | +1 | +3 | +7 | |
| 最低负化合价 | -2 | -4 | -2 | -1 |
(1)元素e在周期表中的位置为
(2)c、d、g原子半径由大到小的顺序为
(3)BaCl2溶液中先加入d元素最高价氧化物对应的水化物,再通入eb2,可观察到的现象是
您最近半年使用:0次
名校
解题方法
3 . 完成下列问题。
(1)现有下列9种物质:①O2;②I2;③NH3;④CO2;⑤Na2O2;⑥H2SO4;⑦Ba(OH)2;⑧NaF;⑨NH4NO3。其中只含离子键的是_______ ;既含离子键又含非极性键的是_______ (填序号,下同);既含离子键又含极性键的是_______ 。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为_______ ;若XY2为共价化合物,则其结构式为_______ 。
(3)X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质为黄绿色有害气体。请回答下列问题:
①R在元素周期表中的位置为_______ ,Y的原子结构示意图为_______ 。
②Z、Q、M简单离子半径由大到小的顺序为(写元素离子符号)_______ 。
③M的单质与R的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(1)现有下列9种物质:①O2;②I2;③NH3;④CO2;⑤Na2O2;⑥H2SO4;⑦Ba(OH)2;⑧NaF;⑨NH4NO3。其中只含离子键的是
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为
(3)X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质为黄绿色有害气体。请回答下列问题:
①R在元素周期表中的位置为
②Z、Q、M简单离子半径由大到小的顺序为(写元素离子符号)
③M的单质与R的最高价氧化物对应的水化物反应的离子方程式为
您最近半年使用:0次
4 . A、B、C、D四种有机物,A、B 属于烃类物质,C、D都是烃的衍生物。A 是含氢质量分数最大的有机物,分子结构为正四面体;B的球棍模型为 ;C的相对分子质量为46,能与Na反应, 但不能与NaOH 溶液反应;D的比例模型为
;C的相对分子质量为46,能与Na反应, 但不能与NaOH 溶液反应;D的比例模型为 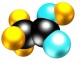 ,该物质的水溶液中滴加石蕊变红色。
,该物质的水溶液中滴加石蕊变红色。
请回答下列问题:
(1)A的结构式是___________ ,C 中官能团的名称是___________ 。
(2)B的结构简式是___________ ,该物质发生加聚反应的化学方程式为___________ 。
(3)已知 B 可以发生如下转化过程:

i.上述转化过程中属于加成反应的是___________ (填序号)。
ii.完成转化②的化学方程式:___________ 。
iii.下列关于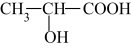 的说法正确的是
的说法正确的是___________ (填字母序号)。
A.该物质属于烃类化合物
B.该物质可以发生酯化反应
C.1mol该物质与足量金属钠反应,可生成1mol氢气
D.该物质既能使酸性高锰酸钾溶液褪色,也能使溴水褪色
(4)请写出C和D发生酯化反应的化学方程式___________ 。
 ;C的相对分子质量为46,能与Na反应, 但不能与NaOH 溶液反应;D的比例模型为
;C的相对分子质量为46,能与Na反应, 但不能与NaOH 溶液反应;D的比例模型为  ,该物质的水溶液中滴加石蕊变红色。
,该物质的水溶液中滴加石蕊变红色。请回答下列问题:
(1)A的结构式是
(2)B的结构简式是
(3)已知 B 可以发生如下转化过程:

i.上述转化过程中属于加成反应的是
ii.完成转化②的化学方程式:
iii.下列关于
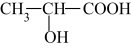 的说法正确的是
的说法正确的是A.该物质属于烃类化合物
B.该物质可以发生酯化反应
C.1mol该物质与足量金属钠反应,可生成1mol氢气
D.该物质既能使酸性高锰酸钾溶液褪色,也能使溴水褪色
(4)请写出C和D发生酯化反应的化学方程式
您最近半年使用:0次
解题方法
5 . 已知X、Y、Z、R、W、Q六种元素中,X的原子序数为1;Y元素原子最外层电子数是内层电子总数的2倍;Z元素原子次外层电子数比其最外层电子数少4个;R元素原子最外层有1个电子,其阳离子与Z的阴离子原子核外电子总数相同;W元素原子K层和M层电子总数等于其L层电子数。请要求填空:
(1)Z元素形成的原子的结构示意图为___________ ;
(2)从前五种元素中选出三种元素组成化合物,其中属于碱的是___________ (填化学式);属于非电解质的是___________ (填一种物质的名称即可);
(3)现有标准状况下YZ和 混合气体8.96L,其质量为16g,则该气体中,YZ和
混合气体8.96L,其质量为16g,则该气体中,YZ和 的物质的量之比为
的物质的量之比为___________ ;
(4)55.0g化合物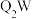 中含有
中含有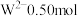 ,则Q的相对原子质量为
,则Q的相对原子质量为___________ ;
(5)将4.00gRZX溶于一定量水,所得溶液的体积为100mL,该溶液中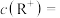
___________ ;
(6)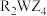 溶于水的电离方程式
溶于水的电离方程式___________ ;
(7)化合物 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
(1)Z元素形成的原子的结构示意图为
(2)从前五种元素中选出三种元素组成化合物,其中属于碱的是
(3)现有标准状况下YZ和
 混合气体8.96L,其质量为16g,则该气体中,YZ和
混合气体8.96L,其质量为16g,则该气体中,YZ和 的物质的量之比为
的物质的量之比为(4)55.0g化合物
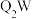 中含有
中含有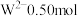 ,则Q的相对原子质量为
,则Q的相对原子质量为(5)将4.00gRZX溶于一定量水,所得溶液的体积为100mL,该溶液中
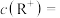
(6)
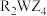 溶于水的电离方程式
溶于水的电离方程式(7)化合物
 与
与 反应的化学方程式为
反应的化学方程式为
您最近半年使用:0次
解题方法
6 . 下表显示了元素周期表中的一部分。
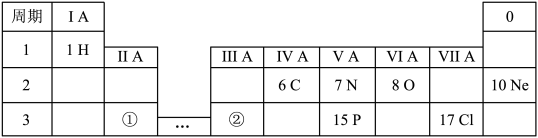
请回答下列问题:
(1)磷元素的原子序数是___________ 。
(2)属于稀有气体的是___________ (选填“ ”或“
”或“ ”)。
”)。
(3)碳元素在元素周期表的第___________ (选填“二”或“三”)周期第___________ (选填“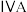 ”或“
”或“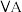 ”)族。
”)族。
(4)红棕色气体 中氮元素的化合价为
中氮元素的化合价为___________ (选填“ ”或“
”或“ ”)价。
”)价。
(5)含有共价键的单质是___________ (选填“ ”或“
”或“ ”)。
”)。
(6)已知同周期元素从左到右金属性逐渐减弱,则元素的金属性强弱:①___________ ②(选填“大于”或“小于”)。
(7)下列化学用语使用正确的是:___________ (填写字母)。
A.中子数为8的碳原子符号为 B.氯化氢的电子式为
B.氯化氢的电子式为

请回答下列问题:
(1)磷元素的原子序数是
(2)属于稀有气体的是
 ”或“
”或“ ”)。
”)。(3)碳元素在元素周期表的第
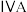 ”或“
”或“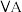 ”)族。
”)族。(4)红棕色气体
 中氮元素的化合价为
中氮元素的化合价为 ”或“
”或“ ”)价。
”)价。(5)含有共价键的单质是
 ”或“
”或“ ”)。
”)。(6)已知同周期元素从左到右金属性逐渐减弱,则元素的金属性强弱:①
(7)下列化学用语使用正确的是:
A.中子数为8的碳原子符号为
 B.氯化氢的电子式为
B.氯化氢的电子式为
您最近半年使用:0次
解题方法
7 . X、Y、Z、W、M、N、P为元素周期表前20号主族元素,Y原子最外层电子数为其内层电子数的一半,Z的原子序数为8,M的焰色为黄色,N与Z同主族,P是人体含量最多的金属元素,其中元素的原子序数和原子半径的关系如图所示,请回答下列问题:
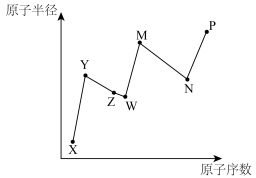
(1)Y为_______ (填元素名称);非金属性:W_______ (填“>”或“<”,下同)N;简单离子半径:Y_______ W。
(2)单质M与X2Z反应的化学方程式为______ ,该反应的还原产物为_______ (填化学式)。
(3)MX可用作金属氯化物的还原剂、有机合成的还原剂、加氢剂、缩合剂,该化合物熔融状态下能导电。MX为_______ (填“离子”或“共价”)化合物,用电子式表示MX的形成过程:_______ 。
(4)下列说法正确的是_______ (填标号)。
a.最高价氧化物对应水化物的碱性:Y>M
b.X2与W2在暗处混合后会剧烈反应并发生爆炸
c.P与水反应时部分生成物会覆盖在P表面,可能导致P与水反应的剧烈程度不如M
d.Y在Z2中燃烧的产物为YZ2

(1)Y为
(2)单质M与X2Z反应的化学方程式为
(3)MX可用作金属氯化物的还原剂、有机合成的还原剂、加氢剂、缩合剂,该化合物熔融状态下能导电。MX为
(4)下列说法正确的是
a.最高价氧化物对应水化物的碱性:Y>M
b.X2与W2在暗处混合后会剧烈反应并发生爆炸
c.P与水反应时部分生成物会覆盖在P表面,可能导致P与水反应的剧烈程度不如M
d.Y在Z2中燃烧的产物为YZ2
您最近半年使用:0次
名校
解题方法
8 . 随着原子序数的递增,8种短周期元素(用英文字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
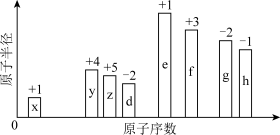
(1)这8种元素中,金属性最强的元素在周期表中的位置是___________ 。
(2)元素x分别与y、z、d形成的10电子气态分子中,热稳定性由强到弱的顺序为___________ (填化学式)。元素z、d、e、f形成的简单离子,半径较大的离子是___________ (填离子符号)。
(3)将化合物eh由固态加热至熔融态,吸收的能量主要用于断裂___________ 键(填“离子”或“共价”)。x与d可形成多种共价分子,其中三原子共价分子的电子式为___________ ;四原子共价分子的结构式为___________ 。
(4)不能作为比较g与h的非金属性强弱的依据是___________。
(5)f的单质与盐酸发生反应的离子方程式为___________ 。

(1)这8种元素中,金属性最强的元素在周期表中的位置是
(2)元素x分别与y、z、d形成的10电子气态分子中,热稳定性由强到弱的顺序为
(3)将化合物eh由固态加热至熔融态,吸收的能量主要用于断裂
(4)不能作为比较g与h的非金属性强弱的依据是___________。
| A.氢化物酸性h强于g |
B.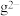 的还原性强于 的还原性强于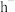 |
| C.与x单质反应,g单质比h单质更困难 |
| D.常温下g单质呈固态,h单质呈气态 |
(5)f的单质与盐酸发生反应的离子方程式为
您最近半年使用:0次
2024-02-26更新
|
98次组卷
|
2卷引用:河北省唐山市2023-2024学年高一上学期1月期末考试化学试题
名校
解题方法
9 . 下表为元素周期表中主族元素的相关信息,其中 、
、 、
、 、
、 、
、 、
、 为短周期元素
为短周期元素

请依据上述信息回答下列问题:
(1) 在元素周期表的位置是
在元素周期表的位置是___________ 。
(2) 离子
离子 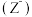 的原子结构示意图:
的原子结构示意图:___________ 。
(3)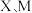 分别与
分别与  形成的化合物中较稳定的是
形成的化合物中较稳定的是___________ (写化学式)。
(4) 和
和  形成的化合物
形成的化合物  可在野外用作供氢剂。请写出
可在野外用作供氢剂。请写出 跟水反应化学方程式:
跟水反应化学方程式:___________ 。
(5)写出 与水反应的离子方程式:
与水反应的离子方程式:___________ 。向 的水溶液中滴加几滴紫色石蕊溶液,现象为
的水溶液中滴加几滴紫色石蕊溶液,现象为___________ 。
 、
、 、
、 、
、 、
、 、
、 为短周期元素
为短周期元素| 元素 | 相关信息 |
 |  在自然界中有三种核素,其中一核素没有中子 在自然界中有三种核素,其中一核素没有中子 |
 |  为第三周期元素,其最高价氧化物的水化物A是一种强碱 为第三周期元素,其最高价氧化物的水化物A是一种强碱 |
 |  的原子最外层电子数是其内层电子数的三倍 的原子最外层电子数是其内层电子数的三倍 |
 |  是自然界中含量最高的金属 是自然界中含量最高的金属 |
 |  、 、 、 、 组成的36电子的化合物B是家用消毒剂的主要成分 组成的36电子的化合物B是家用消毒剂的主要成分 |
 | 元素原子最外层比次外层少2个电子 |
 |  在元素周期表中的位置如图所示 在元素周期表中的位置如图所示 |

请依据上述信息回答下列问题:
(1)
 在元素周期表的位置是
在元素周期表的位置是(2)
 离子
离子 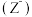 的原子结构示意图:
的原子结构示意图:(3)
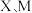 分别与
分别与  形成的化合物中较稳定的是
形成的化合物中较稳定的是(4)
 和
和  形成的化合物
形成的化合物  可在野外用作供氢剂。请写出
可在野外用作供氢剂。请写出 跟水反应化学方程式:
跟水反应化学方程式:(5)写出
 与水反应的离子方程式:
与水反应的离子方程式: 的水溶液中滴加几滴紫色石蕊溶液,现象为
的水溶液中滴加几滴紫色石蕊溶液,现象为
您最近半年使用:0次
名校
解题方法
10 . 随着原子序数的递增,7种短周期元素A~G的最高正价或最低负价与原子序数的关系如图。
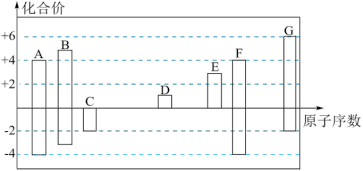
回答下列问题:
(1)写出中子数为8的A元素的一种核素的化学符号_______ 。
(2)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为_______ 。
(3)E元素最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式为_______ 。
(4)元素A与G形成的电子总数为38的分子的结构式为_______ 。
(5)元素C与D按原子个数比1:1形成的化合物的电子式为_______ ,所含有化学键类型有_______ 。
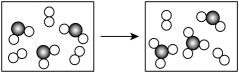
(6)如图表示由C、G元素组成的两种气体分子在一定条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:_______ 。

回答下列问题:
(1)写出中子数为8的A元素的一种核素的化学符号
(2)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(3)E元素最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式为
(4)元素A与G形成的电子总数为38的分子的结构式为
(5)元素C与D按原子个数比1:1形成的化合物的电子式为
(6)如图表示由C、G元素组成的两种气体分子在一定条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:

您最近半年使用:0次



