解题方法
1 . 我国承诺在2030年实现“碳达峰”,2060年实现“碳中和”, 资源化利用具有重要意义,回答下列问题:
资源化利用具有重要意义,回答下列问题:
I. 和
和 在镍基催化作用下重整模型如图所示(已知:*表示催化剂活性位点,
在镍基催化作用下重整模型如图所示(已知:*表示催化剂活性位点,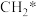 表示活性亚甲基)。
表示活性亚甲基)。 和
和 在镍基催化作用下发生重整反应的化学方程式为
在镍基催化作用下发生重整反应的化学方程式为_____ 。该反应在高温下才能自发进行,判断反应焓变
_____ (填“大于”“小于”或“等于”)0,判断理由是_____ 。
(2)已知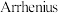 经验公式:
经验公式: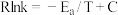 (
( 为活化能,k为速率常数,R和C为常数),该反应的速率常数
为活化能,k为速率常数,R和C为常数),该反应的速率常数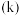 、活化能
、活化能 与温度
与温度 的关系如图:
的关系如图: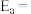
_____  。(用含有
。(用含有 的式子表示)
的式子表示)
Ⅱ.已知二氧化碳和氢气合成甲醇可能发生如下反应:
i.

ii.

(3)为提高甲醇平衡产率,可采取的措施有_____ (至少答两条)。
(4)若以 为催化剂,其活性温度范围通常为
为催化剂,其活性温度范围通常为 。向装有催化剂的密闭容器按投料比为
。向装有催化剂的密闭容器按投料比为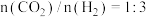 通入反应物,保持压强为
通入反应物,保持压强为 ,若只发生反应i,其他条件相同,不同温度下。5分钟内,测得温度与甲醇的产率关系如图,实际产率呈现先升高后降低的原因是
,若只发生反应i,其他条件相同,不同温度下。5分钟内,测得温度与甲醇的产率关系如图,实际产率呈现先升高后降低的原因是_____ 。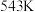 时的压强平衡常数
时的压强平衡常数
_____  。(写出计算式)
。(写出计算式)
 资源化利用具有重要意义,回答下列问题:
资源化利用具有重要意义,回答下列问题:I.
 和
和 在镍基催化作用下重整模型如图所示(已知:*表示催化剂活性位点,
在镍基催化作用下重整模型如图所示(已知:*表示催化剂活性位点,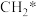 表示活性亚甲基)。
表示活性亚甲基)。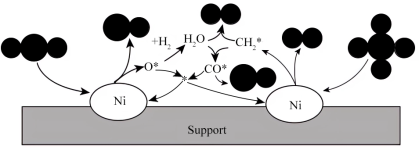
 和
和 在镍基催化作用下发生重整反应的化学方程式为
在镍基催化作用下发生重整反应的化学方程式为
(2)已知
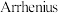 经验公式:
经验公式: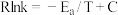 (
( 为活化能,k为速率常数,R和C为常数),该反应的速率常数
为活化能,k为速率常数,R和C为常数),该反应的速率常数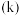 、活化能
、活化能 与温度
与温度 的关系如图:
的关系如图: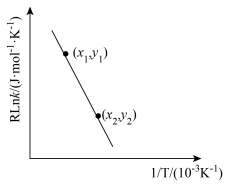
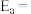
 。(用含有
。(用含有 的式子表示)
的式子表示)Ⅱ.已知二氧化碳和氢气合成甲醇可能发生如下反应:
i.


ii.


(3)为提高甲醇平衡产率,可采取的措施有
(4)若以
 为催化剂,其活性温度范围通常为
为催化剂,其活性温度范围通常为 。向装有催化剂的密闭容器按投料比为
。向装有催化剂的密闭容器按投料比为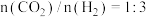 通入反应物,保持压强为
通入反应物,保持压强为 ,若只发生反应i,其他条件相同,不同温度下。5分钟内,测得温度与甲醇的产率关系如图,实际产率呈现先升高后降低的原因是
,若只发生反应i,其他条件相同,不同温度下。5分钟内,测得温度与甲醇的产率关系如图,实际产率呈现先升高后降低的原因是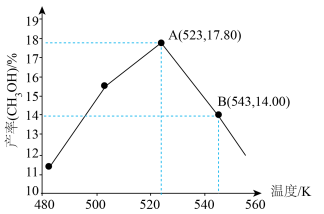
 时的压强平衡常数
时的压强平衡常数
 。(写出计算式)
。(写出计算式)
您最近半年使用:0次
名校
解题方法
2 . 中国科学家以 为催化剂,在不同电解质溶液中实现常温电催化合成氨来对
为催化剂,在不同电解质溶液中实现常温电催化合成氨来对 进行活化,其反应历程与相对能量模拟计算结果如图。下列说法正确的是
进行活化,其反应历程与相对能量模拟计算结果如图。下列说法正确的是
 为催化剂,在不同电解质溶液中实现常温电催化合成氨来对
为催化剂,在不同电解质溶液中实现常温电催化合成氨来对 进行活化,其反应历程与相对能量模拟计算结果如图。下列说法正确的是
进行活化,其反应历程与相对能量模拟计算结果如图。下列说法正确的是
A. 溶液更加有利于 溶液更加有利于 对 对 的活化 的活化 |
B.两种电解质溶液环境下反应 → → 的焓变不同 的焓变不同 |
C. 活化过程中· 活化过程中· →· →· 吸收的热量最多 吸收的热量最多 |
D. 的活化过程中只包含N≡N键断裂 的活化过程中只包含N≡N键断裂 |
您最近半年使用:0次
3 . 一种利用 和
和 直接合成
直接合成 的反应历程如下图所示。下列说法中错误的是
的反应历程如下图所示。下列说法中错误的是
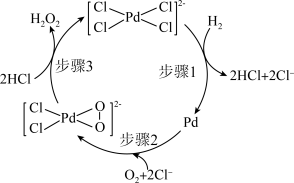
| A.总反应的原子利用率理论上可达100% |
B.步骤2中,若 完全反应,则理论上转移电子数目为2NA 完全反应,则理论上转移电子数目为2NA |
C.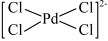 降低了反应的活化能,加快了反应速率 降低了反应的活化能,加快了反应速率 |
D. 和 和 中Pd的化合价不相同 中Pd的化合价不相同 |
您最近半年使用:0次
解题方法
4 . 乙烯氢化的热化学方程式为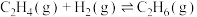
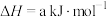 ,使用不同含Au催化剂的反应历程如图所示。下列说法错误的是
,使用不同含Au催化剂的反应历程如图所示。下列说法错误的是
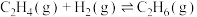
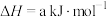 ,使用不同含Au催化剂的反应历程如图所示。下列说法错误的是
,使用不同含Au催化剂的反应历程如图所示。下列说法错误的是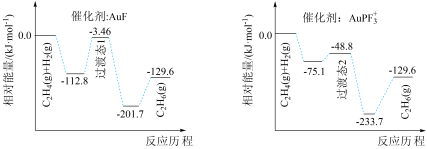
A.1mol 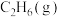 的能量小于1mol 的能量小于1mol 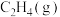 与1mol 与1mol  具有的能量之和 具有的能量之和 |
B.该反应的焓变: |
| C.过渡态物质的稳定性:过渡态1>过渡态2 |
D.相应的活化能:催化剂AuF>催化剂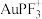 |
您最近半年使用:0次
5 . 2-溴丁烷在乙醇钾(C2H5OK)作用下发生消去反应的能量变化如下图所示。下列说法正确的是
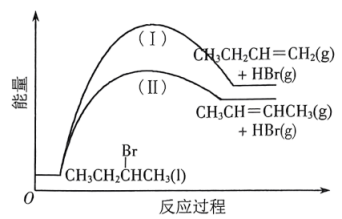
| A.活化能:反应Ⅰ<反应Ⅱ |
| B.产物的稳定性:1-丁烯>2-丁烯 |
| C.相同条件下完全燃烧放出的热量:1-丁烯>2-丁烯 |
| D.选择相对较短的反应时间,及时分离可获得高产率的1-丁烯 |
您最近半年使用:0次
6 . 多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),甲醇 与水在铜基催化剂上的反应机理和能量图如图:
与水在铜基催化剂上的反应机理和能量图如图:
 与水在铜基催化剂上的反应机理和能量图如图:
与水在铜基催化剂上的反应机理和能量图如图:
A.反应Ⅱ的热化学方程式为: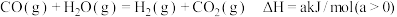 |
B. 在反应中生成又消耗, 在反应中生成又消耗, 可认为是催化剂 可认为是催化剂 |
C.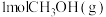 和 和 的总能量小于 的总能量小于 和 和 的总能量 的总能量 |
| D.选择优良的催化剂可以降低反应Ⅰ和Ⅱ的活化能,减少过程中的能耗和反应的焓变 |
您最近半年使用:0次
7 . 某反应由两步反应A→B→C构成,其反应能量曲线如图所示,下列叙述不正确的是

| A.A→C的反应为放热反应 |
| B.三种物质中B最不稳定 |
| C.A与B的能量差为E1-E2 |
| D.B→C的反应不需要加热 |
您最近半年使用:0次
解题方法
8 . 25℃时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图所示。

| A.在该反应条件下,产物1比产物2稳定 |
| B.固体酸分子筛可通过氢键吸附乙醇 |
| C.固体酸分子筛能减小图示反应的焓变 |
D.生成产物1的决速步骤的活化能为36.7 |
您最近半年使用:0次
2024-04-13更新
|
213次组卷
|
2卷引用:河南省新乡市2024届高三第二次模拟考试理综-化学试题
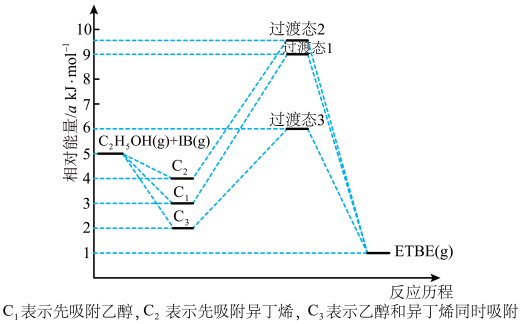
9 . 乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应的化学方程式为C2H5OH(g)+IB(g) ETBE(g) △H。回答下列问题:
ETBE(g) △H。回答下列问题:
(1)反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=______ kJ•mol-1。反应历程的最优途径是______ (填“C1”、“C2”或“C3”)。 2CO2(g)+S(l) △H=-270kJ•mol-1。
2CO2(g)+S(l) △H=-270kJ•mol-1。
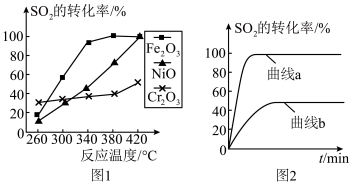
①其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是_______ 。
②某科研小组用Fe2O3作催化剂。在380℃时,分别研究了n(CO):n(SO2)为1:1、3:1时SO2转化率的变化情况(图2)。则图2中表示n(CO):n(SO2)=3:1的变化曲线为______ 。 N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压
N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压 物质的量分数)有如下关系:
物质的量分数)有如下关系: (NO2)=k1×p2(NO2),
(NO2)=k1×p2(NO2), (N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
(N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=______ ;在图3标出的点中,能表示反应达到平衡状态的点是______ 。
 ETBE(g) △H。回答下列问题:
ETBE(g) △H。回答下列问题:(1)反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=
 2CO2(g)+S(l) △H=-270kJ•mol-1。
2CO2(g)+S(l) △H=-270kJ•mol-1。①其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是
②某科研小组用Fe2O3作催化剂。在380℃时,分别研究了n(CO):n(SO2)为1:1、3:1时SO2转化率的变化情况(图2)。则图2中表示n(CO):n(SO2)=3:1的变化曲线为
 N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压
N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压 物质的量分数)有如下关系:
物质的量分数)有如下关系: (NO2)=k1×p2(NO2),
(NO2)=k1×p2(NO2), (N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
(N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
您最近半年使用:0次
名校
解题方法
10 . 卤代烃是重要的工业原料,同时对环境造成严重影响,如破坏臭氧层等,请回答下列问题:
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)
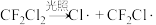 反应①
反应①
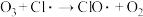 反应②
反应②
 反应③
反应③
(1)活性氯( )的作用是
)的作用是_____ 。
反应②和反应③的能量变化图如下所示
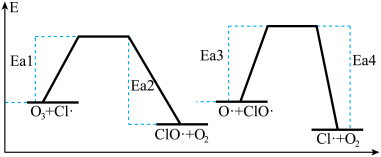
(2)利用上图数据计算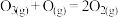 的
的
_____ 。
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)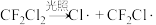 反应①
反应①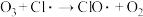 反应②
反应② 反应③
反应③(1)活性氯(
 )的作用是
)的作用是反应②和反应③的能量变化图如下所示

(2)利用上图数据计算
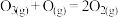 的
的
您最近半年使用:0次



