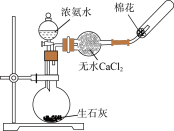
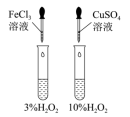
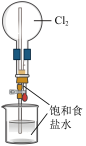
1 . 科学探究要实事求是、严谨细致。某化学兴趣小组设计实验进行有关氯化物的探究实验,回答下列问题:
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:___________ 。
(2)装置A中设计g管的作用是___________ 。
(3)装置A中发生反应的离子方程式为___________ 。
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
(4)由实验1、2现象可以得出结论:增大pH,___________ 优先于___________ 放电;
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是___________ ;
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验___________ 作对照实验;
③实验目的ii是___________ ;
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:___________ 。
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:
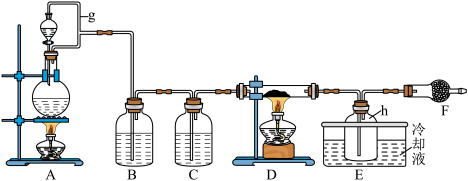
(2)装置A中设计g管的作用是
(3)装置A中发生反应的离子方程式为
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
| 实验编号 | 电压/V | pH | 阳极现象 | 阴极现象 |
| 1 | 1.5 | 1.00 | 无气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
| 2 | 1.5 | 5.52 | 无气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 3 | 3.0 | 5.52 | 少量气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 4 | 4.5 | 5.52 | 大量气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
(4)由实验1、2现象可以得出结论:增大pH,
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
| 实验编号 | c(NH4Cl)/mol·L-1 | 温度/℃ | 待测物理量X | 实验目的 |
| 5 | 0.5 | 30 | a | ___________ |
| 6 | 1.5 | i | b | 探究浓度对氯化铵水解平衡的影响 |
| 7 | 1.5 | 35 | c | ii |
| 8 | 2.0 | 40 | d | 探究温度、浓度同时对氯化铵化解平衡的影响 |
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验
③实验目的ii是
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:
您最近半年使用:0次
2 . 用下列实验装置完成对应实验,能达到实验目的的是
|
|
|
|
| A | B | C | D |
| A.制取并收集少量氨气 |
| B.探究Fe3+、Cu2+对H2O2分解速率的影响 |
| C.除去CO2中的SO2 |
| D.氯气的喷泉实验 |
您最近半年使用:0次
名校
解题方法
3 . 某小组设计实验探究铜和浓硫酸反应产物的装置如图所示:
已知:浓硫酸的沸点约为338℃;实验中可能有 、
、 生成,都是难溶于水、难溶于稀硫酸的黑色固体。
生成,都是难溶于水、难溶于稀硫酸的黑色固体。
下列关于实验操作或实验结论的叙述正确的是
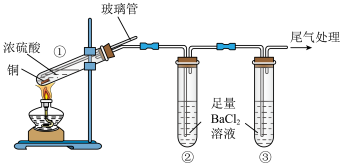
试管 | ① | ② | ③ |
实验现象 | 铜完全溶解后,溶液仍为无色,有白雾、灰白掺杂的黑色固体产生 | 有大量白色沉淀产生 | 有少量白色沉淀产生 |
 、
、 生成,都是难溶于水、难溶于稀硫酸的黑色固体。
生成,都是难溶于水、难溶于稀硫酸的黑色固体。下列关于实验操作或实验结论的叙述正确的是
| A.为防止实验时压强过大,可将玻璃管拉出液面以上 |
| B.为了检验试管①中的固体成分,实验结束后,取下试管①并向其中加入适量的水 |
C.试管②和③中白色沉淀的主要成分都是 |
| D.用浓氨水吸收尾气防污染 |
您最近半年使用:0次
4 . 过二硫酸钠( )也叫高硫酸钠,可用于废气处理及有害物质的氧化降解。用
)也叫高硫酸钠,可用于废气处理及有害物质的氧化降解。用 溶液和一定浓度的NaOH溶液混合可制得
溶液和一定浓度的NaOH溶液混合可制得 晶体。实验室制备
晶体。实验室制备 晶体的装置如下图所示:
晶体的装置如下图所示: 。
。
(1)写出装置中生成 的反应的化学方程式:
的反应的化学方程式:___________ 。
(2)盛装NaOH溶液的仪器名称为___________ ,持续通入氮气的目的是___________ 。
(3)装置中硫酸的作用是___________ 。
(4)某兴趣小组设计实验探究不同环境下 氧化性的强弱。将
氧化性的强弱。将 (1.69g)与过量
(1.69g)与过量 (10g)溶于水中形成的混合溶液煮沸3min,观察并记录加入试剂时和加热过程中的现象(如下表所示)。
(10g)溶于水中形成的混合溶液煮沸3min,观察并记录加入试剂时和加热过程中的现象(如下表所示)。
①在___________ (填“中性”“酸性”或“碱性”)条件下, 的氧化能力最强。
的氧化能力最强。
②若用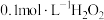 溶液滴定碱性氧化反应后的溶液(先将溶液调至酸性再滴定),滴定终点时的现象为
溶液滴定碱性氧化反应后的溶液(先将溶液调至酸性再滴定),滴定终点时的现象为___________ ;达到滴定终点时,消耗 溶液的体积为
溶液的体积为 。则碱性氧化后的溶液中
。则碱性氧化后的溶液中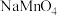 的质量为
的质量为___________ g(用含 的代数式表示,
的代数式表示,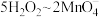 )
)
 )也叫高硫酸钠,可用于废气处理及有害物质的氧化降解。用
)也叫高硫酸钠,可用于废气处理及有害物质的氧化降解。用 溶液和一定浓度的NaOH溶液混合可制得
溶液和一定浓度的NaOH溶液混合可制得 晶体。实验室制备
晶体。实验室制备 晶体的装置如下图所示:
晶体的装置如下图所示: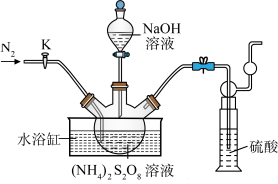
 。
。(1)写出装置中生成
 的反应的化学方程式:
的反应的化学方程式:(2)盛装NaOH溶液的仪器名称为
(3)装置中硫酸的作用是
(4)某兴趣小组设计实验探究不同环境下
 氧化性的强弱。将
氧化性的强弱。将 (1.69g)与过量
(1.69g)与过量 (10g)溶于水中形成的混合溶液煮沸3min,观察并记录加入试剂时和加热过程中的现象(如下表所示)。
(10g)溶于水中形成的混合溶液煮沸3min,观察并记录加入试剂时和加热过程中的现象(如下表所示)。| 环境 | 调节溶液氧化环境时的现象 | 加热煮沸3min期间产生的现象 |
| 中性 | 加入VmL蒸馏水,无明显现象 | 30s时开始有大量气泡冒出,3min后溶液变为深棕色,溶液中有悬浮小颗粒 |
| 碱性 | 加入VmL某浓度的NaOH溶液,瞬间变为棕色( ) ) | 10s后溶液逐渐变为深紫色( ),没有明显冒气泡现象 ),没有明显冒气泡现象 |
| 酸性 | 加入VmL稀硫酸无明显现象 | 煮沸3min后,有气泡冒出 |
 的氧化能力最强。
的氧化能力最强。②若用
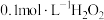 溶液滴定碱性氧化反应后的溶液(先将溶液调至酸性再滴定),滴定终点时的现象为
溶液滴定碱性氧化反应后的溶液(先将溶液调至酸性再滴定),滴定终点时的现象为 溶液的体积为
溶液的体积为 。则碱性氧化后的溶液中
。则碱性氧化后的溶液中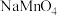 的质量为
的质量为 的代数式表示,
的代数式表示,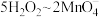 )
)
您最近半年使用:0次
5 . 氮及其化合物的转化具有重要应用。
(1)实验室模拟用浓硫酸脱除氮氧化物,装置如下图所示,实验开始后装置C中发生反应: 。
。_______ ,B装置的作用是_______ 。
②理论上应相同时间内控制 处通入气体的物质的量之比为
处通入气体的物质的量之比为_______ 。
(2)已知: (浓)
(浓)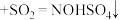 。请补充完整由
。请补充完整由 固体制备纯净的
固体制备纯净的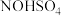 晶体的实验方案:向一定量
晶体的实验方案:向一定量 固体中加入
固体中加入_______ ,将反应后得到的混合物过滤、洗涤、干燥。(须选用的试剂有: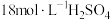 溶液,浓
溶液,浓 ,
, 溶液)
溶液)
(1)实验室模拟用浓硫酸脱除氮氧化物,装置如下图所示,实验开始后装置C中发生反应:
 。
。
②理论上应相同时间内控制
 处通入气体的物质的量之比为
处通入气体的物质的量之比为(2)已知:
 (浓)
(浓)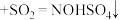 。请补充完整由
。请补充完整由 固体制备纯净的
固体制备纯净的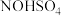 晶体的实验方案:向一定量
晶体的实验方案:向一定量 固体中加入
固体中加入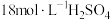 溶液,浓
溶液,浓 ,
, 溶液)
溶液)
您最近半年使用:0次
6 . 根据下列实验操作和现象得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,溶液变为黄色 | 氧化性:H2O2>Fe3+ |
| B | 将灼热的炭加入盛有浓HNO3的试管中,试管上方出现红棕色气体 | C和浓HNO3反应产生NO2 |
| C | 将少量NH4Cl晶体放入试管底部,在试管口塞上一团棉花,用酒精灯在试管底部药品处小火微热,试管底部的固体消失,试管口处的内壁上出现“白霜” | NH4Cl晶体依次发生了升华和凝华 |
| D | 将Fe2O3粉末与铝粉混合均匀,在混合物上面加适量KClO3,再用镁条引燃混合物,有熔融铁水流出 | 铝的还原性强于铁,且Fe2O3与铝粉的反应放热 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
7 . 已知:常温下,铝表面致密的氧化膜能提高铝的抗腐蚀性。为研究影响铝抗腐蚀性的因素,进行如下实验:(已知:含Cu2+溶液呈酸性)
现将一置于空气中的铝片投入浓氯化铜溶液中,铝片表面出现一层海绵状暗红色物质,接下来铝片上产生大量气泡,溶液温度迅速上升。若用同样的铝片投入相同浓度的硫酸铜溶液中,在短时间内铝片无明显变化。
(1)造成上述不同现象的原因可能是___________。
(2)请设计一个简单实验验证你的选择___________ 。
现将一置于空气中的铝片投入浓氯化铜溶液中,铝片表面出现一层海绵状暗红色物质,接下来铝片上产生大量气泡,溶液温度迅速上升。若用同样的铝片投入相同浓度的硫酸铜溶液中,在短时间内铝片无明显变化。
(1)造成上述不同现象的原因可能是___________。
| A.铝与氯化铜溶液反应,与硫酸铜溶液不反应 |
| B.氯离子能破坏氧化铝薄膜,而硫酸根离子不能 |
C.生成物AlCl3溶于水,而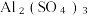 不溶于水 不溶于水 |
| D.氯化铜溶液酸性比同浓度的硫酸铜溶液酸性强 |
您最近半年使用:0次
8 . 取一支硬质大试管,通过排饱和NaCl溶液的方法先后收集半试管甲烷和半试管氯气(如图),下列对于试管内发生的反应及现象的说法正确的是

| A.为加快化学反应速率,应在强烈日光直接照射下完成 |
| B.甲烷和Cl2反应后试管内壁出现了油状液滴,是因为该反应生成了氯化氢 |
| C.CH4和Cl2的反应属于取代反应 |
| D.该反应结束后,液面上升,液体充满试管 |
您最近半年使用:0次
昨日更新
|
305次组卷
|
2卷引用:广东省江门市鹤山市第一中学2023-2024学年高一下学期第一阶段测试(选考)化学试题
名校
解题方法
9 . 下列有关离子的检验结论正确的是
A.取少量溶液于试管中,加入稀NaOH溶液后,将湿润红色石蕊试纸置于试管口,若不变蓝,则该溶液一定不含 |
B.取少量溶液于试管中,加入KSCN溶液,无明显现象,再加入 溶液,溶液变为红色,该溶液中含有 溶液,溶液变为红色,该溶液中含有 |
C.取少量溶液于试管中,用玻璃棒蘸取该溶液,灼烧,观察火焰焰色呈黄色,该溶液中含有 |
D.取少量溶液于试管中,滴入硝酸酸化的 溶液,有白色沉淀产生,说明溶液中一定含 溶液,有白色沉淀产生,说明溶液中一定含 |
您最近半年使用:0次
解题方法
10 . 下列方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究浓硫酸的特性 | 将浓硫酸滴到蔗糖表面,固体变黑膨胀,有刺激性气体产生 | 浓硫酸有脱水性和强氧化性 |
| B | 检验 和浓盐酸反应后是否有酸剩余 和浓盐酸反应后是否有酸剩余 | 取少量反应后的溶液于试管中,依次加入稀硝酸、 溶液,观察 溶液,观察 | 若产生大量白色沉淀,则说明盐酸有剩余 |
| C | 证明 有氧化性 有氧化性 | 将足量的 溶液滴入酸性高锰酸钾溶液中 溶液滴入酸性高锰酸钾溶液中 | 若溶液中的紫红色褪去,则证明 有氧化性 有氧化性 |
| D | 鉴别两种红棕色气体 和 和 | 向盛有 淀粉溶液的试管中通入气体 淀粉溶液的试管中通入气体 | 溶液变成蓝色,说明该气体是 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次