1 . X、Y、Z各代表一种物质,若X+Y=Z+H2O,则X和Y的反应不可能是
| A.盐和盐的反应 | B.酸与碱的反应 |
| C.碱性氧化物和酸性氧化物反应 | D.酸性氧化物和碱的反应 |
您最近一年使用:0次
2023-05-19更新
|
1920次组卷
|
6卷引用:江西省宜春市上高二中2022-2023学年高一上学期第一次月考化学试题
江西省宜春市上高二中2022-2023学年高一上学期第一次月考化学试题 河南省信阳高级中学(北湖校区)2023-2024学年高一上学期8月月考化学试题(已下线)专题01 物质的分类及转化【考点清单】(讲+练)(已下线)专题01 物质的分类及转化【考题猜想】(9大题型)湖北省孝感七县市一中联考协作体2023-2024学年高一上学期9月月考化学试题山西省实验中学2023-2024学年高一上学期第一次月考化学试题
名校
解题方法
2 . 下列离子方程式书写正确的是
A.氯化铁溶液与铜反应: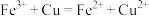 |
B. 在酸性条件下被 在酸性条件下被 氧化: 氧化: |
C.氯化铁溶液中加入足量的氨水: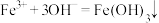 |
D. 溶于HI溶液: 溶于HI溶液: |
您最近一年使用:0次
2022-10-09更新
|
570次组卷
|
2卷引用:江西省赣州市赣县第三中学2022-2023学年高二上学期10月月考化学试题
3 . 某学习小组拟研究FeSO4的分解实验探究,请你利用所学知识帮该小组完成以下实验方案。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2;假设2:FeO、SO3、SO2;假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
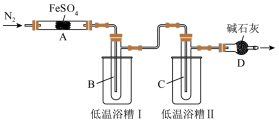
回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是_______ 。
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是_______ ,(只填操作),当A处固体完全分解后通入N2的目的是_______ 。
(3)低温浴槽I收集的物质是_______ (填化学式),低温浴槽II控制的温度范围为_______ 。
(4)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
甲组实验中A装置得到固体产物是_______ (填化学式)。
(5)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是_______ 。
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(6)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案_______ (填“1”或“2”)可行。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2;假设2:FeO、SO3、SO2;假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
| 物质 | SO3 | SO2 | O2 | N2 |
| 熔点/℃ | 16.8 | -72.4 | -218.4 | -209.9 |
| 沸点/℃ | 44.8 | -10 | -182.9 | -195.8 |

回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是
(3)低温浴槽I收集的物质是
(4)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
| 实验 | A处温度/℃ | FeSO4质量/g | 低温浴槽I净增质量/g | 低温浴槽II净增质量/g |
| 甲 | T1 | 3.04 | 0.80 | 0.64 |
| 乙 | T2 | 4.56 | 1.60 | 0.64 |
(5)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(6)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案
您最近一年使用:0次
名校
解题方法
4 . 以高硫铝土矿(主要成分为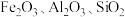 ,少量
,少量 和硫酸盐)为原料制备聚合硫酸铁
和硫酸盐)为原料制备聚合硫酸铁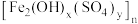 和明矾的部分工艺流程如下,下列说法错误的是
和明矾的部分工艺流程如下,下列说法错误的是
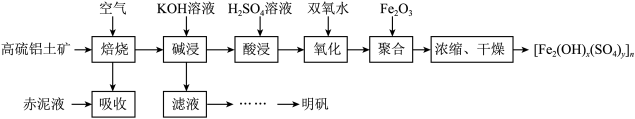
已知:赤泥液的主要成分为
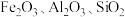 ,少量
,少量 和硫酸盐)为原料制备聚合硫酸铁
和硫酸盐)为原料制备聚合硫酸铁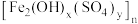 和明矾的部分工艺流程如下,下列说法错误的是
和明矾的部分工艺流程如下,下列说法错误的是
已知:赤泥液的主要成分为

A.赤泥液的作用是吸收“焙烧”阶段中产生的 |
B.聚合硫酸铁可用于净化自来水,与其组成中的 具有氧化性有关 具有氧化性有关 |
C.在“聚合”阶段,若增加 用量,会使 用量,会使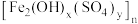 中x变小 中x变小 |
| D.从“滤液”到“明矾”的过程中还应有“除硅”步骤 |
您最近一年使用:0次
2022-05-12更新
|
828次组卷
|
7卷引用:江西省景德镇市第一中学2021-2022学年高二上学期期末(重点班)化学试题
江西省景德镇市第一中学2021-2022学年高二上学期期末(重点班)化学试题湖南省郴州市第一中学2022届高三下学期期中考试化学试题湖南省常宁市第一中学2022届高三下学期第三次模拟考试化学试题河南省大联考2022届高三上学期阶段性测试(一)化学试题(已下线)第二单元 化学物质及其变化(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)福建省龙岩第一中学2021-2022学年高三上学期第二次月考化学试题山西省怀仁市2021-2022学年高三上学期期中化学试题
名校
解题方法
5 . 向NaOH、NaAlO2的混合溶液中逐滴加入稀盐酸,生成沉淀的质量随稀盐酸加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是
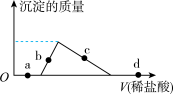

A.a点对应的溶液中: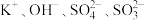 |
B.b点对应的溶液中: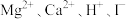 |
C.c点对应的溶液中: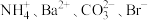 |
D.d点对应的溶液中: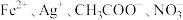 |
您最近一年使用:0次
2022-04-28更新
|
863次组卷
|
4卷引用:江西省赣州市于都县第二中学等六校2021-2022学年高二下学期期中考试化学试题
江西省赣州市于都县第二中学等六校2021-2022学年高二下学期期中考试化学试题(已下线)第03练 用分类思想突破离子反应-2022年【暑假分层作业】高二化学(2023届一轮复习通用)云南省楚雄州2021-2022学年高二下学期期末考试化学试题江西省丰城中学2022-2023学年高三上学期月考化学试题
名校
解题方法
6 . 河南省镁资源丰富,河南崮山镁业为国内最大的氧化镁生产企业,其利用蛇纹石制备的高纯氧化镁,颗粒细腻不结团。其工艺流程如下:
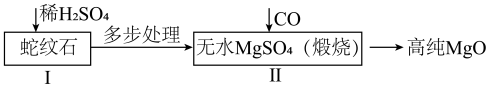
某校化学兴趣小组在实验室探究流程II中的反应原理,并检验产物纯度。回答下列问题:
(1)甲同学设计了如图实验装置探究流程II中的反应原理。
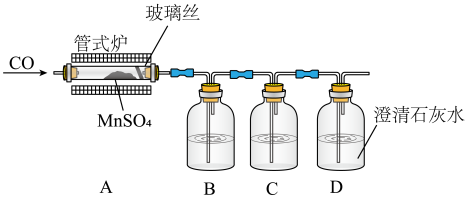
①检验气态产物中是否有SO2及SO3,则装置B、C中的溶液分别是_______ (填标号)。
a.Ba(NO3)2溶液 b.BaCl2溶液 c.浓硫酸 d.酸性高锰酸钾溶液
②实验过程中,装置B中没有明显现象,装置C、D中现象明显,写出A中发生反应的化学方程式:_______ 。
(2)丙同学利用反应:HCOOH CO↑+H2O为甲同学的实验提供CO气体,并设计以下实验装置图。
CO↑+H2O为甲同学的实验提供CO气体,并设计以下实验装置图。

①E装置中,仪器b的名称是_______ 。
②制备的CO气体中常含有杂质气体_______ 、挥发出来的少量甲酸蒸气及水蒸气,已知F装置中盛放的是NaOH溶液,则G装置的作用是_______ 。
(3)Mg2+的含量测定:向含Mg2+的溶液中加入铬黑T溶液(含Hlnd2-离子)作指示剂,用EDTA标准溶液(含H2Y2-离子)滴定。溶液中发生的反应如下:Mg2++Hlnd2-(天蓝色)=Mglnd-(酒红色)+H+,Mg2++H2Y2-=MgY2-+2H+。丁同学称取4.1g样品MgO,溶于稀硫酸,移入1000mL容量瓶中稀释至刻度。取20 mL溶液于锥形瓶中,加2滴铬黑T溶液,用0.1000mol·L-1EDTA溶液滴定,实验数据如下:
①滴定终点的现象是_______ 。
②计算4.1 g样品MgO中镁离子的物质的量为_______ mol(保留两位有效数字)。

某校化学兴趣小组在实验室探究流程II中的反应原理,并检验产物纯度。回答下列问题:
(1)甲同学设计了如图实验装置探究流程II中的反应原理。

①检验气态产物中是否有SO2及SO3,则装置B、C中的溶液分别是
a.Ba(NO3)2溶液 b.BaCl2溶液 c.浓硫酸 d.酸性高锰酸钾溶液
②实验过程中,装置B中没有明显现象,装置C、D中现象明显,写出A中发生反应的化学方程式:
(2)丙同学利用反应:HCOOH
 CO↑+H2O为甲同学的实验提供CO气体,并设计以下实验装置图。
CO↑+H2O为甲同学的实验提供CO气体,并设计以下实验装置图。
①E装置中,仪器b的名称是
②制备的CO气体中常含有杂质气体
(3)Mg2+的含量测定:向含Mg2+的溶液中加入铬黑T溶液(含Hlnd2-离子)作指示剂,用EDTA标准溶液(含H2Y2-离子)滴定。溶液中发生的反应如下:Mg2++Hlnd2-(天蓝色)=Mglnd-(酒红色)+H+,Mg2++H2Y2-=MgY2-+2H+。丁同学称取4.1g样品MgO,溶于稀硫酸,移入1000mL容量瓶中稀释至刻度。取20 mL溶液于锥形瓶中,加2滴铬黑T溶液,用0.1000mol·L-1EDTA溶液滴定,实验数据如下:
| 序号 | 1 | 2 | 3 | 4 |
| 标准溶液体积/mL | 20.10 | 18.40 | 19.90 | 20.00 |
②计算4.1 g样品MgO中镁离子的物质的量为
您最近一年使用:0次
名校
解题方法
7 . W、X、Y、Z是原子序数依次增大的短周期主族元素,原子序数总和为25,Y是地壳中含量最多的元素,由这四种元素形成的某化合物的结构如图所示。下列叙述正确的是
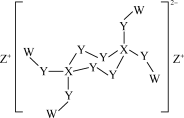
| A.原子半径大小:Z>Y>X>W |
| B.该化合物具有强氧化性,用于消毒杀菌 |
| C.X可与Y形成XY、XY2等共价化合物 |
| D.W分别与X、Y、Z形成的化合物所含化学键类型相同 |
您最近一年使用:0次
2022-03-29更新
|
2669次组卷
|
17卷引用:江西省景德镇一中2022-2023学年高二上学期期中考试化学试题
江西省景德镇一中2022-2023学年高二上学期期中考试化学试题安徽省安庆市第二中学2021-2022学年高二下学期期中考试化学试题黑龙江省实验中学 2021-2022学年高二下学期第一次月考化学试题吉林省吉林市第一中学2021-2022学年高二下学期6月月考化学试题(理科创新班)陕西省咸阳市2022届高考模拟检测(二模)理科综合化学试题山东省泰安市2022届高三二轮验收考试化学试题(已下线)化学-2022年高考考前押题密卷(湖南卷)广东省深圳外国语学校2021-2022学年高一下学期期中考试化学试题山西省太原市英才学校高中部2022-2023学年高三上学期12月第三次测试化学试题湖北省宜昌英杰学校2021-2022学年高三上学期9月月考化学试题山西省太原市第五中学校2022-2023学年高三上学期期末考试化学试题湖南省株洲市南方中学2023届高三第六次月考化学试题巩固训练8辽宁省沈阳市第一二〇中学2022-2023学年高一下学期期初质量监测化学试题四川省绵阳南山中学2023届高三下学期高考仿真考试理综化学试题湖南衡阳名校2024届高三一轮复习12月第2周周练 化学试题山东省营市胜利第一中学2023-2024学年高一下学期4月份阶段性测试化学试题
名校
解题方法
8 . 水合肼(N2H4·H2O)是一种重要的化工原料,其沸点约为118℃,具有强还原性,实验室将NaClO稀溶液缓慢滴加到CO(NH2)2和NaOH的混合溶液中制备水合肼,其流程如图所示,下列说法正确的是
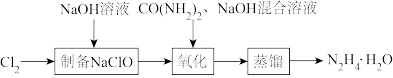
| A.“制备NaClO”过程中每消耗标准状况下2.24L Cl2,转移0.2mol电子 |
| B.“蒸馏”操作需要用到的冷凝仪器有球形冷凝管 |
| C.“氧化”步骤中药品的滴加顺序不能颠倒 |
D.“氧化”步骤中发生反应的离子方程式为 |
您最近一年使用:0次
2022-03-10更新
|
1275次组卷
|
8卷引用:江西省景德镇一中2021-2022学年高二下学期重点班期末考试化学试题
江西省景德镇一中2021-2022学年高二下学期重点班期末考试化学试题湖南省长沙市雅礼中学2021-2022学年高三下学期月考(六)化学试题(已下线)秘籍18 工艺流程新情景方程式书写-备战2022年高考化学抢分秘籍(全国通用)(已下线)2022年湖南卷高考真题变式题(1-10)(已下线)二轮专题强化练 专题8 常见无机物性质的转化(已下线)T10-物质反应及转化河南省洛阳市宜阳县第一高级中学2023-2024学年高一下学期竞赛选拔赛化学试题湖南省岳阳市岳汨联考2023-2024学年高三下学期5月月考化学试题
名校
解题方法
9 . 通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。已知:氨气能与水反应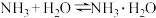 下列判断不正确的是
下列判断不正确的是
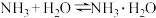 下列判断不正确的是
下列判断不正确的是| A.A、B、E中的一种肯定含有金属元素 | B.A为电解质,B为非电解质 |
| C.A和B中所含元素可以组成盐类物质 | D.能够确定该白色沉淀的化学组成 |
您最近一年使用:0次
2021-10-17更新
|
676次组卷
|
2卷引用:江西省景德镇市第一中学2021-2022学年高二上学期期末(重点班)化学试题
10 . 某同学探究Fe2+还原性的实验记录如下:
下列说法错误的是
| ① | ② | ③ |
 | 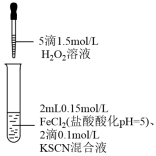 | 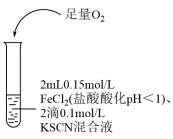 |
溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2)。取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀。 | 溶液变红且不褪色,有气体生成(经检验为O2),经检验有丁达尔效应。 | 溶液变红且不褪色,滴加盐酸和BaCl2溶液,无白色沉淀,经检验无丁达尔效应。 |
| A.对比①②,可以判定酸性越强,H2O2的氧化能力越强 |
| B.①中发生的氧化还原反应只有两种 |
| C.②中红色溶液中含有Fe(OH)3胶体 |
| D.③中发生的氧化还原反应为4Fe2++O2+4H+=4Fe3++2H2O |
您最近一年使用:0次
2021-10-09更新
|
1281次组卷
|
11卷引用:江西省景德镇市第一中学2021-2022学年高二上学期期末(重点班)化学试题
江西省景德镇市第一中学2021-2022学年高二上学期期末(重点班)化学试题湖南省宁远县第一中学2022-2023学年高二上学期第一次适应性考试化学试题(已下线)解密11 化学实验(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)湖南省永州市2023届高考第一次适应性考试化学试题(已下线)专题24 实验分析设计型选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)北京市海淀区第二十中学2022-2023学年高一上学期11月月考化学试题山东省滨州市2021届高三上学期期末考试化学试题(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)山东省六校(泰安一中、菏泽一中、章丘四中、东营一中、济宁一中、聊城一中、胜利一中)2022届高三“山东学情”10月联考化学试题A卷山东省六校(泰安一中、菏泽一中、章丘四中、东营一中、济宁一中、聊城一中、胜利一中)2022届高三“山东学情”10月联考化学试题B卷



