名校
解题方法
1 . 元素X、Q、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3︰4,M原子的最外层电子数与次外层电子数之比为3︰4;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,Q和Y在周期表中的位置相邻。请回答下列问题。
(1)M在元素周期表中的位置是___ ,写出Z的离子结构示意图:__ ;Q的简单氢化物的结构式为___ 。
(2)写出X、Y、R按原子个数之比1︰1︰1形成的化合物的化学式:___ 。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:___ 。
(4)写出单质R的一种工业用途:___ 。
(5)如图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,写出该转化过程的化学方程式:___ 。
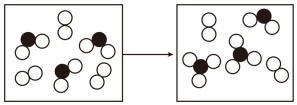
(6)科学家认为存在QX5这种物质,且预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式:___ 。
(1)M在元素周期表中的位置是
(2)写出X、Y、R按原子个数之比1︰1︰1形成的化合物的化学式:
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:
(4)写出单质R的一种工业用途:
(5)如图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,写出该转化过程的化学方程式:

(6)科学家认为存在QX5这种物质,且预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
2 . A~H均为短周期元素,A~F在元素周期表中的相对位置如图1所示,G与其他七种元素不在同一周期,H是短周期中原子半径最大的主族元素。由B、G构成的最简单化合物常作为氮肥工业和纯碱工业的原料。由上述某些元素组成的物质甲~戊的转化关系如图2所示。

已知图2中反应①是复分解反应,生成物中水已略去。请回答下列问题:
(1)上述元素组成的单质中,硬度最大的是_________________ (填该物质名称)。
(2)若戊是含有18电子的双原子分子,则丙的电子式为________________ ;在①中制取气体丙的化学方程式为_______________________________________________ 。
(3)若甲的水溶液呈碱性,丙的凝胶经干燥脱水后,常用作干燥剂,写出甲的一种用途:_____________________________ 。
(4)如果图2中反应①是置换反应,戊是单质,则戊不可能是_____________ 。 (填序母序号)
A、O2 B、Cl2 C、H2 D、N2

已知图2中反应①是复分解反应,生成物中水已略去。请回答下列问题:
(1)上述元素组成的单质中,硬度最大的是
(2)若戊是含有18电子的双原子分子,则丙的电子式为
(3)若甲的水溶液呈碱性,丙的凝胶经干燥脱水后,常用作干燥剂,写出甲的一种用途:
(4)如果图2中反应①是置换反应,戊是单质,则戊不可能是
A、O2 B、Cl2 C、H2 D、N2
您最近一年使用:0次
名校
3 . Ⅰ.几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期。(请用相应的化学用语答题 )
(1)R的元素符号为________ ;M在元素周期表中的位置为________________ 。
(2)X与Y按原子个数比1∶1构成的物质的电子式为________________ ;所含化学键类型__________________________ 。
(3)X+、Y2-、M2-离子半径大小顺序为__________________ 。
(4)将YM2通入FeCl3溶液中的离子方程式:_________________________________________ 。
Ⅱ.如图转化关系(A、B、C中含相同元素)
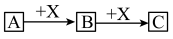
(1)若B为白色胶状不溶物,则A与C反应的离子方程式为_________________________ 。
(2)若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应生成B的离子方程式为_____________________________________________ 。
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(1)R的元素符号为
(2)X与Y按原子个数比1∶1构成的物质的电子式为
(3)X+、Y2-、M2-离子半径大小顺序为
(4)将YM2通入FeCl3溶液中的离子方程式:
Ⅱ.如图转化关系(A、B、C中含相同元素)

(1)若B为白色胶状不溶物,则A与C反应的离子方程式为
(2)若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应生成B的离子方程式为
您最近一年使用:0次
2019-05-11更新
|
168次组卷
|
2卷引用:【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二下学期期中考试化学试题
名校
4 . Ⅰ.形式一:(由粒子数推断)A+、B+、C-、D、E5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①A++ C-→D+E;②B++C-→2D。据此,回答下列问题:写出A+、B+的化学式:____________ 、____________ 。
Ⅱ. 形式二:(由元素原子结构推断)A、B、C、D、E、F的原子序数依次增大,它们都是同周期的元素。已知:A、C、F三种原子最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多2。
(1)写出下列元素的符号:A________ ,B________ ,E________ 。
(2)F在元素周期表中的位置为___________________________________ 。
(3)写出C的单质和A的最高价氧化物的水化物反应的离子方程式_______ 。
(4)元素的非金属性为(原子的得电子能力):E________ F(填“强于”或“弱于”),请以E、F为例列举元素非金属性强弱的比较方法_________________ 、___________________ (至少2条)。
(学法题)通过Ⅱ的解题你认为推断出本题各元素的关键环节为___________ 。
III.形式三:(由元素位置推断)下表为元素周期表的一部分:
请参照元素①-⑧在表中的位置,用化学用语 回答下列问题:
(1)请画出元素⑦的离子结构示意图________________ 。
(2)写出元素⑤在周期表中的位置______________ 。
(3)②、③、⑥的离子半径由大到小的顺序为_________________________ 。
(4)⑤、⑥、⑦的最高价氧化物对应水化物酸性由强到弱的顺序是______ 。
(5)①、②、③三种元素形成化合物与④的最高价氧化物反应的离子方程式为_________ 。
(6)请你预测:如果发现了原子序数为116号元素,它在周期表中的位置是第________ 周期_______ 族,它属于_____ 元素(填“金属”或“非金属”)。
Ⅱ. 形式二:(由元素原子结构推断)A、B、C、D、E、F的原子序数依次增大,它们都是同周期的元素。已知:A、C、F三种原子最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多2。
(1)写出下列元素的符号:A
(2)F在元素周期表中的位置为
(3)写出C的单质和A的最高价氧化物的水化物反应的离子方程式
(4)元素的非金属性为(原子的得电子能力):E
(学法题)通过Ⅱ的解题你认为推断出本题各元素的关键环节为
III.形式三:(由元素位置推断)下表为元素周期表的一部分:
| 族 周期 | ||||||||
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
(1)请画出元素⑦的离子结构示意图
(2)写出元素⑤在周期表中的位置
(3)②、③、⑥的离子半径由大到小的顺序为
(4)⑤、⑥、⑦的最高价氧化物对应水化物酸性由强到弱的顺序是
(5)①、②、③三种元素形成化合物与④的最高价氧化物反应的离子方程式为
(6)请你预测:如果发现了原子序数为116号元素,它在周期表中的位置是第
您最近一年使用:0次
5 . 下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:a.A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。b.反应①②是化工生产中的重要反应。c.化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。d.化合物L具有漂白性,可由Cl2与NaOH溶液反应制得。e.化合物J由两种元素组成,其相对分子质量为32。
请按要求填空:
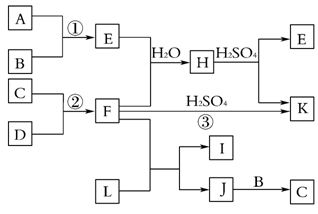
(1)A元素在元素周期表中的位置____________________ 。
(2)反应③的化学方程式:________________________ 。
(3)C的结构式:________________________ ;
F的一种用途:_________________________ 。
(4)L的溶液与化合物E反应的离子方程式:_________ 。
(5)化合物J的化学式:________________________ 。
请按要求填空:

(1)A元素在元素周期表中的位置
(2)反应③的化学方程式:
(3)C的结构式:
F的一种用途:
(4)L的溶液与化合物E反应的离子方程式:
(5)化合物J的化学式:
您最近一年使用:0次
2019-01-30更新
|
1077次组卷
|
2卷引用:2014-2015江西省新余市第一中学高一4月月考化学试卷
名校
解题方法
6 . A、B、C、D、E、F、G均为常见短周期元素,原子序数依次递增。已知A、B、C能分别与D 组成二元化合物K、L、M,甲、乙分别是B、D的单质,常温下分别是常见的固体和气体,化合物M是产生光化学烟雾的主要气体之一,丙是C的最高价氧化物对应的水化物,它们之间有如图所示转化关系。E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
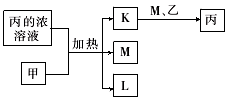
(1)C在元素周期表中的位置为_________ 。
(2)甲与丙的浓溶液反应的化学方程式_______________ 。
(3)D与E按原子个数比1:1形成化合物的电子式为________ ,其与水发生反应的化学方程式是_______________ 。
(4)E、F、G形成的简单离子,半径由大到小顺序是________ (用离子符号表示)。B、F、G元素的非金属性由强到弱的顺序__________ (用元素符号表示)。

(1)C在元素周期表中的位置为
(2)甲与丙的浓溶液反应的化学方程式
(3)D与E按原子个数比1:1形成化合物的电子式为
(4)E、F、G形成的简单离子,半径由大到小顺序是
您最近一年使用:0次
2018-07-16更新
|
244次组卷
|
5卷引用:【全国市级联考】山东省烟台市2017-2018学年高一下学期期末考试化学试题
名校
7 . 元素X、Q、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,Q和Y在周期表中的位置相邻,请回答下列问题:
(1)M在元素周期表中的位置_________________ ,写出Z的离子结构示意图___________ 。
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式________________ 。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式__________________________________ 。
(4)写出单质R的一种工业用途_______________________ 。
(5)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,写出该转化过程的化学方程式为____________________ 。
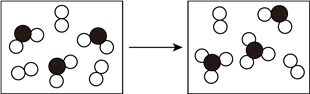
(6)由X、Y、Z、M四种元素组成的一种离子化合物A,已知A,既能与盐酸反应,又能与氢氧化钠溶液反应,还能和氯水反应,写出A与氯水反应的离子方程式___________ 。
(7)科学家认为存在QX5这种物质,且预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式___________________________ ,已知QX5中含有离子键和极性键,写出它的电子式______________ 。
(1)M在元素周期表中的位置
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式
(4)写出单质R的一种工业用途
(5)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,写出该转化过程的化学方程式为

(6)由X、Y、Z、M四种元素组成的一种离子化合物A,已知A,既能与盐酸反应,又能与氢氧化钠溶液反应,还能和氯水反应,写出A与氯水反应的离子方程式
(7)科学家认为存在QX5这种物质,且预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式
您最近一年使用:0次
名校
解题方法
8 . 元素X、Y、Z、M、N均为原子序数依次增大的短周期主族元素;R在地壳金属元素中的含量仅次于Z。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4;N-、Z3+、X+离子半径逐渐减小;化合物XN常温下为气体,请回答下列问题:
(1)R在元素周期表中的位置是____________ ;Z3+的离子结构示意图是____________ 。
(2)写出X、Y、N按原子个数之比1:1:1:形成的化合物的电子式__________ ;M和N气态氢化物的稳定性大小比较为________ (用化学式和“>”“<”或“=”表示)。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式__________________________________ .
(4)Z元素的单质能与Y和R形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为_____________________________ 。
(5)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,在该转化关系中还原剂是__________ (填化学式),示意图中转移电子的数目为______ 。
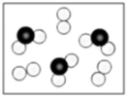


(6)由X、Y、M三种元素组成的离子,在水溶液中与H+和OH-均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式_______________________ 。
(1)R在元素周期表中的位置是
(2)写出X、Y、N按原子个数之比1:1:1:形成的化合物的电子式
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式
(4)Z元素的单质能与Y和R形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为
(5)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,在该转化关系中还原剂是



(6)由X、Y、M三种元素组成的离子,在水溶液中与H+和OH-均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式
您最近一年使用:0次
2017-12-08更新
|
236次组卷
|
3卷引用:山东省烟台市2018届高三上学期期中考试化学试题
名校
9 . 下图转化关系中,A、B、G、Y都是主族元素组成的单质,其余均是化合物。通常条件下B、E、F、Y均为气体;A、C、H焰色反应均呈黄色;E、F相遇会产生白烟。

请按要求回答下列问题:
(1)化合物F的电子式_______________ 。
(2)G在元素周期表中位置_______________ 。
(3)以上反应既属于化合又属于氧化还原反应的有________________ (填反应编号)。
(4)E与F反应的化学方程式为________________________________________ ;
加热条件下C与D的溶液反应的离子反应方程式为_______________________ 。
(5)G与C的溶液发生反应的离子方程式为_____________________________ 。

请按要求回答下列问题:
(1)化合物F的电子式
(2)G在元素周期表中位置
(3)以上反应既属于化合又属于氧化还原反应的有
(4)E与F反应的化学方程式为
加热条件下C与D的溶液反应的离子反应方程式为
(5)G与C的溶液发生反应的离子方程式为
您最近一年使用:0次
名校
10 . I .短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为 。
。
请回答下列问题:
(1)Z元素在元素周期表中的位置是________________________________________ 。
(2)X、Y、Z三种元素的原子半径由大到小的顺序为_________________ (元素符号表示)。
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为____________ (用化学式表示)
(4)用电子式表示WY2的形成过程:__________________________________ 。
(5)写出W单质与浓硫酸反应的化学方程式:__________________________________。
Ⅱ. A、B、C三种物质存在如图转化关系。

(6)若B为白色胶状不溶物,则A与C反应的离子方程式为____________________________ 。
(7)向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为__________________________________ 。
 。
。| W | X | Y |
| Z |
(1)Z元素在元素周期表中的位置是
(2)X、Y、Z三种元素的原子半径由大到小的顺序为
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)用电子式表示WY2的形成过程:
(5)写出W单质与浓硫酸反应的化学方程式:__________________________________。
Ⅱ. A、B、C三种物质存在如图转化关系。

(6)若B为白色胶状不溶物,则A与C反应的离子方程式为
(7)向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为
您最近一年使用:0次



