名校
解题方法
1 .  是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:
实验(一)制备 。
。
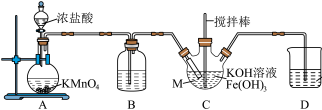
(1)仪器M的名称是_____ ,装置B的作用是_____ 。
(2)装置C中生成 的化学方程式为
的化学方程式为_____ 。
(3)实验得知装置D中吸收的 为装置A中生成
为装置A中生成 的25%,不考虑其他消耗,若装置D中生成的氧化产物只有
的25%,不考虑其他消耗,若装置D中生成的氧化产物只有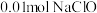 ,则生成
,则生成_____ 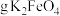 。
。
实验(二)探究 的性质。
的性质。

实验中观察到b中溶液变为蓝色,a中溶液由紫红色变为黄色,并产生气泡。
(4)酸R选择稀硫酸,不选择盐酸,其主要原因是_____ ;酸R选择稀硫酸时,从d口逸出的气体_____ (填“可以”或“不可以”)直接排放至大气中。
(5)当选用硫酸时,装置a中的离子方程式为_____ 。
(6)另设计一种方案确认有 产生:
产生:_____ 。
(7)向另一试管中的 溶液中滴加
溶液中滴加 溶液,溶液变为紫红色。不能证明氧化性:
溶液,溶液变为紫红色。不能证明氧化性: ,其原因是
,其原因是_____ 。
 是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:实验(一)制备
 。
。
(1)仪器M的名称是
(2)装置C中生成
 的化学方程式为
的化学方程式为(3)实验得知装置D中吸收的
 为装置A中生成
为装置A中生成 的25%,不考虑其他消耗,若装置D中生成的氧化产物只有
的25%,不考虑其他消耗,若装置D中生成的氧化产物只有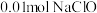 ,则生成
,则生成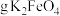 。
。实验(二)探究
 的性质。
的性质。
实验中观察到b中溶液变为蓝色,a中溶液由紫红色变为黄色,并产生气泡。
(4)酸R选择稀硫酸,不选择盐酸,其主要原因是
(5)当选用硫酸时,装置a中的离子方程式为
(6)另设计一种方案确认有
 产生:
产生:(7)向另一试管中的
 溶液中滴加
溶液中滴加 溶液,溶液变为紫红色。不能证明氧化性:
溶液,溶液变为紫红色。不能证明氧化性: ,其原因是
,其原因是
您最近一年使用:0次
2023-09-28更新
|
89次组卷
|
2卷引用:湖南省三湘创新发展联合体2023-2024学年高三上学期9月月考化学试题
名校
解题方法
2 . 某硫酸厂以硫铁矿焙烧后的烧渣(其主要成分为 、
、 、
、 )为原料来制取铵明矾晶体
)为原料来制取铵明矾晶体 的一种工艺流程如图。
的一种工艺流程如图。
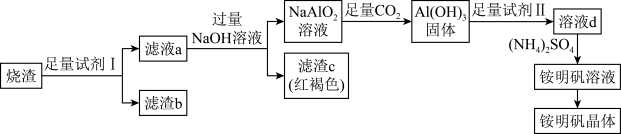
已知:① 是酸性氧化物,难溶于水,酸浸时不发生反应。
是酸性氧化物,难溶于水,酸浸时不发生反应。
② 固体可溶于
固体可溶于 等强碱溶液。
等强碱溶液。
请回答下列问题:
(1)写出 中含有的化学键类型:
中含有的化学键类型:_______ 。
(2)“试剂Ⅰ”为_______ (填试剂名称),“滤渣b”为_______ (填化学式)。
(3)写出“滤液a”和 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 、_______ 。
(4)“滤渣c”的化学式为_______ ,证明铁元素已沉淀完全的实验方法是_______ 。
(5)向 溶液中通入足量
溶液中通入足量 的离子方程式为
的离子方程式为_______ 。
(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、_______ (填操作名称)、洗涤、干燥。
 、
、 、
、 )为原料来制取铵明矾晶体
)为原料来制取铵明矾晶体 的一种工艺流程如图。
的一种工艺流程如图。
已知:①
 是酸性氧化物,难溶于水,酸浸时不发生反应。
是酸性氧化物,难溶于水,酸浸时不发生反应。②
 固体可溶于
固体可溶于 等强碱溶液。
等强碱溶液。请回答下列问题:
(1)写出
 中含有的化学键类型:
中含有的化学键类型:(2)“试剂Ⅰ”为
(3)写出“滤液a”和
 溶液反应的离子方程式:
溶液反应的离子方程式:(4)“滤渣c”的化学式为
(5)向
 溶液中通入足量
溶液中通入足量 的离子方程式为
的离子方程式为(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、
您最近一年使用:0次
名校
解题方法
3 . 实验小组制备高铁酸钾( )并探究其性质。
)并探究其性质。
资料: 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生
为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
(1)制备 。(夹持装置略)
。(夹持装置略)
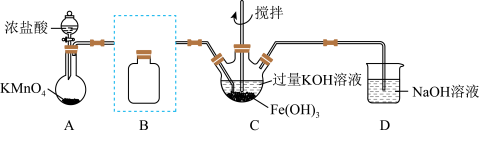
①A为氯气发生装置,A中反应的离子方程式是_______ 。
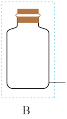
②将除杂装置B补充完整并标明所用试剂_______ 。
③C中得到紫色固体和溶液,C中 发生的反应有
发生的反应有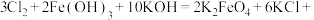
 ,另外还有
,另外还有_______ 。
(2)探究 的性质
的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有 。为证明是否
。为证明是否 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:
ⅰ.向沸水中逐滴滴加1mol/L  溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是
溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是_______ nm。
ⅱ.由方案上可知a中含有 离子,但该离子的产生不能判断一定是
离子,但该离子的产生不能判断一定是 将
将 氧化,还可能由
氧化,还可能由_______ 产生(用离子方程式表示)。
ⅲ.方案Ⅱ可证明 氧化了
氧化了 用KOH溶液洗涤的目的是
用KOH溶液洗涤的目的是_______ 。
②根据 的制备实验得出:氧化性
的制备实验得出:氧化性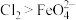 ,而方案Ⅱ实验表明,
,而方案Ⅱ实验表明, 和
和 的氧化性强弱关系相反,原因可能是
的氧化性强弱关系相反,原因可能是_______ 。
 )并探究其性质。
)并探究其性质。资料:
 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生
为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。(1)制备
 。(夹持装置略)
。(夹持装置略)
①A为氯气发生装置,A中反应的离子方程式是
②将除杂装置B补充完整并标明所用试剂

③C中得到紫色固体和溶液,C中
 发生的反应有
发生的反应有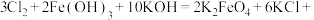
 ,另外还有
,另外还有(2)探究
 的性质
的性质①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有
 。为证明是否
。为证明是否 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:| 方案Ⅰ | 取少量a,经过检验溶液中含有 。 。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将 溶出,得到紫色溶液b,取少量b,滴加盐酸,有 溶出,得到紫色溶液b,取少量b,滴加盐酸,有 产生。 产生。 |
 溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是
溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是ⅱ.由方案上可知a中含有
 离子,但该离子的产生不能判断一定是
离子,但该离子的产生不能判断一定是 将
将 氧化,还可能由
氧化,还可能由ⅲ.方案Ⅱ可证明
 氧化了
氧化了 用KOH溶液洗涤的目的是
用KOH溶液洗涤的目的是②根据
 的制备实验得出:氧化性
的制备实验得出:氧化性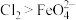 ,而方案Ⅱ实验表明,
,而方案Ⅱ实验表明, 和
和 的氧化性强弱关系相反,原因可能是
的氧化性强弱关系相反,原因可能是
您最近一年使用:0次
名校
解题方法
4 . 某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
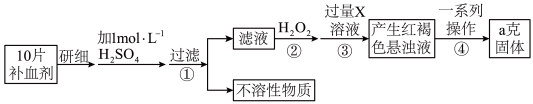
请回答下列问题:
Ⅰ、
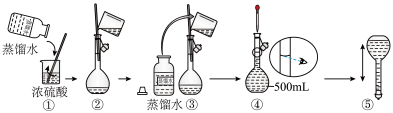
(1)实验时用 的浓硫酸,配制100mL
的浓硫酸,配制100mL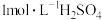 溶液,所需浓硫酸的体积为
溶液,所需浓硫酸的体积为___________ mL(计算结果精确到小数点后一位)。
(2)下列操作中,容量瓶所具备的功能有___________(填序号)。
(3)在下列配制过程示意图中,有错误的是(填写序号)___________ 。
(4)下列说法正确的___________。
Ⅱ、
(5)步骤②加入过量 的目的:
的目的:___________ 。发生反应的离子方程式为:___________ 。
(6)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a、___________ ,b、洗涤,c、灼烧,d、冷却
(7)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为___________ g。

请回答下列问题:
Ⅰ、
(1)实验时用
 的浓硫酸,配制100mL
的浓硫酸,配制100mL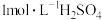 溶液,所需浓硫酸的体积为
溶液,所需浓硫酸的体积为(2)下列操作中,容量瓶所具备的功能有___________(填序号)。
| A.配制一定体积准确浓度的标准溶液 | B.长期贮存溶液 |
| C.用来溶解固体溶质 | D.常用来代替量筒量取一定体积的液体 |

(4)下列说法正确的___________。
| A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差 |
| B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低 |
| C.定容时仰视观察,所配溶液浓度会偏低 |
| D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可 |
Ⅱ、
(5)步骤②加入过量
 的目的:
的目的:(6)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a、
(7)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为
您最近一年使用:0次
2023-01-10更新
|
195次组卷
|
3卷引用:湖南省邵阳市第二中学2023-2024学年高一上学期第二次月考化学试题
名校
解题方法
5 . 如图为  在
在 和
和 气氛中的热重曲线(样品质量随温度变化的曲线)。下列有关说法错误的是
气氛中的热重曲线(样品质量随温度变化的曲线)。下列有关说法错误的是
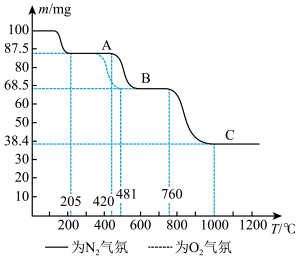
 在
在 和
和 气氛中的热重曲线(样品质量随温度变化的曲线)。下列有关说法错误的是
气氛中的热重曲线(样品质量随温度变化的曲线)。下列有关说法错误的是
A.无论是 气氛还是 气氛还是 气氛,当 气氛,当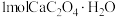 最终转变为 最终转变为 时,转移电子的物质的量相同 时,转移电子的物质的量相同 |
B.无论是 气氛还是 气氛还是 气氛, 气氛, 阶段均发生了氧化还原反应,但两者的气态产物不同 阶段均发生了氧化还原反应,但两者的气态产物不同 |
C.物质 为 为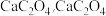 在隔绝空气条件下, 在隔绝空气条件下, 以下热稳定,不会分解 以下热稳定,不会分解 |
D.在酸性 溶液中加入少量 溶液中加入少量 固体样品时,溶液褪色且有少量气泡产生 固体样品时,溶液褪色且有少量气泡产生 |
您最近一年使用:0次
2021-11-24更新
|
738次组卷
|
3卷引用:湖南省长沙市第一中学2022-2023学年高三下学期月考(八)化学试题
湖南省长沙市第一中学2022-2023学年高三下学期月考(八)化学试题重庆市缙云教育联盟2021-2022学年高二11月质量检测化学试题(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)
19-20高一·浙江·期中
名校
6 . 下列说法不正确的是
| A.某硝酸密度为1.42g·cm-3,质量分数为63%,此硝酸物质的量浓度为14.2 mol·L-1 |
| B.100 g浓度为c mol·L-1 的硫酸中加入一定的水稀释成0.5c mol·L-1, 则加入水的体积大于100 mL(已知硫酸的浓度越大,其密度越大) |
| C.将a%的氨水和(100-a)%的氨水等体积混合后,所得溶液的质量分数可能为小于或等于50%(已知氨水的浓度越大,其密度越小) |
D.VLAl2(SO4)3溶液中含Al3+mg,则溶液中 的物质的量浓度为 的物质的量浓度为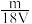 mol·L-1 mol·L-1 |
您最近一年使用:0次
2020-12-16更新
|
2356次组卷
|
4卷引用:湖南省邵阳市第二中学2023-2024学年高一上学期基础知识竞赛化学试题



